
 的说法中正确的是( )
的说法中正确的是( )| A. | 所有碳原子都在同一平面上 | |
| B. | 最多只可能有9个碳原子在同一平面上 | |
| C. | 只可能有5个碳原子在同一直线上 | |
| D. | 可能有6个碳原子在同一直线上 |
科目:高中化学 来源: 题型:选择题
| A. | 糖类的分子通式为 Cm(H2O)n | B. | 糖类物质都有甜味 | ||
| C. | 蔗糖不是淀粉水解的产物 | D. | 糖类一般都能水解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应①为氧化还原反应,反应②为复分解反应 | |
| B. | 反应①中物质氧化性的强弱顺序是:NaClO>Na2FeO4>FeCl3 | |
| C. | 若有2mol FeCl3 发生反应,转移电子的物质的量为 6mol | |
| D. | Na2FeO4能杀菌消毒是因为溶于水产生Fe(OH)3胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向能使pH试纸显深蓝色的溶液中通入少量二氧化碳:OH-+CO2═HCO3- | |
| B. | 向NaClO溶液中加入浓氢溴酸:ClO-+2H++2 Br-═Cl-+Br2+H2O | |
| C. | 向NaClO溶液中通入少量二氧化碳:2ClO-+CO2+H2O═2HClO+CO32- | |
| D. | 向FeBr2溶液中滴加少量Cl2溶液:2 Br-+Cl2═Br2+2Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 空气质量监测中的PM2.5是指大气中直径小于或等于2.5微米的颗粒物,也称可入肺颗粒物 | |
| B. | 采用纳米TiO2光触媒技术,将汽车尾气中的NO和CO转化为无害气体 | |
| C. | 大量排放SO2或CO2都会导致酸雨的形成 | |
| D. | 利用太阳能、潮汐能、风力发电,以获取清洁能源减少污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
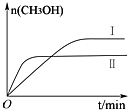 研究CO2的利用对促进低碳社会的构建具有重要的意义.
研究CO2的利用对促进低碳社会的构建具有重要的意义.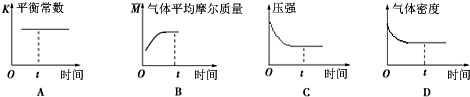
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 强电解质溶液的导电能力一定比弱电解质溶液强 | |
| B. | 中和等体积、等物质的量浓度的盐酸和醋酸溶液,盐酸所需氢氧化钠等于醋酸 | |
| C. | 将氢氧化钠和氨水溶液各稀释一倍,两者的OH-浓度均减少到原来的$\frac{1}{2}$ | |
| D. | 如果盐酸的浓度是醋酸浓度的二倍,则盐酸的H+浓度也是醋酸的二倍 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com