
如右图所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向烧杯中央滴入浓CuSO4溶液,一段时间后,下列有关杠杆的偏向判断正确的是(实验过程中,不考虑铁丝反应及两球的浮力变化)( )
A.杠杆为导体和绝缘体时,均为A端高B端低
B.杠杆为导体和绝缘体时,均为A端低B端高
C.当杠杆为绝缘体时,A端低,B端高;为导体时,A端高,B端低
D.当杠杆为绝缘体时,A端高,B端低;为导体时,A端低,B端高

科目:高中化学 来源: 题型:
下面有关氧化还原反应的叙述正确的是( )。
A.金属单质在反应中只作还原剂
B.非金属单质在反应中只作氧化剂
C.金属原子失电子越多其还原性越强
D.Cu2+比Fe2+的氧化性强,Fe比Cu的还原性强
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
①漂白粉、水玻璃和铝热剂都是混合物;
②煤的干馏和石油的分馏都是化学变化;
③氨基酸、纯碱、芒硝和生石灰分别属于酸、碱、盐和氧化物;
④非极性键也可能存在于离子化合物中
A.①④ B.①③ C.②④ D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是( )
A.焓是与内能有关的物理量,当反应在恒压条件下进行时,反应热效应等于焓
B.当能量变化以热的形式表现时,将反应分为放热反应和吸热反应
C.测定中和反应的反应热时,为提高实验准确性,使用稍过量的碱
D.新能源有太阳能、氢能、风能、生物质能等,它们都是可再生的
查看答案和解析>>
科目:高中化学 来源: 题型:
根据以下3个热化学方程式,下列有关Q1、Q2、Q3三者关系的判断中正确的是
2H2S(g)+3O2(g)=2SO2(g)+2H2O(l) ΔH=―Q1 kJ/mol
2H2S(g)+O2(g)=2S(s)+2H2O(l) ΔH=―Q2 kJ/mol
2H2S(g)+O2(g)=2S(s)+2H2O(g) ΔH=―Q3 kJ/mol
A. Q1>Q2>Q3 B. Q1>Q3>Q2
C. Q3>Q2>Q1 D. Q2>Q1>Q3
查看答案和解析>>
科目:高中化学 来源: 题型:
新型高能钠硫电池以熔融的钠、硫为电极,以导电的陶瓷为固体电解质。该电池放电时为原电池,充电时为电解池,反应原理为:2Na+xS Na2Sx。
Na2Sx。
(1)放电时Na发生_______反应,S作________极。
(2)充电时Na所在电极与直流电源的__________极相连。
(3)放电时负极反应为___________________________________________________;
充电时阳极反应为__________________________________________________。
(4)用此电池作电源电解饱和NaCl溶液,当阳极产生33.6 L(标准状况)气体时,消耗金属Na的质量为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
关于氢键,下列说法正确的是
A.含氢元素的化合物中一定有氢键
B.因为分子间存在氢键的缘故, 比
比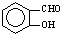 熔沸点高
熔沸点高
C.由于氢键比范德华力强,所以H2O分子比H2S分子稳定
D.“可燃冰”——甲烷水合物(例如:8CH4·46H2O)中CH4与H2O之间存在氢键
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期主族元素X、Y、Z、R、W的原子序数逐渐增大,X原子的p轨道半充满,且X、Y、Z同周期,Y与R的价电子数相同。
(1)在化合物YZ2中中心原子的VSEPR模型为_______________,Y与Na的离子半径由小到大的顺序为______________;
(2)X 的常见氢化物的空间构型是_____________,它的另一氢化物 X2H4 是一种火箭燃料的成分,其电子式是___________________;
(3)R、W两元素电负性较强的是(写元素符号) _______;写出证明这一结论的一个
实验事实(用化学方程式表示) ;
(4)W的含氧酸有多种,写出其中两种的分子式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
图中X、Y、Z为单质,其他为化学物,它们之间存在如下转化关系(部分产物已略去)。其中,A俗称磁性氧化铁;E是不溶于水的酸性氧化物,能与氢氟酸反应。
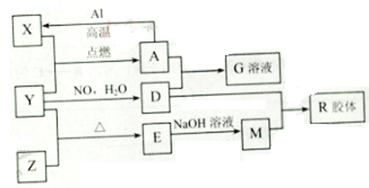
回答下列问题:
(1)组成单质Y的元素在周期表中的位置是 ;M中存在的化学键类型为 ;R的化学式是 。
(2)一定条件下,Z与H2反应生成ZH4,ZH4的电子式为 。
(3)已知A与1molAl反应转化为X时(所有物质均为固体)。放出aKJ热量。写出该反应的热化学方程式:
。
(4)写出A和D的稀溶液反应生成G的离子方程式:
(5)向含4mol D的稀溶液中,逐渐加入X粉末至过量。假设生成的气体只有一种,请在坐标系中画出n(X2+)随n(X)变化的示意图,并标出n(X2+)的最大值。
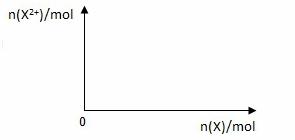

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com