
����Ŀ���Ӻ�ˮ����Ҫ��ˮ���Ȼ��ƣ�����������þ���ӵȣ�����ȡþ���ɰ����²�����У�
�ٰѱ��ǣ���Ҫ�ɷ�̼��ƣ��Ƴ�ʯ���飨�������Ƶ�����Һ����
��������ĺ�ˮ�м���ʯ���飬���������ˡ�ϴ�ӳ������Ҫ��������þ����
�۽������������ᷴӦ���ᾧ���ˡ���HCl�����Χ�и������õ��Ȼ�þ���
�ܽ��õ��IJ������ڵ��õ�þ��
����˵������ȷ����
A. ��ˮ�м����������������ɫ����
B. ��������漰�������ӷ�Ӧ����ʽΪ2OH��+Mg2��=Mg(OH)2��
C. �٢ڢ۲����漰���ϡ��ֽ���ֽⷴӦ
D. �ڢܲ��ķ�Ӧ���ڷֽⷴӦҲ��������ԭ��Ӧ
���𰸡�B
��������
A����ˮ����Ҫ����Na+��Cl-�����ӣ���ˮ�м���������������Ȼ�����ɫ������A����ȷ��
B. �����������ĺ�ˮ�м���ʯ��������������þ�����ӷ���ʽΪ��Ca(OH)2+Mg2��=Mg(OH)2��+Ca2+��B�����
C. ������漰�ķ�Ӧ����ʽΪCaCO3![]() CaO��CO2�������ڷֽⷴӦ��������CaO��ˮ��Ӧ��������Һ�������ƣ����ڻ��Ϸ�Ӧ��������漰�����ӷ���ʽΪ��Ca(OH)2+Mg2��=Mg(OH)2��+Ca2+���Լ�������н������������ᷴӦ�����Ȼ�þ��ˮ�����漰���ֽⷴӦ��C����ȷ��
CaO��CO2�������ڷֽⷴӦ��������CaO��ˮ��Ӧ��������Һ�������ƣ����ڻ��Ϸ�Ӧ��������漰�����ӷ���ʽΪ��Ca(OH)2+Mg2��=Mg(OH)2��+Ca2+���Լ�������н������������ᷴӦ�����Ȼ�þ��ˮ�����漰���ֽⷴӦ��C����ȷ��
D. �ڢܲ��ķ�ӦΪ����Ȼ�þ����þ�������Ĺ��̣����ڷֽⷴӦ���л��ϼ۵�������Ҳ��������ԭ��Ӧ��D����ȷ��
��ѡB��


 �㾦�½̲�ȫ�ܽ��ϵ�д�
�㾦�½̲�ȫ�ܽ��ϵ�д� Сѧ�̲���ȫ���ϵ�д�
Сѧ�̲���ȫ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ȼ�ѧ����ʽ�е���H��С����
A. NaOH (aq) + HCl (aq) ===NaCl (aq) + H2O (l)�� ��H1
B. NaOH (aq) + ![]() H2SO4 (aq) ===
H2SO4 (aq) ===![]() Na2SO4 (aq) + H2O (l)�� ��H2
Na2SO4 (aq) + H2O (l)�� ��H2
C. CH3COOH (aq) + NaOH (aq) ===CH3COONa (aq) + H2O (l)�� ��H3
D. NaOH (aq) + ![]() H2SO4 (Ũ) ===
H2SO4 (Ũ) ===![]() Na2SO4 (aq) + H2O (l)�� ��H4
Na2SO4 (aq) + H2O (l)�� ��H4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪25��ʱ�й�����ĵ���ƽ�ⳣ�����±�:
���ữѧʽ | HA | H2B |
����ƽ�ⳣ��/ mol/ L | Ka=1.7��10-6 | Ka1=1.3��10-3 Ka2=5.6��10-8 |
������˵����ȷ����
A. �����ʵ���Ũ�ȵĸ���ҺpH��ϵΪ��pH(Na2B)>pH(NaHB)>pH(NaA)
B. ����Ũ�ȵ� HA��Һ��NaA��Һ�������ϣ����Һ�У�c(A-)<c(Na+)
C. �� Na2B��Һ�м��������� HA��Һ������Ӧ�����ӷ���ʽΪ��B2-+2HA=2A-+H2B
D. NaHB��Һ�в�����Ũ�ȵĹ�ϵΪ��c(Na+)=c(HB-) +c(H2B)+c(B2-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ǰ��ԴΣ����һ��ȫ�������⣬��Դ������Ӧ����ԴΣ������Ҫ�ٴ롣
��1������������������Դ����Դ����������________(����ĸ)��
A��������չũ���������������Ľո�ת��Ϊ����Ч����Դ
B����������ú��ʯ�ͺ���Ȼ������������������������Դ����
C������̫���ܡ�ˮ�ܡ����ܡ������ܵ�����Դ������ʹ��ú��ʯ�͵Ȼ�ʯȼ��
D��������Դ���ģ��Ӵ���Դ���ظ�ʹ�á���Դ��ѭ������
��2�����ʯ��ʯī��Ϊ̼��ͬ�������壬��������������ʱȼ������һ����̼������������ʱ���ȼ�����ɶ�����̼����Ӧ�зų���������ͼ��ʾ��

����ͨ��״���£����ʯ��ʯī��Ƚϣ�________(�������ʯ������ʯī��)���ȶ���ʯī��ȼ������H��________��
��3����֪��N2��O2�����л�ѧ���ļ��ֱܷ���946kJ/mol��497kJ/mol��N2(g)��O2(g)=2NO(g)����H= +180.0kJ/mol��NO�����л�ѧ���ļ���Ϊ__________________kJ/mol��
��4���ۺ������й���Ϣ����д����CO��ȥNO��������Ⱦ������Ȼ�ѧ����ʽ��_______________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ȼ���ͭ��һ����Ҫ�Ļ�����Ʒ���������л��ϳɴ����������������ϣ������ȹ�ҵ���������ϵ�֪��CuCl��һ�ְ�ɫ���壬����ˮ�������ھƾ���������Ũ���ᣬ�������ﵼ���Ժܲ
(1)CuClΪ__________(�������ۻ��������������ӻ�������)��
(2)��CuCl2��Һ����μ������ KI��Һ���ܷ�����
a.2Cu2++4I-=2CuI��(��ɫ)+I2
b.2Cu2++2Cl-+2I-=2CuCl��(��ɫ)+I2
��a��ӦΪ��Ҫ��Ӧ����Ksp(CuI)________Ksp(CuCl)����������������������=������
(3)ʵ���ҿ����Ȼ�ͭ��Һ��ͭ�ۡ�Ũ���ᷴӦ�Ʊ��Ȼ���ͭ���䷴Ӧԭ��������Ϊ��
CuCl2+Cu+2HCl(Ũ)![]() 2HCuCl2(��ɫ)
2HCuCl2(��ɫ)![]() 2CuCl��(��ɫ)+2HCl
2CuCl��(��ɫ)+2HCl
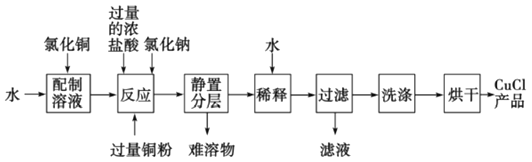
��������Ӧ�����У������Ȼ��Ƶ�Ŀ����________________________��
�ڳ����£�CuOH��KspΪ1.0��10-14����Cu++H2O![]() CuOH+H+��ƽ�ⳣ��Ϊ��________
CuOH+H+��ƽ�ⳣ��Ϊ��________
��Ϊ�õ�������CuCl���壬���ѡ��__________�����ţ��Լ�����ϴ�ӡ�
a������ˮ b��ϡ���� c���Ȼ�ͭ��Һ d���Ҵ�
��CuCl�ڳ�ʪ�Ļ������ױ�����ΪCu2(OH)3Cl����Ӧ�Ļ�ѧ����ʽΪ__________��ʵ��ʱ������2mL0.5mol/L��CuCl2 ��Һ�����տɵõ���Ʒ0.16g����ʵ��IJ���Ϊ__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ũ�Ⱦ�Ϊ0.1 mol/L�������ΪV0��HX��HY��Һ���ֱ��ˮϡ�������V��pH��![]() ���仯��ϵ��ͼ��ʾ������������ȷ����
���仯��ϵ��ͼ��ʾ������������ȷ����

A��HX��HY�������ᣬ��HX�����Ա�HY����
B�������£���ˮ�������c(H+)��c��OH -����a<b
C����ͬ�¶��£����볣��K( HX)��a>b
D��![]() =3����ͬʱ��������Һ��������HX ��HY��H2O�Ļӷ�������
=3����ͬʱ��������Һ��������HX ��HY��H2O�Ļӷ�������![]() ��С
��С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڵ�n���Ӳ��У�������Ϊԭ�ӵ�������Ӳ�ʱ��������ɵĵ�������n-1����ͬ��������Ϊԭ�ӵĴ����ʱ�����������n+1������ܶ�10������˵��Ӳ��ǣ� ��
A.K��B.M��
C.L��D.N��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�������£����淴ӦN2(g)��3H2(g) ![]() 2NH3(g)����H��0���ﵽƽ�⣬�������ı������������й������������
2NH3(g)����H��0���ﵽƽ�⣬�������ı������������й������������
A. �Ӵ���v����v���������仯�����ұ仯�ı������
B. ��ѹv����v����������v������ı�������v������ı���
C. ���£�v����v������С����v����С�ı���С��v����С�ı���
D. ���������v����v����������v������ı�������v������ı���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������(ClNO)���л��ϳ��е���Ҫ�Լ�����ͨ�����·�Ӧ��ã�2NO(g)��Cl2(g) ![]() 2ClNO(g)��
2ClNO(g)��
��1�����������������ڴ����еĺ������������ʱ�������������ȣ��漰���·�Ӧ��
��2NO2(g)��NaCl(s) ![]() NaNO3(s)��ClNO(g)��K1
NaNO3(s)��ClNO(g)��K1
��4NO2(g)��2NaCl(s) ![]() 2NaNO3(s)��2NO(g)��Cl2(g)��K2
2NaNO3(s)��2NO(g)��Cl2(g)��K2
��2NO(g)��Cl2(g) ![]() 2ClNO(g)��K3
2ClNO(g)��K3
��K3��________(��K1��K2��ʾ)��
��2����֪���ֻ�ѧ���ļ����������±�(�������ȵĽṹΪCl��N===O)��
��ѧ�� | N��O | Cl��Cl | Cl��N | N===O |
����/(kJ��mol��1) | 630 | 243 | a | 607 |
��2NO(g)��Cl2(g) ![]() 2ClNO(g)��Ӧ�Ħ�H��a�Ĺ�ϵΪ��H��_______kJ��mol��1��
2ClNO(g)��Ӧ�Ħ�H��a�Ĺ�ϵΪ��H��_______kJ��mol��1��
��3����Ͷ�ϱ�2��1��NO��Cl2���뵽һ��ѹ���ܱ������з�����Ӧ��ƽ��ʱNO��ת�������¶�T��ѹǿp(��ѹ)�Ĺ�ϵ��ͼ(a)��ʾ��
�ٸ÷�Ӧ�Ħ�H________(�>����<������)0��
����pѹǿ�����£�M��ʱ������NO���������Ϊ________��
������Ӧһֱ������pѹǿ�����½��У���M��ķ�ѹƽ�ⳣ��Kp��________(�ú�p�ı���ʽ��ʾ����ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ����ѹ���������)��
 ��
��
��4��һ���������ں��º��ݵ��ܱ������а�һ����������NO(g)��Cl2(g)����n(NO)/n(Cl2)��1.5ʱ�ﵽƽ��״̬��ClNO���������������ͼ(b)��D��E��F�����е�________�㡣
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com