
【题目】(1)浓度为0.1mol/L醋酸钠溶液中质子守恒表达式为__________________;
(2)等浓度的NaHCO3 、Na2CO3混合溶液中的物料守恒表达式为___________________;
(3) 浓度为0.1mol/LNa2CO3溶液电荷守恒表达式为____________________;
(4) Fe2(SO4)3溶液显酸性,用离子方程式表示其原因____________________;
(5) NaHCO3溶液中粒子浓度由大到小的顺序是______________________________。
(6)常温下,NaHSO3溶液中粒子浓度由大到小的顺序是______________________________。
【答案】c(CH3COOH)+c(H+)=c(OH-) 2c(Na+)=3c(H2CO3)+ 3c(CO32-)+3c(HCO3-) c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-) Fe3++3H2O ![]() Fe(OH)3+3H+ c(Na +)>c (HCO3-)> c(OH-) >c (H2CO3)>C(H+)>c(CO32-) c(Na +)>c (HSO3-)>c (H+)>c(SO32-) > c(OH-) >c (H2SO3)
Fe(OH)3+3H+ c(Na +)>c (HCO3-)> c(OH-) >c (H2CO3)>C(H+)>c(CO32-) c(Na +)>c (HSO3-)>c (H+)>c(SO32-) > c(OH-) >c (H2SO3)
【解析】
(1) 质子守恒是指酸失去的质子和碱得到的质子数目相同,浓度为0.1mol/L醋酸钠溶液中质子守恒表达式为c(CH3COOH)+c(H+)=c(OH-);
(2)等浓度的NaHCO3 、Na2CO3混合溶液中Na原子和C原子总数之比为3:2,则物料守恒表达式为2c(Na+)=3c(H2CO3)+ 3c(CO32-)+3c(HCO3-);
(3) 浓度为0.1mol/LNa2CO3溶液电荷守恒表达式为c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-);
(4) Fe2(SO4)3水解生成氢氧化铁和硫酸,溶液显酸性,用离子方程式表示其原因为Fe3++3H2O ![]() Fe(OH)3+3H+;
Fe(OH)3+3H+;
(5) NaHCO3在溶液中存在水解和电离,水解程度大于电离程度,溶液显碱性,c(OH-) > c (H+),钠离子不水解,HCO3-电离和水电离都生成H+,所以离子浓度关系为c(Na +)>c (HCO3-)> c(OH-) >c (H2CO3)>c(H+)>c(CO32-);
(6) 因为NaHSO3完全电离出Na+和HSO3-离子,HSO3-少量电离出H+和SO32- ,HSO3-同时水解生成H2SO3和OH-,因HSO3-电离程度大于水解程度,所以水中各离子浓度大小关系为:c(Na +)>c (HSO3-)>c (H+)>c(SO32-) > c(OH-) >c (H2SO3)。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】在25℃时,用蒸馏水稀释1 mol/L氨水至0.01 mol/L,随溶液的稀释,下列各项中始终保持增大趋势的是( )
A.![]() B.c(H+)·c(OH-)
B.c(H+)·c(OH-)
C.![]() D.c(OH-)
D.c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列电子排布式或轨道表示式正确的是( )
①C原子的轨道表示式:![]()
②Cr原子的电子排布式:1s22s22p63s23p63d44s2
③O原子的轨道表示式:![]()
④Br原子的外层电子排布式:3d104s24p5
⑤B原子的轨道表示式:![]()
A.① ② ③B.② ③ ④C.① ② ④ ⑤D.只有③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组的同学用下图所示装置研究有关电化学的问题。当闭合该装置的电键时,观察到检流计的指针发生了偏转。
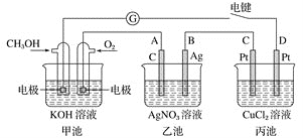
请回答下列问题:
(1)甲池为________(填“原电池”、“电解池”或“电镀池”),通入CH3OH一极的电极反应式为_____________________________________________________________;
(2)乙池中A(石墨)电极的名称为________(填“正极”、“负极”、“阴极”或“阳极”),总反应式为_________________________________________________________;
(3)当乙池中B极质量增加5.40 g时,甲池中理论上消耗O2的体积为________ mL(标准状况),丙池中________极析出________ g铜;
(4)若丙中电极不变,将其溶液换成NaCl溶液,电键闭合一段时间后,甲中溶液的pH将________(填“增大”、“减小”或“不变”);丙中溶液的pH将________(填“增大”、“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】燃料电池具有广阔的发展前途,科学家近年研制出一种微型的燃料电池,采用甲醇取代氢气做燃料可以简化电池设计,该电池有望取代传统电池。某学生在实验室利用碱性甲醇燃料电池电解Na2SO4溶液。

请根据图示回答下列问题:
(1)图中a电极是______(填“正极”、“负极”、“阴极”或“阳极”)。该电极上发生的电极反应式为_________________________________________。
(2)碱性条件下,通入甲醇的一极发生的电极反应式为____________________________。
(3)当消耗3.36 L氧气时(已折合为标准状况),理论上电解Na2SO4溶液生成气体的总物质的量是__。
(4)25℃、101kPa时,燃烧16g甲醇生成CO2和H2O(l),放出的热量为363.26kJ,写出甲醇燃烧的热化学方程式:_________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述正确的是( )
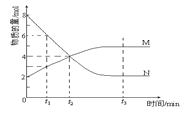
A.反应的化学方程式:2M![]() N
N
B.t2时,正、逆反应速率相等,达到平衡
C.t3时,正反应速率大于逆反应速率
D.t1时N的浓度是M浓度的2倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前工业上有一种方法是用CO2生产燃料甲醇(CH3OH)。在一定条件下发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),图1表示该反应过程中能量(单位为kJ·mol-1)的变化。
CH3OH(g)+H2O(g),图1表示该反应过程中能量(单位为kJ·mol-1)的变化。

(1)该反应为___(填吸热或放热)反应。
(2)在体积固定的密闭容器中,下列能说明该反应已经达到平衡状态的是___(填序号)。
A.v(H2)=3v(CO2)
B.容器内气体压强保持不变
C.v逆(CO2)=v正(CH3OH)
D.容器内气体密度保持不变
E.2molC=O键断裂的同时CH3OH中有1molH—O键形成
F.混合气体的平均摩尔质量不变
(3)在体积为1L的密闭容器中,充入1molCO2和3molH2,测得CO2和CH3OH(g)的浓度随时间变化如图2所示。从反应开始到平衡,用氢气浓度变化表示的平均反应速率v(H2)=___。达平衡时容器内平衡时与起始时的压强比___。
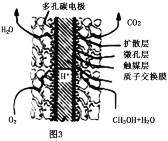
(4)甲醇、氧气在一定条件下可构成如图3所示的燃料电池,其负极的电极反应为___,与铅蓄电池相比,当消耗相同质量的负极物质时,甲醇燃料电池的理论放电量是铅蓄电池的___倍(保留小数点后1位)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】肼![]() 又称联氨,是一种可燃性的液体,可用作火箭燃料。
又称联氨,是一种可燃性的液体,可用作火箭燃料。
![]() 已知在101kPa时,
已知在101kPa时,![]() 时,
时,![]() 在氧气中完全燃烧生成氮气和水,放出624kJ的热量,则
在氧气中完全燃烧生成氮气和水,放出624kJ的热量,则![]() 的燃烧热的热化学方程式是_____________。
的燃烧热的热化学方程式是_____________。
![]() 下图是一个电化学过程示意图。
下图是一个电化学过程示意图。

![]() 图中甲池是_________
图中甲池是_________![]() 填“原电池”或“电解池”
填“原电池”或“电解池”![]() ,其电解质溶液为KOH溶液,则该池电极M的电极反应式是_________________________。
,其电解质溶液为KOH溶液,则该池电极M的电极反应式是_________________________。
![]() 乙池中石墨电极2的电极反应式是_________________________。 当石墨电极2上生成
乙池中石墨电极2的电极反应式是_________________________。 当石墨电极2上生成![]() 气体时
气体时![]() 标准状况下
标准状况下![]() ,转移的电子的数目为_________,则甲池理论上消耗标标准状况下的空气是________
,转移的电子的数目为_________,则甲池理论上消耗标标准状况下的空气是________![]() 假设空气中氧气体积含量为
假设空气中氧气体积含量为![]() 。
。
![]() 传统制备肼的方法,是以NaClO氧化
传统制备肼的方法,是以NaClO氧化![]() ,制得肼的稀溶液。该反应的离子方程式是_________。
,制得肼的稀溶液。该反应的离子方程式是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求完成下列各小题:
Ⅰ.(1)理论上稀的强酸、强碱反应生成1molH2O(l)时放出57.3kJ的热量,写出表示稀硫酸和稀氢氧化钠溶液反应的中和热的热化学方程式__________________________。
(2)已知:乙苯催化脱氢制苯乙烯反应:![]() +H2(g)
+H2(g)
化学键 | C-H | C-C | C=C | H-H |
键能/kJmol-1 | 412 | 348 | 612 | 436 |
计算上述反应的△H=_________kJmol-1。
Ⅱ.25℃时,部分物质的电离平衡常数如表所示,请回答下列问题:
化学式 | CH3COOH | H2CO3 | HClO |
电离平衡常数 | 1.7×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
(1)CH3COOH、H2CO3、HClO的酸性由强到弱的顺序为_____________________________。
(2)将少量CO2气体通入NaClO溶液中,写出反应的离子方程式:____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com