
【题目】某实验小组设计用50mL1.0 mol/L盐酸跟50mL1.1mol/L氢氧化钠溶液在如图装置中进行中和反应。在大烧杯底部垫泡沫塑料(或纸条),使放入的小烧杯杯口与大烧杯杯口相平。然后再在大、小烧杯之间填满碎泡沫塑料(或纸条),大烧杯上用泡沫塑料板(或硬纸板)作盖板,在板中间开两个小孔,正好使温度计和环形玻璃搅拌棒通过。通过测定反应过程中所放出的热量可计算中和热。试回答下列问题:
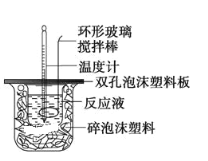
(1)本实验中用稍过量的NaOH的原因教材中说是为保证盐酸完全被中和。试问:盐酸在反应中若因为有放热现象,而造成少量盐酸在反应中挥发,则测得的中和热___(填“偏大”“偏小”或“不变”)。
(2)该实验小组做了三次实验,每次取溶液各50 mL,并记录如下原始数据。
实验序号 | 起始温度t1/℃ | 终止温度t2/℃ | 温差(t2-t1)/℃ | ||
盐酸 | NaOH溶液 | 平均值 | |||
1 | 24.8 | 25.2 | 25.0 | 31.6 | 6.6 |
2 | 25.1 | 25.1 | 25.1 | 31.8 | 6.7 |
3 | 25.2 | 25.0 | 25.1 | 31.9 | 6.8 |
已知盐酸、NaOH溶液密度近似为1.00g/cm3,中和后混合液的比热容c=4.18×10-3 kJ/(g·℃),混合后溶液质量为m,反应放出的热量Q=cm△t,则该反应生成水的物质的量为____,中和热为ΔH=____。
(3)若用等浓度的盐酸与NH3·H2O溶液反应,则测得的中和热会___(填“偏大”“偏小”或“不变”),其原因是____。
(4)在中和热测定实验中存在用水洗涤温度计上的盐酸溶液的步骤,若无此操作步骤,则测得的中和热____(填“偏大”“偏小”或“不变”)。
【答案】偏小 0.05mol -56.01kJ/mol 偏小 NH3·H2O电离吸热 偏小
【解析】
(1)若因为有放热现象导致少量盐酸在反应中挥发,减少了HCl的量,故测得的中和热会偏小;
(2)实验用50mL1.0 mol/L盐酸跟50mL1.1mol/L氢氧化钠溶液反应来测定中和热,氢氧化钠过量,故生成水的物质的量为50mL×10-3mL/L×1.0 mol/L=0.05mol;反应放出的热量Q=cm△t=4.18×10-3 kJ/(g·℃) ×![]() ℃×(50+50)mL×1.00g/cm3=2.8006 kJ;中和热为ΔH=-
℃×(50+50)mL×1.00g/cm3=2.8006 kJ;中和热为ΔH=-![]() =-
=-![]() =-56.01kJ/mol;
=-56.01kJ/mol;
(3)若用等浓度的盐酸与NH3·H2O溶液反应,则测得的中和热会偏小,其原因是NH3·H2O电离吸热,导致所测中和热偏小;
(4)在中和热测定实验中存在用水洗涤温度计上的盐酸溶液的步骤,若无此操作步骤,如果将盐酸洗涤后不保留在原溶液内,势必造成盐酸的物质的量减少,也就造成反应放出的热量减少,最终中和热的数值减小。


 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案科目:高中化学 来源: 题型:
【题目】在一定条件下,密闭容器中进行反应CH4(g) + H2O(g) ![]() CO(g) + 3H2(g),测得CH4的体积百分含量随温度和压强的变化如图所示。下列说法正确的是
CO(g) + 3H2(g),测得CH4的体积百分含量随温度和压强的变化如图所示。下列说法正确的是

A. p1>p2
B. ΔH<0
C. 加入催化剂可以提高甲烷的转化率
D. 恒温下,缩小容器体积,平衡后CH4浓度减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下0.1molL﹣1醋酸溶液的pH=a,下列能使溶液pH=(a+1)的措施是
A. 将溶液稀释到原体积的2倍B. 加入适量的醋酸钠固体
C. 加入等体积0.2 molL﹣1盐酸D. 加少量冰醋酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.H2(g)+I2(g)![]() 2HI(g),平衡后,减压平衡不移动,气体颜色不变
2HI(g),平衡后,减压平衡不移动,气体颜色不变
B.H2(g)+I2(g)![]() 2HI(g),平衡后,加压平衡不移动,气体颜色不变
2HI(g),平衡后,加压平衡不移动,气体颜色不变
C.2NO2(g)![]() N2O4(g),平衡后,加压平衡正向移动,气体颜色变浅
N2O4(g),平衡后,加压平衡正向移动,气体颜色变浅
D.2NO2(g)![]() N2O4(g),平衡后,加压平衡正向移动,气体颜色先变深后变浅
N2O4(g),平衡后,加压平衡正向移动,气体颜色先变深后变浅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①N2(g)+2O2(g)![]() 2NO2(g) △H=+67.7kJ/mol
2NO2(g) △H=+67.7kJ/mol
②2N2H4(g)+2O2(g)![]() 2N2(g)+4H2O(g) △H=-1068kJ/mol
2N2(g)+4H2O(g) △H=-1068kJ/mol
(1)火箭发射时可用肼(N2H4)作燃料,以二氧化氮作氧化剂,它们相互反应生成氮气和水蒸气。根据盖斯定律写出N2H 4和NO2反应的热化学方程式为____;
(2)肼(N2H4)和氧气反应的能量变化如图所示,图中E1表示___,E2表示____,△H=-534kJ/mol表示_____。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在给定条件下,下列选项所示的物质间转化均能实现的是( )
A.Ca(OH)2![]() Ca(ClO)2(aq)
Ca(ClO)2(aq)![]() HClO(aq)
HClO(aq)
B.Fe(s)![]() Fe2O3(s)
Fe2O3(s)![]() FeCl3(aq)
FeCl3(aq)
C.S(s)![]() SO2(g)
SO2(g)![]() BaSO3(s)
BaSO3(s)
D.NH3(g)![]() NO(g)
NO(g)![]() HNO3(aq)
HNO3(aq)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示___________,K值大小与温度的关系是:温度升高,K值_________(填一定增大、一定减小、或可能增大也可能减小)。
(2)对于可逆反应CO(g) +H2O(g) ![]() CO2(g)+H2(g) △H<0在850℃时,KC=1 该反应的平衡常数K的表达式为K=______;若温度为900℃,达到平衡后KC_____1 (填“>“<”=)
CO2(g)+H2(g) △H<0在850℃时,KC=1 该反应的平衡常数K的表达式为K=______;若温度为900℃,达到平衡后KC_____1 (填“>“<”=)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示三套实验装置,分别回答下列问题。
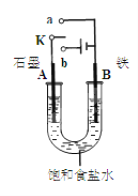
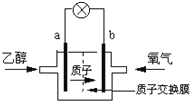
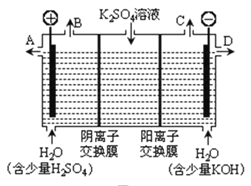
图1图2图3
(1)图1中,① 若开始时开关K与a连接,则该装置为_____(填装置名称),电极A的电极反应式为________________________
②若开始时开关K与b连接,则总反应的离子方程式为 ___________________________
(2)2004年美国圣路易斯大学研制了一种新型的乙醇电池,它用磺酸类质子溶剂,在200°C左右时供电,电池示意如图2所示:
①______极(填a或b)为电池的正极,电池工作时电流方向为_________(填a→b或b→a)
②写出该电池负极的电极反应式________________________________________
(3)用图3装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾(电解槽内的阳离子交换膜只允许阳离子通过,阴离子交换膜只允许阴离子通过)。
①该电解槽的阴极反应式为_____________________。
②制得的硫酸溶液从出口____(填“A”、“D”)导出,并简述原因__________________________(请用化学用语和文字解释)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙烯酰胺是一种重要的有机合成的中间体。它的球棍模型如图所示:(图中“棍”代表单键或双键或三键,不同颜色球表示不同原子:C、H、O、N)

(1)丙烯酰胺的分子式为___,结构简式为___。
(2)有关丙烯酰胺的说法正确的是___。
A.丙烯酰胺分子内所有原子不可能在同一平面内
B.丙烯酰胺属于烃的含氧衍生物
C.丙烯酰胺能够使酸性高锰酸钾溶液褪色
D.丙烯酰胺能够使溴的四氯化碳溶液褪色
(3)工业上生产丙烯酰胺可以用下面的反应(反应均在一定条件下进行):
CH![]() CH
CH![]() CH2=CHCN
CH2=CHCN![]() 丙烯酰胺
丙烯酰胺
假设反应Ⅰ和反应Ⅱ都是原子利用率100%的反应,反应Ⅰ所需另一反应物的分子式为___,反应Ⅱ的方程式为___。
(4)聚丙烯酰胺(PAM)是一种合成有机高分子絮凝剂,写出由丙烯酰胺合成聚丙烯酰胺的化学方程式___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com