
【题目】根据题意完成下列填空。
(1)a.金刚石和石墨 b.12C和13C c.CH4和C2H6 d.乙醇与二甲醚(填字母)
①互为同位素的是___;
②互为同素异形体的是___;
③互为同系物的是___;
④互为同分异构体的是___。
(2)请补充完下列方程式:
①CH4+Cl2![]() ___+HCl
___+HCl
②CH2=CH2+Br2→___
【答案】b a c d CH3Cl CH2BrCH2Br
【解析】
同位素是同种元素的不同原子的互称;同素异形体是同种元素组成的不同单质的互称;同系物是性质相同、结构相似、组成上相差1个或若干个“CH2”原子团的有机物的互称;同分异构体是分子式相同、结构不同的两种化合物的互称。书写化学方程式时,需分析有机物的类别,依据同类物质的性质,确定发生反应的类型,从而确定产物。
(1)①12C和13C都是碳元素的两种核素,二者互为同位素,故选b;
②金刚石和石墨都是碳元素组成的两种不同单质,二者的性质不同,互为同素异形体,故选a;
③CH4和C2H6都属于烷烃,分子组成上后者比前者多1个“CH2”,所以二者互为同系物,故选c;
④乙醇与二甲醚的分子式都为C2H6O、前者为醇,后者为醚,二者结构不同,互为同分异构体,故选d。
答案为:b;a;c;d;
(2)①CH4与Cl2在光照条件下发生取代反应,生成CH3Cl 和HCl,反应的化学方程式为CH4+Cl2![]() CH3Cl +HCl
CH3Cl +HCl
②CH2=CH2与Br2发生加成反应,生成CH2BrCH2Br,反应的化学方程式为CH2=CH2+Br2→CH2BrCH2Br。
答案为:CH3Cl;CH2BrCH2Br。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】常温下,用0.1mol/LNaOH溶液分别滴定体积均为20.00mL、浓度均为0.1mol/L的HX、HY溶液,pH随NaOH溶液体积变化如图。下列结论正确的是( )
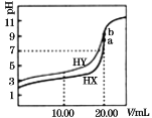
A.已知室温下某碱AOH的Kb=1×10-9,则AY的水溶液呈碱性
B.当加入10.00mL NaOH溶液时,有c(Na+)>c(HX)> c(X-)> c(H+)
C.pH=7时,c(Y-)=c(X-)
D.a、b两点溶液混合后,c(HX)+c(HY)+c(H+)=c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.阅读下列材料后,回答相应问题:一个体重50kg的健康人的体内含铁2g。这2g铁在人体内不是以单质的形式存在的,而是以Fe2+和Fe3+的形式存在。Fe2+易被吸收,给贫血者补充铁时,应给予含Fe2+的亚铁盐,如硫酸亚铁(FeSO4)。服用维生素C,可使食物中的Fe3+转化为Fe2+,有利于铁的吸收。
⑴人体中经常进行![]() 的转化,A转化中Fe2+发生________(填“氧化”或“还原”,下同)反应,B转化中Fe3+做________剂。
的转化,A转化中Fe2+发生________(填“氧化”或“还原”,下同)反应,B转化中Fe3+做________剂。
⑵“服用维生素C,可使食物中的Fe3+转化为Fe2+”,这句话指出维生素C在这一反应中做________剂,具有________性。
Ⅱ.某化工厂排出的废液中含有Ag+、Ba2+、Cu2+三种金属阳离子,现欲用CO32-、OH-、Cl-三种不同的阴离子分别将上述金属阳离子逐一形成沉淀除去。加入阴离子的正确顺序是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请阅读下列材料,完成下面小题。
联合国将2019年定为“国际化学元素周期表年”以纪念门捷列夫发现元素周期律150周年。元素周期律把元素及其化合物纳入一个统一的理论体系,为系统研究元素及其化合物提供了科学方法,为发现和探索新元素、新物质提供了有效思路。
1. 为纪念门捷列夫,科学家将1955年人工合成的一种新元素用符号“Md”表示,中文命名为“钔”。核素![]() Md的中子数为(______)
Md的中子数为(______)
A. 101 B. 359 C. 258 D. 157
2. O和S都属于元素周期表ⅥA元素,它们原子结构中相同的是(______)
A. 质子数 B. 电子层数 C. 电子数 D. 最外层电子数
3. 锂是第2周期ⅠA族元素,下列有关锂元素性质推测正确的是(______)
A. 金属性比钠弱
B. 最高化合价为+2
C. 单质与水的反应比钠更剧烈
D. 原子半径比钠的大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知 4NH3+5O2 = 4NO+6H2O(g),若反应速率分别用 v(NH3)、v(O2)、v(NO)、v(H2O)表示,则正确的关系是( )
A.v(O2)=![]() v(NH3)B.v(H2O)=
v(NH3)B.v(H2O)= ![]() v(O2)C.v(H2O)=
v(O2)C.v(H2O)=![]() v(NH3)D.v(NO)=
v(NH3)D.v(NO)= ![]() v(O2)
v(O2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】大气中CO2含量的增多除了导致地球表面温度升高外,还会影响海洋生态环境。某研究小组在实验室测得不同温度下(T1,T2)海水中CO32-浓度与模拟空气中CO2浓度的关系曲线。已知:海水中存在以下平衡:CO2(aq)+CO32-(aq)+H2O(aq)![]() 2HCO3-(aq),下列说法不正确的是
2HCO3-(aq),下列说法不正确的是
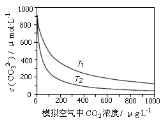
A.T1>T2
B.海水温度一定时,大气中CO2浓度增加,海水中溶解的CO2随之增大,CO32-浓度降低
C.当大气中CO2浓度确定时,海水温度越高,CO32- 浓度越低
D.大气中CO2含量增加时,海水中的珊瑚礁将逐渐溶解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定质量Fe、Fe2O3和CuO的混合粉末投入到100 mL 1.80 molL-1的硫酸中,充分反应后收集到标准状况下0.896 L H2,又测得反应后的混合体系中只有FeSO4溶液和1.28 g固体Cu。请你确定原混合粉末中Fe的质量_____________。(要求写出简要推理过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将25℃时浓度均为0.1mol/L的HA溶液和BOH溶液按体积分别为Va和Vb混合,保持Va+Vb=100mL,且生成的BA可溶于水。已知Va、Vb与混合液pH关系如图所示。下列说法错误的是( )
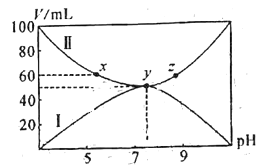
A.曲线II表示HA溶液的体积
B.x点存在c(A-)+c(OH-)=c(B+)+c(H+)
C.电离平衡常数:K(HA)>K(BOH)
D.x、y、z三点对应的溶液中,y点溶液中水的电离程度最大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com