
����Ŀ����ijұ�����ŷŵķ���(��Ҫ�ɷ�Ϊ����,��Fe2+. Pb2+. Cu2+. H3AsO3������)��п��(��ZnO��Zn�����������)Ϊԭ���Ʊ���ؼ�ZnCl2��Һ�Ĺ�����������:
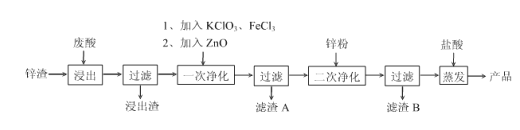
��֪��Fe3+��ʼ����ʱpHΪ2.7��FeAsO4������ˮ��
�ش���������
��1��H3AsO3(������)��AsԪ�صĻ��ϼ���________��
��2����������ʱ��Ӧ��ӦԶ���Դ��ԭ����________��
��3����һ�ξ��������Գ�ȥFe��AsԪ��,����KClO3��FeCl3��ȥ��ʱ������Ӧ�����ӷ���ʽΪ________________________������ZnO��Ŀ����________________________�����෴ӦΪKClO3+3H3AsO3 ![]() KCl+3H3AsO4 ��FeCl3+H3AsO4
KCl+3H3AsO4 ��FeCl3+H3AsO4![]() FeAs04+3HCl,������A�ijɷ���________��________��
FeAs04+3HCl,������A�ijɷ���________��________��
��4������Ʒ���е���Ҫ������________,������������ʵĸĽ�������_______________________��
��5��п�۱�����ؾ��м۸���ˡ���������ŵ�,�ڵ綯������ҵӦ��ǰ������������ʹ�õ��Ǹߴ���пƬ,��ZnCl2��NH4ClΪ��Ҫ����ʡ�п�۱�����طŵ�ʱ,���������ϵĵ缫��ӦʽΪ________________________��
���𰸡� +3 ��Ӧ����п�����ᷴӦ��H2���� KClO3+6FeCl2+6HCl ![]() 6FeCl3+KCl+3H2O ������Һ��pH�Դٽ�Fe3+����ˮ������������������ FeAsO4 Fe(OH)3 KCl ��H2O2(��Cl2)����KClO3 Zn-2e-
6FeCl3+KCl+3H2O ������Һ��pH�Դٽ�Fe3+����ˮ������������������ FeAsO4 Fe(OH)3 KCl ��H2O2(��Cl2)����KClO3 Zn-2e-![]() Zn2+
Zn2+
�������������������������Ϣ��֪��п����������������е�п������п���������У� Cu2+��п��ԭΪ���ʣ�ͭ�������������γ����������ˣ�Ȼ������Һ�м�������غ��Ȼ�����ȥ��Һ�е������飬����ذѷ�������Fe2+��H3AsO3�ֱ�����ΪFe3+��H3AsO4���Ȼ�����H3AsO4��Ӧ����������ˮ��FeAsO4����������п��Ϊ�˵�����Һ��pH�Դٽ�������ˮ�����������������������ξ�����Ŀ����Ϊ�˳�ȥPb2+�����ʡ�
��1��H3AsO3(������)��AsԪ�صĻ��ϼ���+3��
��2����������ʱ��Ӧ��ӦԶ���Դ��ԭ���Ƿ�Ӧ����п�����ᷴӦ������ȼ�ױ���H2���ɡ�
��3����һ�ξ��������Գ�ȥFe��AsԪ��������KClO3��FeCl3��ȥ��ʱ������Ӧ�����ӷ���ʽΪKClO3+6FeCl2+6HCl ![]() 6FeCl3+KCl+3H2O������ZnO��Ŀ���ǵ�����Һ��pH���ٽ�Fe3+����ˮ�����������������������෴ӦΪKClO3+3H3AsO3
6FeCl3+KCl+3H2O������ZnO��Ŀ���ǵ�����Һ��pH���ٽ�Fe3+����ˮ�����������������������෴ӦΪKClO3+3H3AsO3 ![]() KCl+3H3AsO4 ��FeCl3+H3AsO4
KCl+3H3AsO4 ��FeCl3+H3AsO4![]() FeAsO4+3HCl����ˣ�����A�ijɷ���FeAsO4��Fe(OH)3��
FeAsO4+3HCl����ˣ�����A�ijɷ���FeAsO4��Fe(OH)3��
��4������Ʒ���е���Ҫ����������صĻ�ԭ����KCl��Ϊ�˱�������Ȼ����������ʣ�������H2O2(��Cl2) ����KClO3��
��5��п�۱�����ظ���ʹ�õ��Ǹߴ���пƬ����ZnCl2��NH4ClΪ��Ҫ����ʡ�п�۱�����طŵ�ʱ�����������ϵĵ缫��ӦʽΪZn-2e-![]() Zn2+��
Zn2+��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����ʵ��С����Ƶ�����ʵ������������ ��������
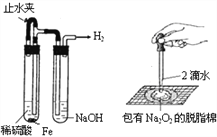
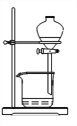
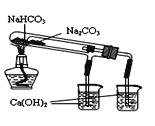
A. ͼ1���Ʊ����۲����������� B. ͼ2��֤������������ˮ��Ӧ����
C. ͼ3����ȡ��Һʱ�ų���ı���Һ D. ͼ4���Ƚ�NaHCO3��Na2CO3���ȶ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧƽ����Ҫ�о�������һ�෴Ӧ�Ĺ��ɣ�������
A.���ַ�Ӧ
B.�κη�Ӧ
C.���淴Ӧ
D.���巴Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʽΪC9H12���л����֪�����ϵ�һ�ȴ���ֻ�����֣�����˵������ȷ���ǣ� ��
A.���л��ﲻ�ܷ���ȡ����Ӧ�����ܷ����ӳɷ�Ӧ
B.���л��ﲻ��ʹ���Եĸ��������Һ��ɫ������ʹ��ˮ��ɫ
C.���л�������е�����ԭ�ӿ�����ͬһƽ����
D.���л����һ�ȴ��������5��ͬ���칹��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪���ס��ҡ���Ϊ�������ʣ��׳�����Ϊ���壬��Ϊһ����ɫ���壬��Ϊ��ɫ���塣A��B��C��D��Ϊ�����DΪһ���ɫ����������֮������ͼת����ϵ��
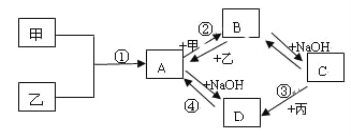
��ش��������⡣
��1��д���������ʵ����ƣ���____________��B______________��
��2��д���۷�Ӧ�Ļ�ѧ����ʽ��_____________________________��
��3��д���ڷ�Ӧ�����ӷ���ʽ��____________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���������İ�������粒��������ܱ������У�������Ӧ��NH2COONH4��s��![]() 2NH3��g��+CO2��g�����÷�Ӧ��ƽ�ⳣ���ĸ���������lgK��ֵ���¶ȣ�T���ı仯������ͼ��ʾ������˵������ȷ����
2NH3��g��+CO2��g�����÷�Ӧ��ƽ�ⳣ���ĸ���������lgK��ֵ���¶ȣ�T���ı仯������ͼ��ʾ������˵������ȷ����

A. �÷�Ӧ�ġ�H��0
B. A���Ӧ״̬��ƽ�ⳣ��K��A��=10��2.294
C. NH3�������������ʱ���÷�Ӧһ���ﵽƽ��״̬
D. 30��ʱ��B���Ӧ״̬����������< �����棩
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʱ���������Լ���������ˮ��0.01mol/L�������pH=12�İ�ˮ��pH=11��̼������Һ��������Һ����ˮ�����c��H+����ϵ��ȷ���ǣ� ��
A.�ڣ���
B.�ۣ���
C.�٣���
D.��=��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ� ��
A.�е������ɵĻ�ѧ��Ӧ����������ԭ��Ӧ
B.���������ﲻһ���Ƿǽ���������
C.Na2O2����ˮ��Ӧ������Na2O2����������ĸ����
D.Ư�����ڴ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������M�м��ۻ������أ������㶹������Ȼ�������M����������������ǣ� �� 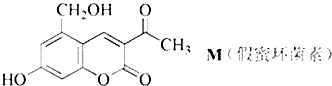
A.���������������ȵ������£�1molM������6molH2�����ӳɷ�Ӧ
B.M������ʹ����KMnO4��Һ��ɫ
C.M�����ȵ�NaOH��Һ�з�����Ӧ����������3molNaOH
D.1molM������2molBr2������Ӧ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com