
【题目】Li4Ti5O12和LiFePO4都是锂离子电池的电极材料,可利用钛铁矿(主要成分为FeTiO3,还含有少量MgO、SiO2等杂质)来制备,工艺流程如下:
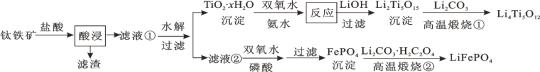
下列说法不正确的是
A.“酸浸”后,若钛主要以TiOCl42-形式存在,则相应反应的离子方程式可表示为:FeTiO3+4H++4Cl-=Fe2++TiOCl42-+2H2O
B.若Li2Ti5O15中Ti的化合价为+4,则其中过氧键的数目为3个
C.“高温煅烧②”中由FePO4制备LiFePO4的化学方程式可表示为:2FePO4+Li2CO3+H2C2O4![]() 2LiFeO4+H2O↑+3CO2↑
2LiFeO4+H2O↑+3CO2↑
D.TiO2·xH2O沉淀与双氧水、氨水反应40min所得实验结果如表所示:
温度/℃ | 30 | 35 | 40 | 45 | 50 |
TiO2·xH2O转化率/% | 92 | 95 | 97 | 93 | 88 |
可知,40℃前,未达到平衡状态,随着温度升高,转化率变大
【答案】B
【解析】
利用钛铁矿(主要成分为FeTiO3,还含有少量MgO、SiO2等杂质)来制备Li4Ti5O12和LiFePO4,根据制备流程可知,加入盐酸过滤后滤渣为SiO2,滤液①中含有Mg2+、Fe2+、TiOCl42-,水解后过滤,沉淀为TiO2xH2O,经过一系列转化为最终转化为Li4Ti5O12.滤液②中加入双氧水,将亚铁离子被氧化,在磷酸的作用下转化为磷酸铁,通过高温煅烧最终转化为LiFePO4,据此分析解答。
A.“酸浸”后,若钛主要以TiOCl42-形式存在,Ti的化合价为+4价,反应前后没有化合价的变化,是非氧化还原反应,因此相应反应的离子方程式可表示为:FeTiO3+4H++4Cl-=Fe2++TiOCl42-+2H2O,故A正确;
B.Li2Ti5O15中Ti的化合价为+4,Li的化合价是+1价,由化合价代数和为0可知,氧元素的负价代数和为22,设其中过氧键的数目为x个,则2x+(15-2x)×2=22,解得x=4,故B错误;
C.根据以上分析可知“高温煅烧②”中由FePO4制备LiFePO4,反应中铁的化合价由+3价降低到+2价,H2C2O4有还原性,其中碳的化合价应由+3价升高到+4价,故化学方程式可表示为:2FePO4+Li2CO3+H2C2O4 ![]() 2LiFePO4+H2O+3CO2↑,故C正确;
2LiFePO4+H2O+3CO2↑,故C正确;
D.根据表中数据可知,40oC时,TiO2·xH2O转化率最高,因低于40oC时,反应未达到平衡状态,TiO2xH2O转化率随温度升高而增加,超过40oC时,双氧水分解和氨气的逸出速率加快,导致TiO2xH2O转化率下降,故D正确;
故选B。


科目:高中化学 来源: 题型:
【题目】现有AlCl3和MgSO4混合溶液,向其中不断加入NaOH溶液,得到沉淀的量与加入NaOH溶液的体积如图所示。原溶液中Cl-与SO42-的物质的量之比为( )
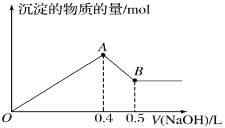
A.3∶1B.4∶1C.5∶1D.6∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿伏加德罗常数的近似值为6.02×1023。按要求完成下列填空:
(1)1molCl2中约含有___个氯气分子,约含有__个氯原子。含有6.02×1023个氢原子的H2SO4的物质的量是___;
(2)某硫酸钠溶液中含有3.01×1023个Na+,则该溶液中SO42-的物质的量是___。
(3)2L1mol/LMgCl2中镁离子的物质的量为___,Cl-的物质的量浓度为___。
(4)三种盐的混合溶液中含有0.2molNa+、0.25molMg2+、0.4molCl-、SO42-,则SO42-的微粒个数约为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是NO2和O2形成的原电池装置。下列说法不正确的是
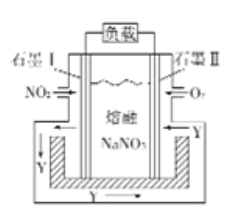
A. 石墨Ⅱ做正极,O2发生还原反应
B. 该电池放电时NO3-从右侧向左侧迁移
C. 当消耗1mol NO2时,电解质中转移1mol e
D. 石墨Ⅰ附近发生的反应为NO2+NO3--e-=N2O5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,在某密闭容器内某一反应中M、N的物质的量随反应时间变化的曲线如图所示.下列叙述中,正确的是( )

A.该反应的化学方程式为M═2N
B.若t1=1,则反应开始至t1时间段M 的反应速率为1mol﹒L-1﹒min-1
C.t3时正反应速率等于逆反应速率
D.t2时正逆反应速率相等,反应达到平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨时,在某个密闭容器中发生反应:3H2(g)+N2(g)![]() 2NH3(g)
2NH3(g)
(1)下列能使反应速率加快的是_____________________
①升高温度 ②减小容器体积 ③通入N2 ④通入Ar使压强增大 ⑤通入HCl气体 ⑥加入合适的催化剂
A.①③④⑤ B.①②③⑥ C.①②③④ D.②④⑤⑥
(2)在恒温、恒容的条件下,下列说法能表示反应达到化学平衡状态的是__________
①当有1molN2被消耗,就有2molNH3生成
②当有6molH—H键形成时,就有12molN—H键形成
③2![]() 正(N2)=
正(N2)=![]() 逆(NH3)
逆(NH3)
④N2的物质的量不再变化
⑤H2、N2、NH3的浓度之比等于3:1:2
⑥混合气体的密度不变
⑦混合气体的压强不变
⑧混合气体的平均相对分子质量不变
A.①③④⑤⑦ B.①②③④⑧ C.②③④⑦⑧ D.②④⑤⑥
(3)在2 L定容密闭容器中通入1 mol N2(g)和3 mol H2(g),发生反应:3H2(g)+N2(g)![]() 2NH3(g)(放热反应)。测得压强-时间图像如图甲,测得p2=0.8p1,此时温度与起始温度相同,在达到平衡前某一时刻(t1)若仅改变一种条件,得到如图乙图像。
2NH3(g)(放热反应)。测得压强-时间图像如图甲,测得p2=0.8p1,此时温度与起始温度相同,在达到平衡前某一时刻(t1)若仅改变一种条件,得到如图乙图像。
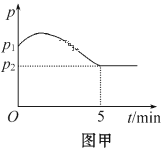
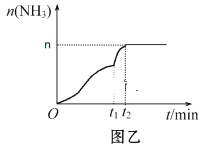
①如图甲,反应开始至平衡时NH3的平均反应速率为_____________________,平衡时氢气的转化率为_________。
②如图乙,下列说法正确的是_________
A.t1时刻可能是加入了催化剂
B.改变条件可以使H2 100℅转化为NH3
C.增大N2的浓度,可以提高H2的转化率
D.t2时刻,N2的浓度与NH3的浓度之比为1:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①Fe+H2SO4(稀)=FeSO4+H2↑
②Cu+2H2SO4(浓)![]() CuSO4+2H2O+SO2↑
CuSO4+2H2O+SO2↑
③KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O。
试回答下列问题:
(1)当反应①转移3 mol电子时,消耗H2SO4的质量是______g,产生氢气的体积(标准状况)________L。
(2)反应②中________作氧化剂,________是氧化产物。
(3)当反应②中生成11.2 L SO2气体(标准状况下)时,被还原的H2SO4的物质的量是________。
(4)用单线桥法表示反应②电子转移的方向和数目(在化学方程式上标出)__________。
(5)反应③中氧化产物与还原产物的物质的量之比为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应属于氧化还原反应的是
A. CaCO3+2HCl=CaCl2+CO2↑+ H2O
B. CaO+H2O=Ca(OH)2
C. 2H2O2![]() 2H2O+O2↑
2H2O+O2↑
D. CaCO3![]() CaO+CO2↑
CaO+CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完成下列实验所选择的装置或仪器(夹持装置已略去)正确的是( )
选项 | A | B | C | D |
实验 | 用CCl4提取溴水中的Br2 | 从食盐水中提取NaCl固体 | 从KI和I2的固体混合物中回收I2 | 配制100 mL0.1000 mol·L-1Na2CO3溶液 |
装置或仪器 |
|
|
|
|
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com