
【题目】合成氨时,在某个密闭容器中发生反应:3H2(g)+N2(g)![]() 2NH3(g)
2NH3(g)
(1)下列能使反应速率加快的是_____________________
①升高温度 ②减小容器体积 ③通入N2 ④通入Ar使压强增大 ⑤通入HCl气体 ⑥加入合适的催化剂
A.①③④⑤ B.①②③⑥ C.①②③④ D.②④⑤⑥
(2)在恒温、恒容的条件下,下列说法能表示反应达到化学平衡状态的是__________
①当有1molN2被消耗,就有2molNH3生成
②当有6molH—H键形成时,就有12molN—H键形成
③2![]() 正(N2)=
正(N2)=![]() 逆(NH3)
逆(NH3)
④N2的物质的量不再变化
⑤H2、N2、NH3的浓度之比等于3:1:2
⑥混合气体的密度不变
⑦混合气体的压强不变
⑧混合气体的平均相对分子质量不变
A.①③④⑤⑦ B.①②③④⑧ C.②③④⑦⑧ D.②④⑤⑥
(3)在2 L定容密闭容器中通入1 mol N2(g)和3 mol H2(g),发生反应:3H2(g)+N2(g)![]() 2NH3(g)(放热反应)。测得压强-时间图像如图甲,测得p2=0.8p1,此时温度与起始温度相同,在达到平衡前某一时刻(t1)若仅改变一种条件,得到如图乙图像。
2NH3(g)(放热反应)。测得压强-时间图像如图甲,测得p2=0.8p1,此时温度与起始温度相同,在达到平衡前某一时刻(t1)若仅改变一种条件,得到如图乙图像。
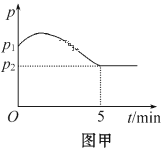
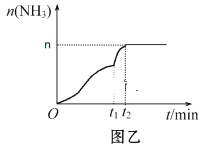
①如图甲,反应开始至平衡时NH3的平均反应速率为_____________________,平衡时氢气的转化率为_________。
②如图乙,下列说法正确的是_________
A.t1时刻可能是加入了催化剂
B.改变条件可以使H2 100℅转化为NH3
C.增大N2的浓度,可以提高H2的转化率
D.t2时刻,N2的浓度与NH3的浓度之比为1:2
【答案】B C 0.08mol/(L·min) 40% AC
【解析】
根据题意,本题考查化学反应速率、化学平衡的判断、化学平衡移动、图像的分析,运用![]() 、勒夏特里原理分析。
、勒夏特里原理分析。
(1)①升高温度,可以加快反应速率,①正确;
②减小容器体积,相当增大压强,反应物和生成物浓度增大,反应速率加快,②正确;
③通入N2 ,增大反应物浓度,反应速率加快,③正确;
④通入Ar使压强增大 ,反应物和生成物浓度不变,反应速率不变,④错误;
⑤通入HCl气体,会与NH3生成NH4Cl,使生成物浓度降低,反应速率减慢,⑤错误;
⑥加入合适的催化剂可以加快反应速率,⑥正确;
故答案:B;
(2)①1molN2被消耗和2molNH3生成 均指正反应速率,不能判断是否达到平衡,①错误;
②当有6molH—H键形成时,就有12molN—H键形成 ,此时![]() 正=
正=![]() 逆,反应达到平衡状态,②正确;
逆,反应达到平衡状态,②正确;
③2![]() 正(N2)=
正(N2)=![]() 逆(NH3),此时
逆(NH3),此时![]() 正=
正=![]() 逆,反应达到平衡状态,③正确;
逆,反应达到平衡状态,③正确;
④反应过程中N2的物质的量会发生变化,当N2的物质的量不再变化时,![]() 正=
正=![]() 逆,反应达到平衡状态,④正确;
逆,反应达到平衡状态,④正确;
⑤非平衡时候H2、N2、NH3的浓度之比也可以等于3:1:2,因此H2、N2、NH3的浓度之比等于3:1:2时不能判断是否达到平衡,⑤错误;
⑥在恒温、恒容的条件下,混合气体的密度始终保持不变,因此混合气体的密度不变时不能判断是否达到平衡,⑥错误;
⑦反应3H2(g)+N2(g)![]() 2NH3(g)前后气体分子数不相同,在恒温、恒容的条件下,混合气体的压强会发生变化,因此混合气体的压强不变时,反应达到平衡,⑦正确;
2NH3(g)前后气体分子数不相同,在恒温、恒容的条件下,混合气体的压强会发生变化,因此混合气体的压强不变时,反应达到平衡,⑦正确;
⑧反应3H2(g)+N2(g)![]() 2NH3(g)前后气体分子数不相同,在恒温、恒容的条件下,混合气体的平均相对分子质量会发生变化,当混合气体的平均相对分子质量不变时,反应达到平衡,⑧正确;
2NH3(g)前后气体分子数不相同,在恒温、恒容的条件下,混合气体的平均相对分子质量会发生变化,当混合气体的平均相对分子质量不变时,反应达到平衡,⑧正确;
故答案为:C;
(3)①假设反应过程中NH3变化的物质的量为2x,则
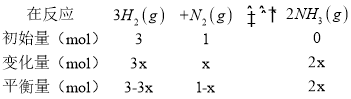
由p2=0.8p1和反应前后压强比等于气体物质的量之比可知,![]() ,解得x=0.4mol,反应开始至平衡时NH3的平均反应速率为
,解得x=0.4mol,反应开始至平衡时NH3的平均反应速率为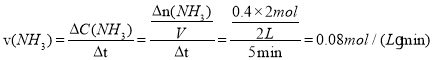 ,平衡时氢气的转化率
,平衡时氢气的转化率![]() ;
;
故答案为:0.08mol/(L·min);40%;
②A.t1时刻改变条件后生成NH3反应速率加快,可能是加入了催化剂,A项正确;
B.可逆反应不能达到 100℅转化,B项错误;
C.增大N2的浓度,平衡向正方向移动,可以提高H2的转化率,C项正确;
D.t2时刻,反应达到平衡状态,此时N2的浓度与NH3的浓度之比不一定为1:2,D项错误;
故答案为:AC。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列图示中,A为一种常见的单质,B、C、D、E是含A元素的常见化合物,它们的焰色反应均为黄色。
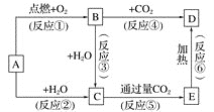
请填写下列空白:
(1)写出化学式:A____,B____,C_____,D____,E____。
(2)以上反应中,属于氧化还原反应的有____________(填写编号)。
(3)A→C反应的离子方程式是________。
(4) B→C反应的化学方程式是____________。
(5)E→D反应的化学方程式是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,生成物所贮的化学能比反应物所贮化学能要多的是( )
A.CaO+H2O=Ca(OH)2
B.NaOH+HCl=NaCl+H2O
C.CH4+2O2 ![]() CO2+2H2O
CO2+2H2O
D.CO2+C ![]() 2CO
2CO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究氮氧化物反应机理,对于控制汽车尾气、保护环境有重要意义。
(1)NO在空气中存在如下反应:2NO(g) + O2(g) ![]() 2NO2(g) ΔH,上述反应分两步完成,其中第一步反应①如下,写出第二步反应②的热化学方程式(其反应的焓变ΔH2用含ΔH、ΔH1的式子来表示): ① 2NO(g)
2NO2(g) ΔH,上述反应分两步完成,其中第一步反应①如下,写出第二步反应②的热化学方程式(其反应的焓变ΔH2用含ΔH、ΔH1的式子来表示): ① 2NO(g) ![]() N2O2(g)ΔH1<0,② ___________;
N2O2(g)ΔH1<0,② ___________;
(2)NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应的热化学方程式为: 4NH3(g)+6NO(g)![]() 5N2(g)+6H2O(g)△H=-1811.63KJ/mol;反应在恒容密闭容器中进行,在其它相条件同时,选用不同的催化剂,反应产生N2的物质的量随时间变化如图所示。
5N2(g)+6H2O(g)△H=-1811.63KJ/mol;反应在恒容密闭容器中进行,在其它相条件同时,选用不同的催化剂,反应产生N2的物质的量随时间变化如图所示。

①在催化剂A的作用下,经过相同时间,测得脱氮率随反应温度的变化情况如图2所示,据图可知,在相同的时间内,300℃之前,温度升高脱氮率逐渐增大,300℃之后温度升高脱氮率逐渐减小(催化剂均末失效),写出300℃之后脱氮率减小的原因是_________。
②其他条件相同时,请在图中补充在催化剂B作用下脱氮率随温度变化的曲线________。

(3)工业制HNO3的尾气中含有的NO2和NO常用NaOH溶液吸收,反应的化学方程式为:NO+NO2+2NaOH=2NaNO2+H2O,2NO2+2NaOH=NaNO2+NaNO3+H2O,现有平均组成为NOx的NO、NO2混合气体,通入足量的NaOH溶液中,充分反应后没有气体剩余,则:
①x的取值范围为_________________。
②反应后溶液中n(NO2-)︰n(NO3-)=____________________。(用含x的代数式表示)
(4)电解法处理氮氧化合物是目前大气污染治理的一个新思路,原理是将NOx在电解池中分解成无污染的N2和O2除去,如图示,两电极间是新型固体氧化物陶瓷,在一定条件下可自由传导O2-,电解池阴极反应为___。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Li4Ti5O12和LiFePO4都是锂离子电池的电极材料,可利用钛铁矿(主要成分为FeTiO3,还含有少量MgO、SiO2等杂质)来制备,工艺流程如下:
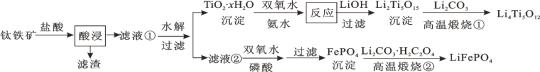
下列说法不正确的是
A.“酸浸”后,若钛主要以TiOCl42-形式存在,则相应反应的离子方程式可表示为:FeTiO3+4H++4Cl-=Fe2++TiOCl42-+2H2O
B.若Li2Ti5O15中Ti的化合价为+4,则其中过氧键的数目为3个
C.“高温煅烧②”中由FePO4制备LiFePO4的化学方程式可表示为:2FePO4+Li2CO3+H2C2O4![]() 2LiFeO4+H2O↑+3CO2↑
2LiFeO4+H2O↑+3CO2↑
D.TiO2·xH2O沉淀与双氧水、氨水反应40min所得实验结果如表所示:
温度/℃ | 30 | 35 | 40 | 45 | 50 |
TiO2·xH2O转化率/% | 92 | 95 | 97 | 93 | 88 |
可知,40℃前,未达到平衡状态,随着温度升高,转化率变大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下:①6.72 LCH4;②3.01×1023个HCl分子;③13.6 gH2S;④0.2 molNH3,下列对这四种气体中含有氢原子数目从大到小表达正确的是( )
A.①③②④B.①③④②C.②③①④D.②④③①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ某无土栽培用的营养液,营养液要求KCl、K2SO4和NH4Cl 3种固体原料的物质的量之比为1:4:8。
(1) 配制该营养液后c(NH4+)=0.016 mol﹒L-1,溶液c(K+)=_______________。
(2) 若采用(NH4)2SO4和KCl来配制该营养液,则(NH4)2SO4和KCl物质的量之比为________
Ⅱ从1L 1 mol﹒L-1氢氧化钠溶液中取出100 mL:
(1)取出的这100 mL氢氧化钠溶液的物质的量浓度是______。若将取出的这100 mL氢氧化钠溶液加水稀释至500 mL,所得溶液的物质的量浓度是_____。
某学生计划用12 mol﹒L-1的浓盐酸配制0.1 mol﹒L-1的稀盐酸450 mL,回答下列问题:
(2)实验过程中,不必使用的是________(填字母)。
A.托盘天平 B.量筒 C.容量瓶 D.250 mL烧杯E.胶头滴管F.500 mL试剂瓶
(3)除上述仪器可使用外,还缺少的仪器是________。
(4)量取浓盐酸的体积为___ mL,应选用的量筒规格为______(提供10.0 mL、25.0 mL)。
(5)配制时应选用的容量瓶规格为______________。
(6)某同学操作出现以下情况,对所配溶液浓度将有何影响(填“偏高”“偏低”或“无影响”)。
定容时俯视刻度线__________加蒸馏水时不慎超过了刻度__________,此时应如何处理 ________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如表是A、B、C、D四种常见有机物的相关信息。
有机物A | 有机物B | 有机物C | 有机物D |
①可用于果实催熟 ②比例模型为 | ①由C、H两种元素组成 ②球棍模型为 | ①生活中常见的液态有机物,分子中碳原子数与有机物A相同, ②能与Na反应,但不能与NaOH反应 | ①相对分子质量比有机物C大14 ②能由有机物C氧化生成 |
根据表中信息回答下列问题:
(1)有机物A的分子式为________。
(2)下列有关有机物A、B的说法正确的是________(填字母)。
a.A、B均可使酸性KMnO4溶液褪色
b.A、B分子中所有的原子在同一平面内
c.等质量的A、B完全燃烧,消耗氧气的量相同
d.A、B分子均含有碳碳双键,能发生加成反应
(3)写出有机物C的同分异构体的结构简式:________。
(4)在一定条件下,有机物C与有机物D反应能生成具有水果香味的物质E,其化学反应方程式为_______,某次实验中,以5.0gD为原料,制得4.4gE,则D的转化率为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】固体化合物X由四种常见的元素组成,为探究其成分,某学生进行如下实验:
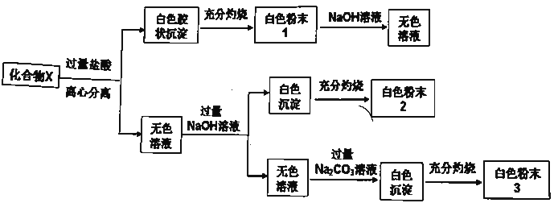
①20.8gX固体进行实验,得到白色粉末1质量12.0g,白色粉末2质量为6.0g;
②白色粉末2可用作耐高温材料,白色粉末3是一种常见干燥剂;请回答问题:
(1)X中金属元素的名称是______。
(2)化合物X与足量盐酸反应离子方程式______。
(3)在高温条件下,白色粉末2中某元素单质与白色粉末1反应,是工业制备另一种单质方法之一,写出该反应的化学方程式______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com