
【题目】可溶性钡盐有毒,医院中常用硫酸钡这种钡盐作为内服造影剂.医院抢救钡离子中毒患者时,除催吐外,还需要向中毒者胃中灌入硫酸钠溶液.已知:某温度下,Ksp(BaCO3)=5.1×10﹣9 mol2L﹣2;Ksp(BaSO4)=1.1×10﹣10 mol2L﹣2下列推断正确的是( )
A.不用碳酸钡作为内服造影剂,是因为Ksp(BaCO3)>Ksp(BaSO4)
B.抢救钡离子中毒患者时,若没有硫酸钠,可以用碳酸钠溶液代替
C.若误饮c(Ba2+)=1.0×10﹣5 molL﹣1的溶液时,会引起钡离子中毒
D.可以用0.36 molL﹣1的Na2SO4溶液给钡离子中毒患者洗胃
 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案科目:高中化学 来源: 题型:
【题目】在2010年温哥华冬季奥运会上,有个别运动员因服用兴奋剂被取消参赛的资格。下图是检测出兴奋剂的某种同系物X的结构,关于X的说法正确的是( )

A. X分子中最多有20个原子在同一平面上
B. X 遇到FeCl3溶液时显紫色,而且能使溴的四氯化碳溶液褪色
C. 1 mol X 与足量的浓溴水反应,最多消耗5 mol Br2
D. 1 mol X在一定条件下与足量的氢气反应,最多消耗1 mol H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知H2O2在催化剂作用下分解速率加快,其能量随反应进程的变化如下图所示.下列说法正确的是( ) 
A.加入催化剂,减小了反应的热效应
B.加入催化剂,可提高H2O2的平衡转化率
C.H2O2分解的热化学方程式:H2O2=H2O+ ![]() O2+Q
O2+Q
D.反应物的总能量高于生成物的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是甲、乙、丙三位同学制取乙酸乙酯的过程,请你参与并协助他们完成相关实验任务。
(1)实验目的:制取乙酸乙酯。
(2)实验原理:甲、乙、丙三位同学均采取乙醇、乙酸与浓硫酸混合共热的方法制取乙酸乙酯,反应的方程式为______________;其中浓硫酸的作用是______________。
(3)装置设计:甲、乙、丙三位同学分别设计下列三套实验装置。
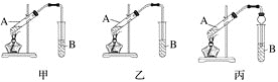
请从甲、乙两位同学设计的装置中选择一种作为实验室制取乙酸乙酯的装置,我选择的装置是______________(选填“甲”或“乙”);丙同学将甲装置中的玻璃管改成球形干燥管,除起冷凝作用外,另一重要作用是___________________________。
(4)实验步骤:
①按我选择的装置仪器,在试管中先加入2mL浓硫酸,缓缓加入3mL乙醇充分摇匀,冷却后再加入2mL冰醋酸;
②将试管固定在铁架台上;
③在试管B中加入适量的饱和碳酸钠溶液;
④用酒精灯对试管A加热;
⑤当观察到试管B中有明显现象时停止实验。
你认为实验操作中存在的错误有____________________________________________。
(5)问题讨论:
①试管B中饱和碳酸钠溶液的作用是_________________________________________。
②从试管B中分离出乙酸乙酯的实验操作是______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某温度下,将2molA和3molB充入一密闭容器中,发生反应:aA(g)+B(g)C(g)+D(g),5分钟后达到平衡,各物质的平衡浓度关系为:[c(A)]ac(B)=c(C)c(D).若在此温度下,将容器的体积扩大为原来的10倍,A的转化率不变,则此时B的转化率为( )
A.60%
B.40%
C.24%
D.4%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钠是一种非常活泼的金属元素,其单质及化合物在科研、生产中起着重要作用.
(1)利用金属钠和CO2反应可制备金刚石,其相关反应的热化学方程式如下: 4Na(g)+3CO2(g)═2Na2CO3(l)+C(s,金刚石)△H=a kJmol﹣1
CO2(g)+4Na(g)═2Na2O(s)+C(s,金刚石)△H=b kJmol﹣1
反应6Na2O(s)+2C(s,金刚石)═8Na(g)+2Na2CO3(l)的△H=kJmol﹣1(用含a、b的代数式表示).
(2)T℃时,体积为2L的恒容容器中加入一定量的Na2SO4固体和氢气,发生如下反应: Na2SO4(s)+4H2(g)Na2S(s)+4H2O(g).
①若降低温度,K值减小,则反应的△H0(填“>或“<”).
②下列说法错误的是 .
A.增加Na2SO4(s)的量可加快反应速率
B.当混合气体的密度一定时,该反应达到平衡状态
C.保持温度不变,向平衡体系中再通入一定量的H2 , △H不变
D.其他条件不变,升高温度,则v(正)增大,v(逆)减小,平衡右移
③若2min内反应达到平衡,此时气体质量增加了8g,则用H2表示的反应速率为;已知反应过程中H2的体积分数与时间的关系如上图所示,则T℃下该反应的平衡常数为 .
④若反应达平衡后,加入一定量的H2 , 再次平衡后H2O的体积分数(填“增大”“减小”或“不变”).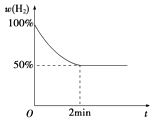
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯、乙炔、甲苯、苯乙烯( ![]() )4种有机物分别在一定条件下与H2充分反应. ①若烃与H2完全加成反应时的物质的量之比为1:3,它是 .
)4种有机物分别在一定条件下与H2充分反应. ①若烃与H2完全加成反应时的物质的量之比为1:3,它是 .
②若烃与H2完全加成反应时的物质的量之比为1:2,它是 .
③苯乙烯与H2完全加成的物质的量之比为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图甲是一种利用微生物将废水中的尿素CO(NH2)2]转化为环境友好物质的原电也装置示意图,利用该电池在图乙装置中的铁上镀铜。下列说法正确的是
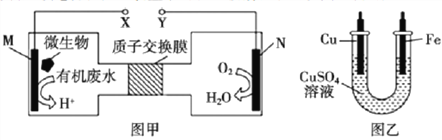
A. 图乙中Fe电极应与图甲中Y相连接
B. 图甲中H+透过质子交护膜由右向左移动
C. 图甲中M电极反应式:CO(NH2)2+5H2O-14e=CO2+2NO2+14H+
D. 当图甲中M电极消耗0.5mol尿素时,图乙中铁电极增重96g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com