
【题目】对有机物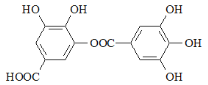 的叙述中,不正确的是
的叙述中,不正确的是
A. 常温下,该物质难溶于水
B. 1mol该有机物与NaOH溶液反应时,可消耗8mol NaOH
C. 酸性条件下水解,生成两种具有酸性的有机物
D. 遇FeCl3溶液显紫色
科目:高中化学 来源: 题型:
【题目】从石油中裂解获得A是目前工业上生产A的主要途径,图中的N是高分子化合物。以A和1,3-丁二烯为原料合成N的流程如图所示。
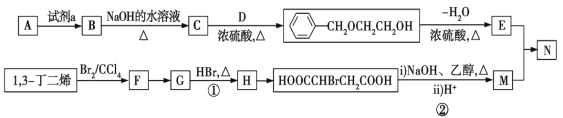
请回答下列问题:
(1)D物质的名称为________;B→C的化学方程式为_______________________。
(2)G中官能团的名称为_____________,C→E涉及的反应类型为________________。
(3)在催化剂存在下,E和M等物质的量发生聚合反应,N的结构简式为______________。
(4)E有多种同分异构体,符合下列条件的同分异构体最多有_____种(不考虑立体异构)。
①可与Na2CO3溶液反应;②分子中只有一个环状结构。
其中核磁共振氢谱中峰数最少的有机物的结构简式为____________________。
(5)试以异戊二烯CH2=C(CH3)CH=CH2为原料(其他无机试剂任选),设计制备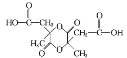 的合成路线,写出合成路线流程图(合成路线流程图可仿照题干)____________________。
的合成路线,写出合成路线流程图(合成路线流程图可仿照题干)____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaClO是漂白液的有效成分,某研究小组探究NaClO溶液的性质,设计了下列实验:
装置图 | 试剂X | 实验现象 | |
| ① | 0.2molL-1盐酸 | 产生黄绿色气体 |
② | 0.2molL-1KI-淀粉溶液 | 溶液变蓝 | |
③ | 0.2molL-1FeSO4(H+)和KSCN混合溶液 | 溶液变红 | |
④ | 0.2molL-1AlCl3溶液 | 产生白色沉淀 | |
下列判断不正确的是
A.实验①中发生的反应:ClO-+Cl-+2H+=Cl2↑+H2O
B.实验②中发生的反应:ClO-+2I-+2H+=Cl-+I2+H2O
C.实验③中该条件下氧化性强弱:ClO->Fe3+
D.实验④中ClO-与Al3+相互促进水解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面有关晶体的叙述中,不正确的是( )
A. 60gSiO2晶体中含Si-O键的个数为4NA(NA为阿伏加德罗常数)
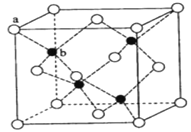
B. 在立方ZnS晶体(如图所示)中,Zn2+、S2-的配位数都是8
C. 设NaCl的摩尔质量为Mg·mol-1,NaCl的密度为ρg·cm-3,阿伏加德罗常数为NAmol-1,在NaCl晶体中,两个距离最近的Cl-中心间的距离为![]() cm
cm
D. CaO晶体结构与NaCl晶体结构相似,CaO晶体中Ca2+的配位数为6,且这些最邻近的O2-围成正八面体
查看答案和解析>>
科目:高中化学 来源: 题型:
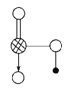
【题目】如图是Na、Cu、Si、H、C、N等元素单质的熔点高低的顺序,其中c、d均是热和电的良导体。

(1)单质a、f对应的元素以原子个数比1:1形成的分子(相同条件下对H2的相对密度为13)中含____个σ键,____个键。
(2)a与b的元素形成的10电子中性分子X的空间构型为_____;将X溶于水后的溶液滴入到AgNO3溶液中至过量,得到配离子的化学式为_____,其中X与Ag+之间以_____键结合。
(3)氢键的形成对物质的性质具有一定的影响.![]() 的沸点_____。(填高或低)
的沸点_____。(填高或低)
(4)如图是上述六种元素中的一种元素形成的最高价含氧酸的结构:请简要说明该物质易溶于水的两个原因:_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁被誉为“第一金属”,铁及其化合物在生活中有广泛应用
(1)基态Fe3+的电子排布式为________。
(2)实验室用KSCN溶液、苯酚(![]() )检验Fe3+。N、O、S的第一电离能由大到小的顺序为_______(用元素符号表示),苯酚中碳原子的杂化轨道类型为______。
)检验Fe3+。N、O、S的第一电离能由大到小的顺序为_______(用元素符号表示),苯酚中碳原子的杂化轨道类型为______。
(3)FeCl3的熔点为306℃,沸点为315℃ FeCl3的晶体类型是______。FeSO4常作补铁剂,SO42-的立体构型是_______。
(4)基铁[Fe(CO)5]可用作催化剂、汽油抗爆剂等,1 mol Fe(CO)5分子中含σ键数目为_______,与CO互为等电子体的离子是__________(填化学式,写一种)
(5)氮化铁晶体的晶体结构示意图如图1所示。该晶体中铁、氮的微粒个数之比为______。
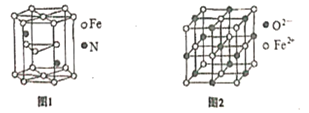
(6)氧化亚铁晶体的晶胞如图2所示。已知:氧化亚铁晶体的密度为ρg·cm-1,NA代表阿伏加德罗常数的值。在该晶胞中,与Fe2+紧邻且等距离的Fe2+数目为_____;Fe2+与O2-的最短间距为_______ pm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分枝酸可用于生化研究,其结构简式如图。下列关于分枝酸的叙述正确的是

A. 分子中含有3种官能团
B. 分枝酸的分子式为C10H10O6
C. 1mol分枝酸最多可与3molNaOH发生中和反应
D. 可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】麻黄素M是拟交感神经药。合成M的一种路线如图所示:
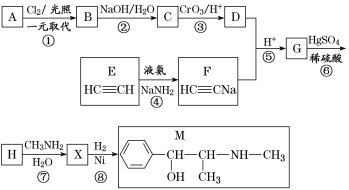
已知:Ⅰ.芳香烃A的相对分子质量为92
Ⅱ.R—CH2OH![]() RCHO
RCHO
III、R1-CHO+
IV、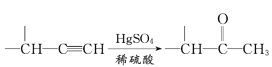
V、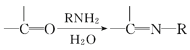
请回答下列问题:
(1)D的名称是_______;G中含氧官能团的名称是_______。
(2)反应②的反应类型为_______;A的结构简式为_______。
(3)写出反应⑦的化学方程式:______________________________。
(4)X分子中最多有_______个碳原子共平面。
(5)在H的同分异构体中,同时能发生水解反应和银镜反应的芳香族化合物中,核磁共振氢谱上有4组峰,且峰面积之比为1∶1∶2∶6的有机物的结构简式为_________________。
(6)已知:![]() 仿照上述流程,设计以苯、乙醛为主要原料合成某药物中间体
仿照上述流程,设计以苯、乙醛为主要原料合成某药物中间体![]() 的路线________________。
的路线________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,反应:6H2 + 2CO2![]() C2H5OH + 3H2O的数据如下图所示。
C2H5OH + 3H2O的数据如下图所示。


下列说法正确的是
A.该反应的△H > 0
B.达平衡时,v(H2)正 = v(CO2)逆
C.b点对应的平衡常数K值大于c点
D.a点对应的H2的平衡转化率为90 %
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com