
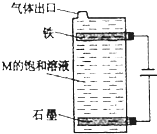
 �ס��ҡ����������졢��Ϊԭ��������������Ķ���������Ԫ�أ��ס�������ͬһ���壬���������촦��ͬһ���ڣ���Ԫ������ϼ�����ͼ۵Ĵ�����Ϊ0�����������������������ˮ����֮�䶼�ܷ�����Ӧ���û�ѧ����ش��������⣺
�ס��ҡ����������졢��Ϊԭ��������������Ķ���������Ԫ�أ��ס�������ͬһ���壬���������촦��ͬһ���ڣ���Ԫ������ϼ�����ͼ۵Ĵ�����Ϊ0�����������������������ˮ����֮�䶼�ܷ�����Ӧ���û�ѧ����ش��������⣺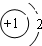 ���õ���ʽ��ʾ����̼���γɻ�����Ĺ���Ϊ
���õ���ʽ��ʾ����̼���γɻ�����Ĺ���Ϊ ��
��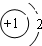 ��
�� ��
��
| ||
| ||


 ȫ�̽��ϵ�д�
ȫ�̽��ϵ�д� ����5��2���ϵ�д�
����5��2���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����ͬ���ʵ���Ũ�ȵ�������Һ�У���NH4Al��SO4��2����NH4Cl����CH3COONH4����NH3?H2O��c��NH4+���ɴ�С��˳���ǣ��٣��ڣ��ۣ��� |
| B��ij���ʵ���Һ����ˮ�������c��H+��=1��10-amol/L����a��7ʱ�������Һ��pHһ��Ϊ14-a |
| C�����ʵ���Ũ����ȵ�H2S��NaHS�����Һ�У�c��Na+��+c��H+��=c��S2-��+c��HS-��+c��OH-��? |
| D��AgCl����Һ�д���ƽ�⣺AgCl��s��?Ag+��aq��+Cl- ��aq���������м�������NaCl��ĩ��ƽ��������ƶ�����Һ�����ӵ���Ũ�Ȼ��С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| t/s | 0 | 2 | 4 | 6 | 8 |
| n��Cl2��/mol | 0 | 0.30 | 0.39 | 0.40 | 0.40 |
| A��A�����������������䣬�����¶ȣ�ƽ��ʱc��Cl2��=0.22 mol?L-1����Ӧ�ġ�H��0 |
| B������2 L���ݾ��ȣ������û�������������ܱ��������и÷�Ӧ����ѧƽ�ⳣ������ |
| C�����������������䣬��ʼ�������г���1.2 molCOCl2��0.60 molCl2��0.60 molCO����Ӧ�ﵽƽ��ǰ�����ʣ�v��������v���棩 |
| D�����������������䣬��ʼ�������г���1.0 molCl2��0.8 molCO���ﵽƽ��ʱ��Cl2��ת����С��60% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���٢� | B���ڢۢ� |
| C���٢ۢ� | D���٢ڢۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��CuCl2+2NaOH�TCu��OH��2��+2NaCl��Cu2++20H�TCu��OH��2�� |
| B��BaSO4+2HCl�TBaCl2+CO2��+H2O��SO42-+2H+�TCO2��+H2O |
| C��Ca��NO3��2+Na2CO3�TCaCO3��+2NaNO3 Ca2++CO32-�TCaCO3�� |
| D��2KOH+H2SO4�TK2SO4+2H2O��H++OH-�TH2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 W��X��Y��Z�����ֳ����Ķ�����Ԫ�أ���ԭ�Ӱ뾶��ԭ�������仯��ͼ��ʾ����֪W��һ�ֺ��ص�������Ϊ18��������Ϊ10��X��Neԭ�ӵĺ�����������1��Y�ĵ�����һ�ֳ����İ뵼����ϣ�Z�ķǽ�������ͬ����Ԫ������ǿ������˵����ȷ���ǣ�������
W��X��Y��Z�����ֳ����Ķ�����Ԫ�أ���ԭ�Ӱ뾶��ԭ�������仯��ͼ��ʾ����֪W��һ�ֺ��ص�������Ϊ18��������Ϊ10��X��Neԭ�ӵĺ�����������1��Y�ĵ�����һ�ֳ����İ뵼����ϣ�Z�ķǽ�������ͬ����Ԫ������ǿ������˵����ȷ���ǣ�������| A��������YZ4�Ȼ�����XZ�۵�� |
| B��W��X��W��Z�����γ�ij�־���Ư���ԵĻ������ԭ����ͬ |
| C��������X2YW3�Ⱥ����Ӽ����ֺ����ۼ�������ճ�����ͷ���� |
| D��Y����������Z���⻯�X������������Ӧ��ˮ�������Һ���ܷ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ͭ�� |
| B������ |
| C��� |
| D��Fe3��SO4��3 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com