
【题目】黄铁矿(FeS2)催化氧化的化学方程式为:2FeS2+7O2+2H2O 2FeSO4+2H2SO4。已知NA是阿伏加德罗常数的值,下列说法正确的是
2FeSO4+2H2SO4。已知NA是阿伏加德罗常数的值,下列说法正确的是
A.FeSO4和H2SO4都是离子化合物,均属于强电解质
B.0.1 mol·L-1 FeSO4 溶液中Fe2+离子的浓度为0.1 mol·L-1
C.FeSO4既是被氧化得到的产物,又是被还原得到的产物
D.当转移2 mol电子时,消耗氧气的体积(标准状况)约为22.4 L
【答案】C
【解析】
A.FeSO4属于盐,是离子化合物,H2SO4属于酸,是共价化合物,它们均属于强电解质,故A错误;
B.FeSO4溶液中Fe2+离子容易水解,故0.1 mol·L-1 FeSO4溶液中Fe2+离子的浓度小于0.1 mol·L-1,故B错误;
C.根据反应2FeS2+7O2+2H2O 2FeSO4+2H2SO4,FeS2中亚铁离子的化合价为+2价,硫元素的化合价为-1价,单质氧气中氧元素的化合价为0价,硫酸亚铁中,铁元素的化合价为+2价,硫元素的化合价为+6价,氧元素的化合价为-2价,硫元素的化合价升高到+6价,氧气单质中的氧元素的化合价降低到-2价,FeSO4既是被氧化得到的产物,又是被还原得到的产物,故C正确;
2FeSO4+2H2SO4,FeS2中亚铁离子的化合价为+2价,硫元素的化合价为-1价,单质氧气中氧元素的化合价为0价,硫酸亚铁中,铁元素的化合价为+2价,硫元素的化合价为+6价,氧元素的化合价为-2价,硫元素的化合价升高到+6价,氧气单质中的氧元素的化合价降低到-2价,FeSO4既是被氧化得到的产物,又是被还原得到的产物,故C正确;
D.根据反应2FeS2+7O2+2H2O 2FeSO4+2H2SO4可知,7mol氧气参加反应,氧元素化合价从0降低到-2价,共转移28mol电子,当转移2 mol电子时,消耗氧气的物质的量为0.5mol,标准状况下的体积约为0.5mol×22.4 L/mol=11.2L,故D错误;
2FeSO4+2H2SO4可知,7mol氧气参加反应,氧元素化合价从0降低到-2价,共转移28mol电子,当转移2 mol电子时,消耗氧气的物质的量为0.5mol,标准状况下的体积约为0.5mol×22.4 L/mol=11.2L,故D错误;
答案选C。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是( )
A.铁粉放入稀硫酸溶液:2Fe+6H+═2Fe3++3H2↑
B.往NH4HCO3溶液中加过量的NaOH溶液并加热:NH4++OH﹣![]() NH3↑+H2O
NH3↑+H2O
C.石灰石与稀盐酸反应:CO32﹣+2H+═ CO2↑+H2O
D.Cl2通入水中:Cl2+H2O = H++Cl﹣+HClO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某粗盐样品中含有Na2SO4、MgCl2、CaCl2等杂质.实验室提纯流程如下:
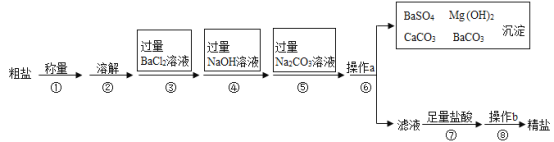
(1)用托盘天平称量粗盐时,若砝码和粗盐位置放颠倒,天平平衡时,读数为5.4g,实际称得粗盐的质量是__________。
A.5.4g B.4.6g C.6.0g D.5.0g
(2)第③步操作发生反应的化学方程式是__________________________
(3)第④步操作发生反应的化学方程式是_______________________
(4)第⑤步操作的目的是 ___________________________
(5)第⑥步操作a的名称是 ________,此步操作中,玻璃棒的末端要轻轻地斜靠在 _____________的一边。
(6)第⑦步操作中,向滤液中滴加足量盐酸的目的是_____________,此步操作中产生气泡的化学方程式是___________________。
(7)在第⑧步操作时,要用玻璃棒不断搅拌,目的是_______________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于金属的说法正确的是
A. 铝箔在空气中受热可以熔化且会发生剧烈燃烧
B. ![]() 在空气中燃烧,发出黄色火焰,生成白色固体
在空气中燃烧,发出黄色火焰,生成白色固体
C. 铁与水蒸气反应的产物是黑色的![]()
D. 铝制餐具不宜用来盛装酸性、碱性较强的食物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酸铈[Ce2(CO3)3]是制备稀土发光材料、汽车尾气净化催化剂的重要原料。碳酸铈可由铈的氯化物和碳酸氢铵反应制备。甲同学利用下列装置模拟制备Ce2(CO3)3:
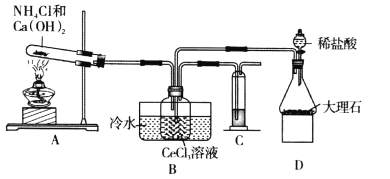
已知:i.装置C中溶液为亚硫酸钠溶液;
ii.Ksp[Ce2(CO3)3]=1.00×10-28;
iii.Ce3+易被空气氧化成Ce4+。
(1)装置D中盛放稀盐酸的实验仪器名称为________,装置C中溶液的作用是________。
(2)装置A中发生的化学反应方程式为________。
(3)实验装置中有一处不合理,请针对不合理之处写出改进措施:________。
(4)装置B中制备Ce2(CO3)3反应的离子方程式为________。
(5)实验过程中当Ce3+沉淀完全时![]() ,溶液中
,溶液中![]() 为________。
为________。
(6)Ce2(CO3)3在装置B中沉淀,然后经过静置、过滤、洗涤、干燥后即可得到产品。检验产品是否洗涤干净的方法为________。
(7)为测定产品中Ce2(CO3)3的纯度,取![]() 产品加入稀硫酸、
产品加入稀硫酸、![]() 溶液至全部溶解,配成
溶液至全部溶解,配成![]() 溶液,取
溶液,取![]() 溶液用
溶液用![]() 的
的![]() 溶液滴定至终点(铈被还原成Ce3+),消耗
溶液滴定至终点(铈被还原成Ce3+),消耗![]() 溶液
溶液![]() ,则产品中Ce2(CO3)3的纯度为________。
,则产品中Ce2(CO3)3的纯度为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜板上铁铆钉处的吸氧腐蚀原理如图所示,下列有关说法中,不正确的是

A. 正极电极反应式为:2H++2e—→H2↑
B. 此过程中还涉及到反应:4Fe(OH)2+2H2O+O2=4Fe(OH)3
C. 此过程中铜并不被腐蚀
D. 此过程中电子从Fe移向Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】气态亚硝酸(HNO2或HONO)是大气中的一种污染物。
(1)亚硝酸的电离平衡常数Ka=6.0×10﹣6,其电离方程式为________。
(2)亚硝酸分子中各原子最外层电子均达到稳定结构,其电子式为________。
(3)亚硝酸进入人体可以与二甲胺[(CH3)2NH]迅速反应生成亚硝酸胺[CH3)2N-N=O],亚硝酸胺是最重要的化学致癌物之一。
① 亚硝酸与二甲胺反应生成亚硝酸胺的一种反应机理如下:
HONO+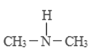
![]()
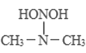
![]()
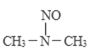
过程ⅰ和过程ⅱ的反应类型分别为:________、消去反应。
② 上述反应机理的反应过程与能量变化的关系如图:
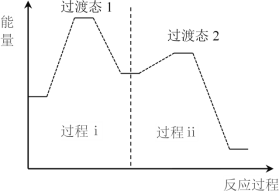
亚硝酸与二甲胺反应生成亚硝酸胺的反应ΔH________0(填“>”或“<”)。反应难度更大的是过程________(填“ⅰ”或“ⅱ”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列措施或事实不能用勒夏特列原理解释的是
A.新制的氯水在光照下颜色变浅
B.NO2和N2O4平衡混合气缩小体积加压后颜色先变深后变浅一点
C.高锰酸钾溶液与草酸发生化学反应刚开始缓慢,随后反应迅速加快
D.硫酸工业上SO2氧化成SO3,通入过量的空气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子序数依次增大的短周期元素X、Y、Z、W、M可形成a、b两种化合物(如图),a为磁共振氢谱中常用的参照物,b为有机合成中的一种还原剂。下列说法错误的是
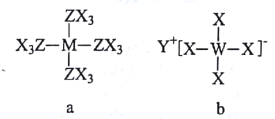
A.原子半径:W>M>Z
B.元素非金属性:Z>M
C.W的最高价氧化物的水化物具有两性
D.常温常压下X与Z形成的化合物为气态
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com