
����Ŀ����̬������(HNO2��HONO)�Ǵ����е�һ����Ⱦ�
(1)������ĵ���ƽ�ⳣ��Ka��6.0��10��6������뷽��ʽΪ________��
(2)����������и�ԭ���������Ӿ��ﵽ�ȶ��ṹ�������ʽΪ________��
(3)��������������������װ�[(CH3)2NH]Ѹ�ٷ�Ӧ���������᰷[CH3)2N��N��O]�������᰷������Ҫ�Ļ�ѧ�°���֮һ��
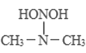
�� ����������װ���Ӧ���������᰷��һ�ַ�Ӧ�������£�
HONO+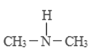
![]()
![]()
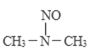
���̢����̢��ķ�Ӧ���ͷֱ�Ϊ��________����ȥ��Ӧ��
�� ������Ӧ�����ķ�Ӧ�����������仯�Ĺ�ϵ��ͼ��
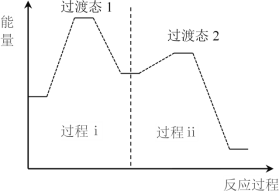
����������װ���Ӧ���������᰷�ķ�Ӧ��H________0(����������������)����Ӧ�Ѷȸ�����ǹ���________(����������������)��
���𰸡�HNO2 H+��NO2�� ![]() �ӳɷ�Ӧ �� ���̢�
�ӳɷ�Ӧ �� ���̢�
��������
(1)��������ĵ��볣������ֵ��֪������һ��һԪ���
(2)���������ڹ��ۻ�����ݴ���д����ʽ��
(3)������������к��е���˫�����������ķ�Ӧ��������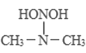 ����˫����ʧ����Ϊ������������������
����˫����ʧ����Ϊ������������������ ����ȥһ���ǻ�����ԭ�ӣ��γɵ���˫��������л���ķ�Ӧ���ͷ�����
����ȥһ���ǻ�����ԭ�ӣ��γɵ���˫��������л���ķ�Ӧ���ͷ�����
�ڸ��ݸ�˹���ɷ�������ѧ��Ӧ����ЧӦֻ����ʼ������״̬�йأ���仯;���ط����жϣ����Խ��Ӧ���е�Խ������Ӧ�Ѷ�Խ��
(1)��������ĵ��볣������ֵ��֪������һ��һԪ���ᣬ����Һ�в��ֵ��룬���뷽��ʽΪHNO2 H+��NO2����
(2)���������ڹ��ۻ���������и�ԭ���������Ӿ��ﵽ�ȶ��ṹ�������ʽΪ![]() ��
��
(3)������������к��е���˫�������̢��ķ�Ӧ�������� ����˫����ʧ����Ϊ�������������Կ���
����˫����ʧ����Ϊ�������������Կ���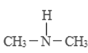 �еĵ�������ѣ��ֱ�ӳ�����������ӵĵ���˫�����ˣ����Կ����Ǽӳɷ�Ӧ�����̢���
�еĵ�������ѣ��ֱ�ӳ�����������ӵĵ���˫�����ˣ����Կ����Ǽӳɷ�Ӧ�����̢��� ����ȥһ���ǻ�����ԭ�ӣ��γɵ���˫�������Կ����л���Ӧ�д��ǻ�����ȥ��Ӧ��
����ȥһ���ǻ�����ԭ�ӣ��γɵ���˫�������Կ����л���Ӧ�д��ǻ�����ȥ��Ӧ��
�ڸ��ݸ�˹���ɷ�������ѧ��Ӧ����ЧӦֻ����ʼ������״̬�йأ���仯;���أ�����ͼʾ����Ӧ�����������������������������÷�Ӧ���ڷ��ȷ�Ӧ����H��0�������ָ���Ӵӳ�̬ת��Ϊ��������ѧ��Ӧ�Ļ�Ծ״̬(����̬)����Ҫ�����������Խ��Ӧ���е�Խ������Ӧ�Ѷ�Խ����ͼʾ�����̢��Ļ�ܴ��ڹ��̢��Ļ�ܣ�����̢��ķ�Ӧ�Ѷȸ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ����������ԭ���������ε����Ķ�����Ԫ��W��X��Y��Z���������һ�ֳ����ӣ����и�Ч�Ĵ����ܣ�����ӽṹʾ��ͼ��ͼ��W��X��Z�ֱ�λ�ڲ�ͬ���ڣ�Z��ԭ�Ӱ뾶��ͬ����Ԫ�������ע��ʵ�ߴ������ۼ��������ظ���Ԫ��W��Xδ��ע������˵������ȷ���ǣ� ��
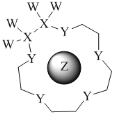
A.Y���ʵ���������ͬ��������ǿ
B.���Ӱ뾶��Z>Y
C.Z��Y����ɶ������ӻ�����
D.�⻯������ȶ��ԣ�Y>X
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Fe3+��SO32-���ܴ��������ԭ���Ǵ���������ԭ��Ӧ��˫ˮ�ⷴӦ֮������ͼ�������ֳּ���������FeCl3��Һ�μ�Na2SO3��Һ�����е�pH�͵絼�ʵı仯�����
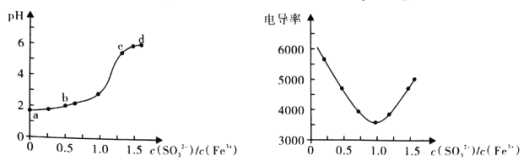
ʵ����̻����֣�
i.b��ʱ��Һ�������������зֱ����KSCN��Һ��NaOH��Һ������ֱ�Ϊ����Ѫ��ɫ�ͻ���ɫ�����
ii.c���d����������Ժ��ɫ�����ȡ�ϲ���Һ���ֱ����KSCN��Һ��NaOH��Һ������ֱ�Ϊ����Ѫ��ɫ�������Ա仯��
���������Ϣ�����з�������������
A.a����Һ������ʱ���������
B.���b�㸽��pH�ı仯�Լ�ʵ������˵���˴�������������ԭ��Ӧ
C.c����Һ�з�������Ҫ��ӦΪ2Fe3++3SO32-+6H2O=2Fe(OH)3��+3H2SO3
D.ȡd�㴦�ϲ���Һ�������еμ�K3[Fe(CN)6]����Һ�������ɫ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������(FeS2)�������Ļ�ѧ����ʽΪ��2FeS2��7O2��2H2O 2FeSO4��2H2SO4����֪NA�ǰ����ӵ�������ֵ������˵����ȷ����
2FeSO4��2H2SO4����֪NA�ǰ����ӵ�������ֵ������˵����ȷ����
A.FeSO4��H2SO4�������ӻ����������ǿ�����
B.0.1 mol��L��1 FeSO4 ��Һ��Fe2�����ӵ�Ũ��Ϊ0.1 mol��L��1
C.FeSO4���DZ������õ��IJ�����DZ���ԭ�õ��IJ���
D.��ת��2 mol����ʱ���������������(��״��)ԼΪ22.4 L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾһ�����أ�װ�е��Һa��X��Y������缫�壬ͨ��������ֱ����Դ��������ش��������⣺

��.��X��Y�Ƕ��Ե缫��a�DZ���NaCl��Һ��ʵ�鿪ʼʱ��ͬʱ�����߸����뼸�η�̪��
��1��д����ⱥ��ʳ��ˮ�����ӷ���ʽ____��
��2����X�������۲쵽��������____��
�����õ�ⷽ��������ͭ�����Һaѡ��CuSO4��Һ����
��1��X�缫�缫��Ӧʽ��____��Y�缫�IJ�����___��
��2������·����0.04mol����ͨ��ʱ����������___g��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��˫�������Դ�����ҩ��ϳ�������Ҫ�����á�����һ�ִ���I�ĺϳ�·�����£�
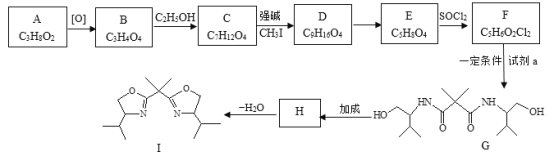
��֪��R-NH2+![]()
![]()
![]()
(1)A����Na��Ӧ������H2����A�еĹ�����������_________��
(2)���й���A��˵���У���ȷ����_________��
a.���Ҵ���Ϊͬϵ��
b.��B��һ�������¿ɷ������۷�Ӧ
c.������ȥ��Ӧ���Լ��������ǣ�NaOH�Ĵ���Һ������
(3)д��B��C�Ļ�ѧ����ʽ��___________��
(4)D�Ľṹ��ʽ��__________��
(5)E��F�ķ�Ӧ������___________��
(6)��֪��NH3+![]() ��H2N-CH2CH2OH��NH3������K������Ӧ�����Ʊ��Լ�a��K�Ľṹ��ʽ��__________��
��H2N-CH2CH2OH��NH3������K������Ӧ�����Ʊ��Լ�a��K�Ľṹ��ʽ��__________��
(7)F��Ա�����(![]() )��һ�������¿ɷ������۷�Ӧ�Ʊ�����MXD6������Ʒ���÷�Ӧ�Ļ�ѧ����ʽ��___________��
)��һ�������¿ɷ������۷�Ӧ�Ʊ�����MXD6������Ʒ���÷�Ӧ�Ļ�ѧ����ʽ��___________��
(8)H�Ľṹ��ʽ��___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����н�����ʵ�ķ���ʽ����ȷ����
A.�������죺 2Fe + Al2O3![]() 2Al + Fe2O3
2Al + Fe2O3
B.��ҵ�̵��� N2 + 3H2![]() 2NH3
2NH3
C.�ô�������ۣ�CO32-+H2O![]() HCO3-+ OH-
HCO3-+ OH-
D.��ʪ��ĵ���KI��ֽ����Cl2��Cl2 + 2I-=2Cl-+I2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Υ����ѧԭ������
A.������ˮΪ֮��������ˮ��˵����ͬ������ˮ�ͱ���ˮ��������
B.��ӦA(g)+3B(g)![]() 2C(g)��ƽ����¶Ȳ��䣬����ѹǿ��ƽ�������ƶ���ƽ�ⳣ��Kֵ����
2C(g)��ƽ����¶Ȳ��䣬����ѹǿ��ƽ�������ƶ���ƽ�ⳣ��Kֵ����
C.SO2�Ĵ�������һ�����ȵķ�Ӧ�������¶ȣ���Ӧ���ʼӿ�
D.��Ԫ����������볣�����ϵΪK1![]() K2
K2![]() K3
K3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������������ڹ�ҵӦ���й㷺��ij�����ӷ����л��ս�������������Ҫ�ɷ���V2O3��FeO��������������CuO��Al2O3������������ͼ��
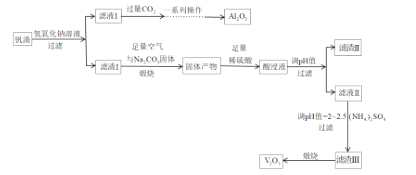
��֪����KspCu(OH)2=1.0��1021��KspFe(OH)3=4.0��1038��KspFe(OH)2=8.0��1016��
��NH4VO3������ˮ��(VO2)2SO4������ˮ��
��1��д����ҺI�м��������CO2ʱ������Ӧ�����ӷ���ʽ����ȡ������Al2O3��Ҫ����һϵ�в��������ˡ�___��___��
��2������ʱ������I����Ҫ�ɷ�V2O3ת��Ϊ������NaVO3��д���䷴Ӧ�Ļ�ѧ����ʽ___��
��3������ϡ��������Һ��VO3��VO2+�ܴ��������ԭ����___�������ӷ���ʽ���ͣ���
��4�������µ������Һ��pH=___����������ȫ��ȥ����ͭ����Ԫ�ض�Ӧ������___��ʵ��pHֵҪ������8����Ŀ����___����pH=2~2.5����ˣ�����III����Ҫ�ɷ�Ϊ___��
��5����д����������IIIʱ��������Ӧ�Ļ�ѧ����ʽ___��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com