
【题目】美国斯坦福大学的工程师设计出一种从污水“提取”潜在电能的新型微生物电池,该电池能将生活污水中的有机物分解同时发电,电池结构如图所示。已知a电极为惰性材料,b电极为Ag2O。下列说法不正确的是( )
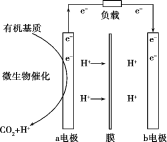
A.a电极是负极,b电极是正极
B.b电极发生的反应是Ag2O+2e-+2H+=2Ag+H2O
C.a电极每生成标准状况下2.24LCO2,可向b电极转移0.1mol电子
D.高温条件下,该电池不能正常工作
科目:高中化学 来源: 题型:
【题目】化学反应有物质的变化过程中还有能量的转化,据此回答下列问题:
(1)已知甲醇的燃烧热为725.8kJ·mol-1,写出表示其燃烧热的热化学方程式:_______。
(2)已知反应2HI(g)=H2(g)+I2(g)的△H=+11kJ·mol-1,1mol H2(g)、1mol I2(g)分子中化学键断裂时分别需要吸收436kJ、151kJ的能量,则1mol HI (g)分子中化学键断裂时需吸收的能量为_____kJ。
(3)己知:CO(g)+2H2(g) →CH3OH(g)△H1=-90.1 kJ·mol-1;3CH3OH(g) ![]() CH3CH=CH2(g)+H2O(g) △H2=-31.0 kJ·mol-1则CO与H2合成CH3CH=CH2的热化学方程式为________。
CH3CH=CH2(g)+H2O(g) △H2=-31.0 kJ·mol-1则CO与H2合成CH3CH=CH2的热化学方程式为________。
(4)甲醇-空气燃料电池(DMFC)是一种高效能、轻污染电动汽车的车载电池。其工作原理示意如图:
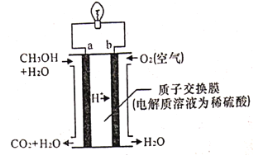
则其负极反应式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙烯酸甲酯(CH2=CHCOOCH3)是一种重要的有机化工原料。实验室制备少量丙烯酸甲酯的反应为:CH2=CHCOOH+CH3OH![]() CH2=CHCOOCH3+H2O,步骤如下:
CH2=CHCOOCH3+H2O,步骤如下:
步骤1:在100mL圆底烧瓶中依次加入10.0g丙烯酸、少许碎瓷片、10mL甲醇和2mL浓硫酸,搅拌。
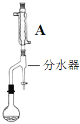
步骤2:如图,连接装置,加热烧瓶中的混合液,用锥形瓶盛接通过分水器分离出的水。当不再有水生成,停止加热。
步骤3:反应液冷却后,依次用5%Na2CO3溶液、饱和食盐水、水洗涤。分离出有机相。
步骤4;向有机相中加无水Na2SO4固体,过滤后蒸馏,收集70~90℃馏分。测得丙烯酸甲酯的质量为6.45g。
可能用到的信息:
密度 | 沸点 | 溶解性 | ||
丙烯酸 | 1.05g·cm-3 | 141℃ | 与水互溶,易溶于有机溶剂 | 有毒 |
甲醇 | 0.79g·cm-3 | 65℃ | 与水互溶,易溶于有机溶剂 | 易挥发,有毒 |
丙烯酸甲酯 | 0.95g·cm-3 | 80.5℃ | 难溶于水,易溶于有机溶剂 | 易挥发 |
请回答下列问题:
(1)步骤1中,加入碎瓷片的目的是__。
(2)步骤2中,图中所示装置中仪器A的名称是__,其作用为__。
(3)步骤3中,用5%Na2CO3溶液洗涤后,分离有机相的操作名称为__。
(4)实验中可能生成的有机副产物结构简式为__(填一种即可)。
(5)本实验中丙烯酸甲酯的产率为__%。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】今年是门捷列夫发现元素周期律150周年。下表是元素周期表的一部分,W、X、Y、Z为短周期主族元素,W与X的最高化合价之和为8。下列说法错误的是
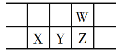
A. 原子半径:W<X
B. 常温常压下,Y单质为固态
C. 气态氢化物热稳定性:Z<W
D. X的最高价氧化物的水化物是强碱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】加热蒸干氯化镁溶液时因水解不完全会得到一种灰白色沉淀——碱式氯化镁,化学式可表示为Mgx(OH)yClz·nH2O,设计如图装置验证其化学式。下列有关实验的说法不正确的是( )
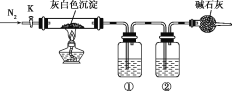
A.碱式氯化镁受热分解可以生成氧化镁、氯气和水
B.结束反应时,先停止加热,通一段时间N2后再关闭活塞K
C.①②中依次盛装浓硫酸、氢氧化钠溶液
D.只需称量原样品质量、反应结束后硬质玻璃管中剩余固体质量以及装置①增重的质量即可推出其化学式
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二水合草酸亚铁(FeC2O42H2O)是制备某种铁锂电池最常用的原料。国内某科研团队以氮气为保护气,对二水合草酸亚铁的受热分解情况进行研究,生成的气体只含CO、CO2和H2O(g),得到固体质量与加热温度的变化曲线如图所示。下列说法正确的是
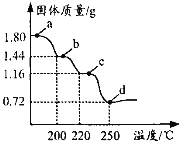
A.b点的固体成份为FeC2O4H2O
B.b→c 的方程式为 FeC2O4![]() FeCO3+CO↑
FeCO3+CO↑
C.从a→d, 生成的CO、CO2的物质的量相等
D.加热至250℃以上,固体质量略有增加,可能是因为FeO与CO反应生成了 Fe3C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,a、b是两根石墨棒。下列叙述正确的是( )
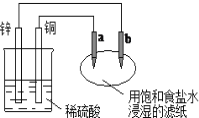
A.a是正极,发生还原反应
B.b是阳极,发生氧化反应
C.往滤纸上滴加酚酞试液,a极附近颜色变红
D.稀硫酸中硫酸根离子的物质的量不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T ℃时,将5mol A和7mol B气体通入体积为10L的密闭容器中(容积不变),反应过程中A、B、C的浓度变化如图Ⅰ所示。若保持其他条件不变,温度分别为T1和T2时,B的体积分数与时间关系如图Ⅱ所示:
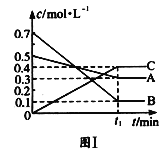
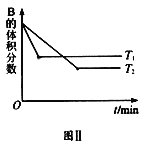
则下列结论正确的是( )
A.T ℃时,将4mol A、4mol B和2mol C气体通入体积为10L的密闭容器中(容积不变),达到平衡时,C的浓度为0.4 mol·L-1
B.保持其他条件不变,在(t1+10)min 时,加入催化剂,平衡向正反应方向移动
C.保持其他条件不变,在(t1+10)min 时,通入稀有气体,平衡向逆反应方向移动
D.保持其他条件不变,升高温度,正、逆反应速率均增大,A的转化率也增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某班同学用以下实验探究![]() 、
、![]() 的性质。回答下列问题:
的性质。回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁、溴化亚铁固体,均配制成![]() 的溶液。在
的溶液。在![]() 溶液中需加入少量铁屑,其目的是_____________________________________。
溶液中需加入少量铁屑,其目的是_____________________________________。
(2)甲组同学取![]() 溶液,加入几滴氯水,再加入1滴
溶液,加入几滴氯水,再加入1滴![]() 溶液,溶液变红,说明
溶液,溶液变红,说明![]() 可将
可将![]() 氧化。
氧化。![]() 溶液与氯水反应的离子方程式为____________________。
溶液与氯水反应的离子方程式为____________________。
(3)乙组同学认为甲组的实验不够严谨,该组同学在![]() 溶液中先加入
溶液中先加入![]() 煤油,再向下层溶液中依次加入几滴氯水和1滴
煤油,再向下层溶液中依次加入几滴氯水和1滴![]() 溶液,溶液变红。煤油的作用是_________________________。
溶液,溶液变红。煤油的作用是_________________________。
(4)丙组同学取![]() 上述
上述![]() 溶液,向其中滴加少量新制的氯水,振荡后溶液呈黄色。某同学对产生黄色的原因提出了假设:
溶液,向其中滴加少量新制的氯水,振荡后溶液呈黄色。某同学对产生黄色的原因提出了假设:
假设1:![]() 被
被![]() 氧化成
氧化成![]() 溶解在溶液中;
溶解在溶液中;
假设2:![]() 被
被![]() 氧化成
氧化成![]() 。
。
请你完成下表,验证假设
实验步骤、预期现象 | 结论 |
①向溶液中加入____________,振荡、静置现象:____________ | 假设1正确 |
②向溶液中加入____________,现象:____________ | 假设2正确 |
(5)已知:![]() 。若在
。若在![]() 上述
上述![]() 溶液中通入标准状况
溶液中通入标准状况![]() ,反应的离子方程式为________________________________。
,反应的离子方程式为________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com