
【题目】(1)已知氯气通入热的苛性钠溶液中会发生如下反应:3Cl2+6NaOH=5NaCl+NaClO3+3H2O反应中还原剂是___(填化学式);把此反应改写成离子方程式:___;
(2)用“双线桥”表示下列氧化还原反应中电子转移的方向和数目:3Cl2+6NaOH=5NaCl +NaClO3+3H2O。___
(3)若生成1mol的NaClO3,转移的电子数是___;若反应中转移了2.5mol的电子,则消耗标况下Cl2的体积是___。
【答案】Cl2 3Cl2+6OH-═5Cl-+ClO3-+3H2O 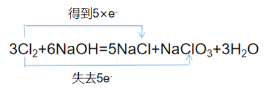 5NA 33.6L
5NA 33.6L
【解析】
反应方程式中共6个Cl原子,5个Cl原子得电子化合价降低,由0价降低到-1价,被还原,做氧化剂。 1个Cl原子失电子化合价升高,由0价升高到+5价,被氧化,做还原剂。
(1)由题意可知,Cl2的化合价升高,做还原剂,反应中的还原剂为Cl2,离子方程式为:3Cl2+6OH-═5Cl-+ClO3-+3H2O;
故答案为:Cl2 ;3Cl2+6OH-═5Cl-+ClO3-+3H2O
(2)5个Cl原子得5个电子,化合价由0价降低到-1价,1个Cl原子失去5个电子,化合价0价升高到+5价,用双线桥表示法表示为: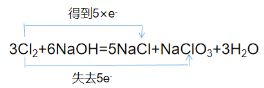 。
。
故答案为: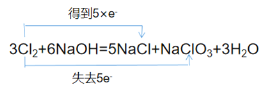 。
。
(3)由分析可知生成1mol的NaClO3,化合价由0价升高到+5价,需要转移5mol电子,即转移电子数为5NA,若反应中转移了2.5mol的电子,则消耗Cl2的物质的量为1.5mol,标况下1.5molCl2的体积为V=n×Vm=1.5mol×22.4mol/L=33.6L。
故答案为:5NA;33.6L


科目:高中化学 来源: 题型:
【题目】Ⅰ.有下列8种晶体,用序号回答下列问题:
A.水晶 B.冰醋酸 C.白磷 D.固态氩 E.氯化铵 F.铝 G.金刚石
(1)属于原子晶体的化合物是___,属于离子晶体的是___,不含化学键的分子晶体是____。
(2)由极性分子构成的晶体是___,含有共价键的离子晶体是___,属于分子晶体的单质是____。
(3)分子内存在化学键,但受热熔化时,化学键不发生变化的是___,受热熔化,需克服共价键的是____。
Ⅱ.现有甲、乙、丙、丁四种晶胞(如图所示),可推知:甲晶体中A与B的离子个数比为___;乙晶体的化学式为___;丙晶体的化学式为____;丁晶体的化学式为____。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,向一定体积 0.1mol/L 醋酸溶液中逐滴加入等浓度的 NaOH 溶液,溶液中pOH 与 pH 的变化关系如图所示,则正确的是( )
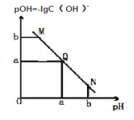
A. M 点所示溶液导电能力强于 Q 点
B. N 点所示溶液中 c(Na+)>c(CH3COO-)
C. Q 点所示的溶液 pH 一定等于 7
D. Q 点加入 NaOH 溶液的体积等于醋酸溶液的体积
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与人类文明进步息息相关,下列说法错误的是( )
A. 蚕丝的主要成分是蛋白质,属于天然高分子材料
B. 汉代烧制出“明如镜、声如磬”的瓷器,主要化学成分是硅酸盐
C. 2022年冬奥会聚氨酯速滑服,是无机非金属材料
D. 城市公交系统推广的清洁燃料压缩天然气“![]() ”、液化石油气“
”、液化石油气“![]() ”,主要成分都是烃
”,主要成分都是烃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上制汞的过程是:焙烧辰砂(主要含HgS),发生反应:HgS+O2![]() Hg+SO2,还原出的汞呈气态,冷凝得液态汞。其流程如图,下列说法不正确的是( )
Hg+SO2,还原出的汞呈气态,冷凝得液态汞。其流程如图,下列说法不正确的是( )

A. 含汞烟气可以采用活性炭吸附法处理达标后再排放
B. HgS+O2![]() Hg+SO2该反应中HgS只做还原剂
Hg+SO2该反应中HgS只做还原剂
C. 洗涤粗汞时不可用5%的硫酸代替5%的硝酸
D. 流程中加入氧化钙的目的是减少SO2的排放
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某工业废水中含有大量FeSO4,较多的Cu2+,极少量的Na+ 以及部分污泥,通过下列流程可从该废水中回收FeSO4·7H2O晶体及金属Cu。
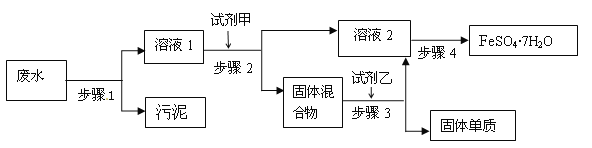
(1)步骤1的主要操作是___,需用到的玻璃仪器除烧杯外还有___。
(2)固体混合物是____(填化学式)
(3)步骤3中发生反应的化学方程式为___。
(4)步骤4中涉及的操作是:蒸发浓缩、___、过滤、洗涤、干燥。
(5)火法制得的粗铜中常混有少量氧化亚铜(Cu2O),氧化亚铜溶于稀硫酸溶液变蓝。试写出该反应的离子方程式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体积之比)后使用。请回答下列问题:
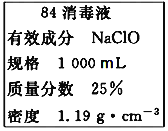
①该“84消毒液”的物质的量浓度约为___mol·L-1。(保留小数点后一位)
②某同学取100mL该“84消毒液”,稀释后用于消毒,稀释后的溶液中c(Na+)=___mol·L-1。
(2)从矿物学资料查得,二硫化亚铁和硫酸铜在一定条件下发生反应:14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4。
当有2.5molFeS2参加反应时,氧化产物的物质的量为__mol,转移的电子__mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列装置能达到实验目的的是( )
A. 实验室制取氨气
B. 测定化学反应速率
C. 验证非金属性:N﹥C﹥Si
D. 实现反应:Cu+2H2O![]() Cu(OH)2+H2
Cu(OH)2+H2![]()

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验现象与实验操作不相匹配的是
实验操作 | 实验现象 | |
A | 向盛有高锰酸钾酸性溶液的试管中通入足量的乙烯后静置 | 溶液的紫色逐渐褪去,静置后溶液分层 |
B | 将镁条点燃后迅速伸入集满CO2的集气瓶 | 集气瓶中产生浓烟并有黑色颗粒产生 |
C | 向盛有饱和硫代硫酸钠溶液的试管中滴加稀盐酸 | 有刺激性气味气体产生,溶液变浑浊 |
D | 向盛有FeCl3溶液的试管中加过量铁粉,充分振荡后加1滴KSCN溶液 | 黄色逐渐消失,加KSCN后溶液颜色不变 |
A. AB. BC. CD. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com