
【题目】化学科学需要借助化学专用语言来描述,现有下列化学用语:①Cl-的结构示意图:![]() ;②羟基的电子式:
;②羟基的电子式:![]() ;③HClO的结构式:H—Cl—O;④NaHCO3在水中的电离方程式:NaHCO3=Na++H++CO32-;⑤CO2的比例模型:
;③HClO的结构式:H—Cl—O;④NaHCO3在水中的电离方程式:NaHCO3=Na++H++CO32-;⑤CO2的比例模型:![]() ;⑥原子核内有10个中子的氧原子:188O。其中说法正确的是( )
;⑥原子核内有10个中子的氧原子:188O。其中说法正确的是( )
A.①④⑤⑥B.①②⑥C.①②③⑥D.②③⑤⑥
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案科目:高中化学 来源: 题型:
【题目】中成药连花清瘟胶囊在对抗新型冠状病毒中发挥了一定的作用,其有效成分绿原酸的结构简式如图,下列有关说法不正确的是( )

A.绿原酸属于芳香族化合物
B.分子中至少有 7个碳原子共面
C.1mol 绿原酸最多可消耗5 mol NaOH或4molBr2
D.与绿原酸苯环上取代基种类及个数均相同的有机物有5 种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有部分短周期元素的性质或原子结构如下:
元素 | 元素的性质或原子结构 |
X | 该元素的一种原子无中子 |
Y | 原子半径最大的短周期元素 |
Z | 第三周期元素中简单离子半径最小 |
M | 地壳中含量最多的元素 |
Q | 其氧化物是光导纤维的基本原料 |
W | 其核电荷数为M元素核电荷数的2倍 |
(1)X的无中子原子的符号为____________,Y的原子结构示意图为_____________,Q在元素周期表中的位置为___________________。
(2)Y、Z的最高价氧化物对应的水化物的碱性由强到弱的顺序是_______________________(用化学式表示),写出两者反应的离子方程式:__________________________________________。
(3)M、W两种元素中非金属性较强的是______________(用元素符号表示),下列表述中能证明这一事实的____________________(填序号),
a. 常温下,M的单质与W的单质的状态不同
b. 向W的氢化物中通入M2,有淡黄色固体析出
c. M、W形成的化合物中W元素为正价
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁、铝的混合物共0.2mol,溶于200mL4mol·L-1的盐酸溶液中,然后再滴加2 mol·L-1的NaOH 溶液。若在滴加NaOH溶液的过程中,沉淀质量m 随加入NaOH溶液的体积V变化情况如图所示。请回答下列问题:

(1)当V1=160mL时,则金属粉末中n(Al)=_____________mol。
(2)V2~V3段发生反应的离子方程式为_____________________________________________________。
(3))若镁、铝的混合物仍为0.2mol,其中镁粉的物质的量分数为a,改用200mL4 mol·L-1的硫酸溶解此混合物后,再加入840mL 2 mol·L-1的NaOH溶液,所得沉淀中无Al(OH)3,则a的取值范围为_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2020年春节前后,新型冠状病毒严重影响了人们的正常生活。次氯酸(![]() )具有强氧化性,可以杀灭新型冠状病毒,被广泛用于物体表面、织物等的消毒。
)具有强氧化性,可以杀灭新型冠状病毒,被广泛用于物体表面、织物等的消毒。
已知:①常温常压下,Cl2O为棕黄色气体,Cl2O和水作用可以生成次氯酸。
②将氯气(易溶于四氯化碳)和空气(不参与反应)按体积比1:3混合通入潮湿的Na2CO3中生成Cl2O气体,用水吸收Cl2O可制得次氯酸溶液,某学习小组利用以下装置制备次氯酸溶液,回答下列问题:
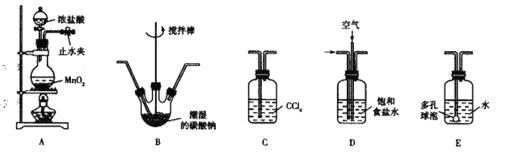
(1)各装置的连接顺序为A、_______________________.
(2)检验装置A气密性的方法是___________________________________________________________.
(3)装置A中发生反应的离子方程式为____________________________________________________.
(4)配平装置B中反应的化学方程式:___________Cl2+___________Na2CO3+_________H2O=___________Cl2O+______________NaCl+_____________NaHCO3._____________
(5)从环境保护角度考虑该装置存在一定的缺陷,改进方法是_____________________________.
(6)若装置A中MnO2的质量为43.5g,浓盐酸过量,完全反应后装置E中得到500mL0.8mol·L-1的次氯酸溶液,则整个过程中氯气的有效利用率为____________________%.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关分子结构如图所示,下列叙述中,正确的是 ( )
![]()
A. 除苯环外的其余碳原子有可能都在一条直线上
B. 所有的原子都在同一平面上
C. 12个碳原子不可能都在同一平面上
D. 12个碳原子有可能都在同一平面上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用反应6NO2+8NH3=7N2+12H2O构成电池的方法,既能实现有效消除氮氧化物的排放,减轻环境污染,又能充分利用化学能,装置如图所示。下列说法不正确的是
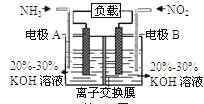
A.电流从右侧电极经过负载后流向左侧电极
B.A电极上发生氧化反应,B为正极
C.电极A极反应式为2NH3-6e-=N2+6H+
D.当有2.24LNO2(标准状况) 被处理时,转移电子为0.4mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种新型动力电池( LiFePO4电池)总反应式为Li1-xFePO4+LixC6![]() C6+LiFePO4,内部结构如图1所示,只有Li+通过聚合物隔膜。以此电池电解Na2SO4溶液(电极材料为石墨),可制得NaOH和H2SO4,其原理如图2所示。下列说法错误的是
C6+LiFePO4,内部结构如图1所示,只有Li+通过聚合物隔膜。以此电池电解Na2SO4溶液(电极材料为石墨),可制得NaOH和H2SO4,其原理如图2所示。下列说法错误的是

A. 电池放电时,LixC6在负极发生氧化反应
B. 电池放电时,正极反应式为 Lil-xFePO4+xLi-+xe-= LiFePO4
C. 电解时,图2的b电极反应式为2H2O-4e-=O2↑+4H+
D. 电解时,当转移0.2mol电子,A口产生气体的质量1.6g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com