
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A.1 mol·L-1AlCl3溶液中含有的Al3+数目小于NA
B.标准状况下,11 g 3H216O中含有的质子数目为6NA
C.1 mol Li2O和Na2O2的混合物中含有的离子总数大于3NA
D.常温常压下,4.6 g NO2所含的氮原子数目为0.1NA
 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:高中化学 来源: 题型:
【题目】下列事实与原因对应关系不正确的是
A | B | C | D | |
物质 |
Na2FeO4 |
海水稻 |
金属铜 |
碳酸钠 |
事实 | 用于自来水净水消毒 | 海水稻的秸杆可以燃烧发电 | Cu作原电池的电极 | 制革工业中原料皮的脱脂 |
主要原因 | Na2FeO4有强氧化性且能在水中产生胶体 | 稻子的秸杆中蕴含生物质能 | Cu能导电且质稳定 | Na2CO3稳定性强 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知元素的电负性和原子半径一样,也是元素的基本性质。下表给出14种元素的电负性:
元素 | AL | B | Be | C | Cl | F | Li | Mg | N | Na | O | P | S | Si |
电负性 | 1.5 | 2.0 | 1.5 | 2.5 | 3.0 | 4.0 | 1.0 | 1.2 | 3.0 | 0.9 | 3.5 | 2.1 | 2.5 | 1.8 |
试结合元素周期律相关知识完成下列问题。
(1)根据上表给出的数据,可推知元素的电负性具有的变化规律是__________ (从电负性与结构的关系考虑)。
(2)请预测Br与I元素电负性的大小关系:_________ 。
(3)经验规律告诉我们:当成键的两原子相应元素的电负性差值大于1.7时,一般为离子键,而小于1.7时,一般为共价键。试推断![]() 中化学键的类型是 ___________
中化学键的类型是 ___________
(4)预测元素周期表中电负性最小的元素是_____ (放射性元素除外)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知w g液态苯(C6H6)完全燃烧生成2 mol CO2气体和1 mol液态水,并放出m kJ的热量,下列能正确表示苯燃烧热的热化学方程式的是( )
A. 2C6H6(l)+15O2(g)===12CO2(g)+6H2O(l) ΔH=-2m kJ·mol-1
B. ![]() C6H6(l)+
C6H6(l)+![]() O2(g)===2CO2(g)+H2O(l) ΔH=-m kJ·mol-1
O2(g)===2CO2(g)+H2O(l) ΔH=-m kJ·mol-1
C. C6H6(l)+![]() O2(g)===6CO2(g)+3H2O(l) ΔH=-m kJ·mol-1
O2(g)===6CO2(g)+3H2O(l) ΔH=-m kJ·mol-1
D. C6H6(l)+![]() O2(g)===6CO2(g)+3H2O(l) ΔH=-3m kJ·mol-1
O2(g)===6CO2(g)+3H2O(l) ΔH=-3m kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知1 g氢气完全燃烧生成水蒸气时放出热量121 kJ,且氧气中1 mol O=O键完全断裂时吸收热量496 kJ,水蒸气中1mol H-O键形成时放出热量463 kJ,则氢气中1mol H-H键断裂时吸收热量为
A.920 kJB.557 kJC.436 kJD.188 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】K层有_____________个能级,用符号表示为_____________;L层有_____________个目自级,用符号表示为_____________;M层有_____________个能级,用符号表示为_____________。由此可推知第n(n为正整数)电子层最多可能有_____________个能级,当![]() 时,能量最低的两个能级的符号分别为_____________,它们的原子轨道形状分别为_____________、_____________。
时,能量最低的两个能级的符号分别为_____________,它们的原子轨道形状分别为_____________、_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为周期表中部分元素某种性质(X值)随原子序数变化的关系。
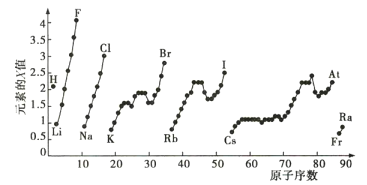
(1)短周期中原子核外p能级上电子数与s能级上电子总数相等的元素是___(填元素符号)。
(2)同主族内不同元素的X值变化的特点是___;同周期内,随着原子序数的增大,X值的变化总趋势是___。周期表中X值的这种变化特点体现了元素性质的___变化规律。
(3)X值较小的元素集中在元素周期表的___(填序号,下同)。
a.左下角 b.右上角 c.分界线附近
(4)下列说法正确的是___。
a.X值可反映元素最高正化合价的变化规律
b.X值可反映原子在分子中吸引电子的能力
c.X值的大小可用来衡量元素金属性和非金属性的强弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚维酮碘的水溶液是一种常见的碘伏类缓释消毒剂,聚维酮通过氢键与 HI3形成聚维酮碘,其结构表示如图,(图中虚线表示氢键)下列说法不正确的是
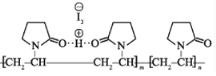
A.聚维酮碘是一种水溶性物质
B.聚维酮的单体是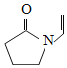
C.聚维酮分子由(m+n)个单体聚合而成
D.聚维酮在一定条件下能发生水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】非金属元素在化学中具有重要地位,请回答下列问题:
(1)氧元素的第一电离能比同周期的相邻元素要小,理由________。
(2)元素X与硒(Se)同周期,且该周期中X元素原子核外未成对电子数最多,则X为_____(填元素符号),其基态原子的电子排布式为_______。
(3)臭齅排放的臭气主要成分为3-MBT-甲基2丁烯硫醇,结构简式为(![]() )1mol 3-MBT中含有
)1mol 3-MBT中含有![]() 键数目为_______NA(NA为阿伏伽德罗常数的值)。该物质沸点低于(CH3)2C=CHCH2OH,主要原因是_______。
键数目为_______NA(NA为阿伏伽德罗常数的值)。该物质沸点低于(CH3)2C=CHCH2OH,主要原因是_______。
(4)PCl5是一种白色晶体,熔融时形成一种能导电的液体测得其中含有一种正四面体形阳离子和一种正八面体形阴离子;熔体中P-Cl的键长只有198pm和206pm两种,试用电离方程式解释PCl5熔体能导电的原因_________,正四面体形阳离子中键角大于PCl3的键角原因为__________,该晶体的晶胞如图所示,立方体的晶胞边长为a pm,NA为阿伏伽德罗常数的值,则该晶体的密度为_______g/cm 3
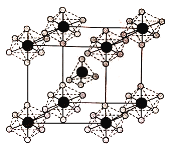
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com