
【题目】在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g) ![]() CO(g)+H2O(g),其化学平衡常数K与温度t的关系如下表:
CO(g)+H2O(g),其化学平衡常数K与温度t的关系如下表:
t℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
请回答下列问题:
(1)该反应的化学平衡常数表达式K= 。
(2)该反应为 反应(填“吸热”或“放热”)。
(3)830℃,在1L的固定容器的密闭容器中放入1 mol CO和5 mol H2O,反应达平衡后,其化学平衡常数K 1.0(填“大于”、“小于”或“等于”)
(4)830℃,容器中的反应达到平衡。在其他条件不变的情况下,扩大容器的体积,平衡 移动。(填“向正方向”、“向逆方向”或“不”)
(5)若1200℃时,在某时刻该容器中CO2、H2、CO、H2O的浓度分别为2 mol·L-1、2 mol·L-1、4 mol·L-1、4 mol·L-1,则此时上述反应的平衡移动方向为 (选填“正反应方向”、“逆反应方向”、“不移动”)。
【答案】(1)K=c(CO)·c(H2O)/c(CO2)·c(H2) ;(2)吸热 ;(3)等于;
(4)不;(5)逆反应方向。
【解析】
试题分析:(1)化学平衡常数是可逆反应达到平衡状态时各生成物浓度幂指数的乘积与各反应物浓度幂指数乘积的比。所以该反应的化学平衡常数K= K=c(CO)·c(H2O)/c(CO2)·c(H2) ;(2)根据化学平衡常数与温度的关系可知:升高温度,化学平衡常数增大,说明升高温度,化学平衡向正反应方向移动,正反应方向为吸热反应;(3)化学平衡常数只与温度有关, 加入的反应物的多少无关,由于温度为830℃,属于K=1.0;(4)830℃,容器中的反应达到平衡。在其他条件不变的情况下,扩大容器的体积,即减小压强,由于该反应是反应前后气体体积不变的反应,属于减小压强,化学平衡不发生移动;(5)若1200℃时,当加入上述物质的量浓度的物质时,Qc= c(CO)·c(H2O)/c(CO2)·c(H2)=(4×4)÷(2×2)=4>2.6,所以此时上述反应的平衡移动方向逆反应方向。


 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案科目:高中化学 来源: 题型:
【题目】已知A是一种气态烃,标况下的密度为1.25g/L,现以A为主要原料合成一种具有果香味的物质E,其合成路线如下图所示。
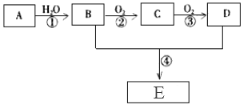
(1)写出A的结构简式 。
(2)B、D分子中所含官能团的名称分别是 、 。
(3)物质B可以直接氧化为D,需要加入的试剂是 。
(4)写出下列反应的化学方程式:
反应②的化学方程式: ;反应类型: 。
反应④的化学方程式: ;反应类型: 。
(5)B可由含淀粉的农产品如玉米、小麦、薯类等经发酵、蒸馏而得。请写出淀粉水解的化学方程式。
____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以硅藻土为载体的五氧化二钒(V2O5)是接触法生产硫酸的催化剂。从废钒催化剂中回收V2O5既避免污染环境又有利于资源综合利用。废钒催化剂的主要成分为:
物质 | V2O5 | V2O4 | K2SO4 | SiO2 | Fe2O3 | Al2O3 |
质量分数/% | 2.2~2.9 | 2.8~3.1 | 22~28 | 60~65 | 1~2 | <1 |
以下是一种废钒催化剂回收工艺路线:
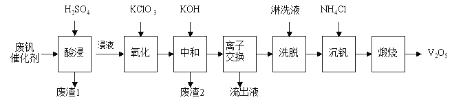
回答下列问题:
(1)“酸浸”时V2O5转化为VO2+,反应的离子方程式为___________,同时V2O4转成VO2+。“废渣1”的主要成分是__________________。
(2)“氧化”中欲使3 mol的VO2+变为VO2+,则需要氧化剂KClO3至少为____________mol。
(3)“中和”作用之一是使钒以V4O124-形式存在于溶液中。“废渣2”中含有_____________。
(4)“离子交换”和“洗脱”可简单表示为:4ROH+![]()
![]() R4V4O12+4OH(以ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈___________性(填“酸”“碱”“中”)。
R4V4O12+4OH(以ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈___________性(填“酸”“碱”“中”)。
(5)“流出液”中阳离子最多的是________。
(6)“沉钒”得到偏钒酸铵(NH4VO3)沉淀,写出“煅烧”中发生反应的化学方程式____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I、今有A.醋酸,B.盐酸,C.硫酸三种酸,请用三种酸的序号和“>”“<”或“=”填空。
(1)在同体积,同pH的三种酸中,分别加入足量的NaHCO3粉末,在相同条件下产生CO2的体积由大到小的顺序是 。
(2)物质的量浓度均为0.1 mol/L的三种酸溶液的pH由大到小的顺序是 ;如果取等体积的0.1 mol/L的三种酸溶液,用0.1 mol/L的NaOH中和,当恰好完全反应时,消耗NaOH溶液的体积由大到小的顺序是 。
II、用实验确定某酸HB的弱电解质。两同学的方案是:
甲:①称取一定质量的HB配制0.1mol/L的溶液100mL;
②用pH试纸测出该溶液的pH值,即可证明HB是弱电解质。
乙:①用已知物质的量浓度的HB溶液、盐酸,分别配制pH = 1的两种酸溶液各100mL;
②分别取这两种溶液各10mL,加水稀释为100mL;
③各取相同体积的两种稀释液装入两个试管,同时加入纯度相同的锌粒,观察现象,即可证明HB是弱电解质。
(1)甲方案中,说明HB是弱电解质的理由是测得溶液的pH 1(选填>、<、=)
(2)请你评价乙方案中难以实现之处和不妥之处: 。
III、硼酸(H3BO3)是生产其它硼化物的基本原料。已知H3BO3的电离常数为5.8×10-10,H2CO3的电离常数为K1=4.4×10-7、K2=4.7×10-11。向盛有饱和硼酸溶液的试管中,滴加0.1 mol/LNa2CO3溶液, (填“能”或“不能”)观察到气泡逸出。
已知H3BO3与足量NaOH溶液反应的离子方程式为H3BO3+OH-=B(OH)4-,写出硼酸在水溶液中的电离方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】日常生活中硫、氮氧化物的排放可能导致“酸雨”。下列活动会导致“酸雨”危害加剧的是( )
A.种草植树,建设“海绵”城市 B.推广使用电动车
C.普及燃煤供暖,减少石油依赖 D.开发太阳能照明
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.配制硫酸亚铁溶液时,常向溶液加入少量稀硝酸和少量铁粉
B.用25.00mL碱式滴定管量取20.00mL酸性高锰酸钾溶液
C.用pH试纸检验气体的酸碱性时,一定要先用蒸馏水湿润
D.可以用洒精萃取碘水中的碘单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右表为元素周期表的一部分。
碳 | 氮 | Y | |
X | 硫 | Z |
回答下列问题
(1)Z元素在周期表中的位置为__________。
(2)表中元素原子半径最大的是(填元素符号)__________。
(3)下列事实能说明Y元素的非金属性比S元素的非金属性强的是__________;
A.Y单质与H2S溶液反应,溶液变浑浊
B.在氧化还原反应中,1molY单质比1molS得电子多
C.Y和S两元素的简单氢化物受热分解,前者的分解温度高
(4)碳与镁形成的1mol化合物Q与水反应,生成2molMg(OH)2和1mol烃,该烃分子中碳氢质量比为9:1,Q与水反应的化学方程式为 。
(5)联氨(又称联肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料,联氨分子的电子式为①_____________,其中氮的化合价为②___________,实验室可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为③ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应aA(g)+bB(g)![]() cC(g)(△H<0)在等容条件下进行。改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如下图所示:
cC(g)(△H<0)在等容条件下进行。改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如下图所示:
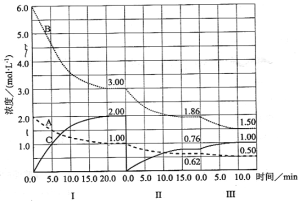
回答问题:
(1)反应的化学方程式中a∶b∶c为 ;
(2)由第一次平衡到第二次平衡,平衡移动的方向是_____,采取的措施是____________。
(3)比较第Ⅱ阶段反应温度(T2)和第Ⅲ阶段反应温度(T3)的高低;T2 T3(填“<”“>”“=”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com