
����Ŀ��ʵ�������ⶨ�����Ͻ����ɣ��������Ͻ��ܽ��ȡ����25.00mL�����벢�ⶨFe3+��Ũ�ȣ�ʵ�鷽��������£�

��֪�������ӷ�����ȼ�ա�
�ش��������⣺
��1�������£��������Ͻ��ܽ���Լ���_________(����ĸ)��
a��ϡ���� b��ϡ���� c��ϡ���� d��Ũ����
��2����֪��������ʵ������������������ˮ�����ͨ�����������������������ķ�����ȷ��c(Fe3+)ʱ���÷��������ϵ���Ҫȱ����________________________��
��3������X��___________________________������X�������Һ���Ƿ���Fe3+�����ķ�����_______________________________��
��4������װ����ͼ��ʾ��װ���д��ڵĴ�����___________________________��

��5������Fe3+����Һ������100mL��Ҫ��������___________________________��
��6����֪�ζ���ӦΪCe4++Fe2+=Ce3++Fe3+�����ζ��ﵽ�յ�ʱ������0.1000 mol��L-1Ce(SO4)2��Һ15.00 mL����ʼ������c(Fe3+)=_____________��������ϡ�����ữ��K2Cr2O7��Һ�ζ���Fe2+�Ĵ���Һ����ù��̵����ӷ�Ӧ����ʽΪ_____________________��
���𰸡� c ��������(Fe2O3��nH2O)û�й̶������ ��Һ ��ˮ��Һ��ȡ�����μ�����KSCN��Һ�Ժ�ɫ˵���в������������� ��ϵ�ܱ� 100mL����ƿ���ձ�������������ͷ�ι� 0.1600 mol��L-1 Cr2O72-+6Fe2++14H+=6Fe3++2Cr3++7H2O
����������1����ͼʾ���Ͻ���Һ����Һ�д��ڵ���Fe3+�����Լ����һ�����������ᣬѡ��a��bһ������������Ũ�����ж��ۻ�������ѡ��d�������ֻ��ʹ��ϡ���ᣬѡ��c��ȷ��
��2����֪��������ʵ������������������ˮ������Ը�ˮ������������������nֵ��ȷ��������ͨ�����������������������ķ�����ȷ��c(Fe3+)�Dz���������
��3�������Dz�����ˮ��Һ�壬���Բ���XӦ���Ƿ�Һ������Fe3+�ķ����ǵμ�KSCN��Һ���۲���Һ��ɫ�Ƿ��Ϊ��ɫ�����Դ�Ϊ����ˮ��Һ��ȡ�����μ�����KSCN��Һ�Ժ�ɫ˵���в���������������
��4��ͼʾ������װ������ȫ�ܱյ�װ�ã�ע�⣺����ţ�ǹܽ���ƿ���ý������ӵģ����������м����Ǻ�Σ�յġ�
��5������Fe3+����Һ������100mL��Ӧ�ý���Һת����100mL����ƿ��ϴ���ձ�����ˮ������������Ҫ������Ϊ��100mL����ƿ���ձ�������������ͷ�ιܡ�
��6��Ce(SO4)2Ϊ15��0.1��1000=0.0015mol�����ݷ�Ӧ�õ�Fe2+Ϊ0.0015mol������Ϊ100mL��ȡ��25mL���еζ������Ը�100mL��Һ����Fe2+Ϊ0.0015��4=0.006mol������Һ�е�Fe2+���������·�Ӧ��Fe + 2Fe3+ = 3Fe2+������ԭ����Fe3=Ϊ0.004mol����ЩFe3+������25mLˮ��������Ũ��Ϊ1000��0.004��25=0.16mol/L��������ϡ�����ữ��K2Cr2O7��Һ�ζ���Fe2+�Ĵ���Һ��Cr2O72-Ӧ�ñ���ԭΪCr3+����ù��̵����ӷ�Ӧ����ʽΪ��Cr2O72-+6Fe2++14H+=6Fe3++2Cr3++7H2O��


 ��ѧ�̸̳����¿α�ϵ�д�
��ѧ�̸̳����¿α�ϵ�д� Сѧ��ʱ��ѵϵ�д�
Сѧ��ʱ��ѵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ϡ�������ҹ������ս����Դ����֪ϡ��Ԫ����(Sm)��ԭ��������62��Sm��ij��ͬλ����������82������������( )
A.144B.82C.62D.20
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ɸ�������ɺ����ʽ��з��ࡣ
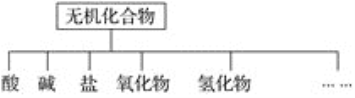
��1����ͼ��ʾ�����ʷ����������________��
��2����Na��K��H��O��C��S��N�������ֻ�����Ԫ����ɺ��ʵ����ʣ��ֱ������±�����
___________��______________��_______________
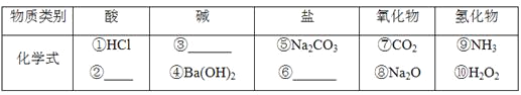
��3��д����ת��Ϊ�ݵĻ�ѧ����ʽ��__________________________________________��
��4��ʵ�����Ʊ��߳���________��________��Ӧ�����������ķ�����_______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������̼�����ָ���ƻ�����������Դ���ġ���Լ��Դ�����ٶ�����̼�ŷŵĽ������ʽ�����в����ϡ���̼����������ǣ�������
A.����������أ�̨�ݸ�������
B.̫������ˮ������ȼ����ˮ��
C.�ž�ʹ��һ��ȼ��
D.����������һ�������ϴ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������(C8H18)�����͵���Ҫ�ɷ�,����O2��Ӧ�������仯��ͼ��ʾ�������ж���ȷ����
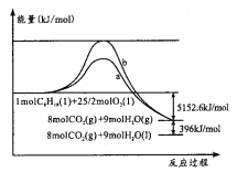
A. ����b�����������ʱ�������仯
B. ��Ӧ���������С���������������
C. ��ʾ����ȼ���ȵ��Ȼ�ѧ����ʽ:C8H18(l)+25/2O2(g)=8CO2(g)+9H2O(g) ��H=-5152.6kJ/mol
D. ��Ӧa��b�Ļ�ܲ�ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶���,����������г���amolH2��amolI2������������ӦH2(g)+I2(g)![]() 2HI(g).�������жϸ÷�Ӧ�ﵽƽ��״̬����
2HI(g).�������жϸ÷�Ӧ�ﵽƽ��״̬����
A. ��������ƽ�������������ٷ����ı�
B. ÿ����1molH-H����ͬʱ������2molI-H��
C. �����л���������ɫ����
D. H2��I2������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Դ�ɷ�Ϊһ����Դ�Ͷ�����Դ,��Ȼ�������ֳ���ʽ�ṩ����Դ��Ϊһ����Դ,������������Դ�����������ȡ����Դ��Ϊ������Դ���ݴ��ж�,����������ȷ����
A. ��Ȼ���Ƕ�����Դ B. ʯ���Ƕ�����Դ
C. ������һ����Դ D. ˮ����һ����Դ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶���,1L�����ܱ������з�����Ӧ:2A(g)+B(g)![]() C(g) ��H��������������,�ı���ʼA��B��Ͷ�ϱȵõ���ͼ��ʾ��ϵ������˵���������
C(g) ��H��������������,�ı���ʼA��B��Ͷ�ϱȵõ���ͼ��ʾ��ϵ������˵���������
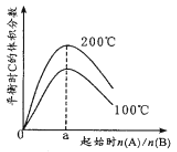
A. n(A)/n(B)=2ʱ��A��B��ת������� B. ��H<0
C. a=2 D. ��ͬ�¶��£�ƽ�ⳣ������ʼͶ�ϱ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ��д��ȷ����
A. Fe-Cu-CuSO4��Һ��ɵ�ԭ����и�����ӦʽΪ��Fe ��3e��= Fe3+
B. �����������Һ��ͨ������SO2���壺ClO����SO2��H2O �� HClO��HSO
C. ��FeCl3��Һ�м�������С�մ���Һ��Fe3+��3HCO3�� �� Fe(OH)3����3CO2��
D. ���AgNO3��Һ���ܷ�Ӧʽ��4Ag+ + OH�� �� 4Ag+O2+2H2O
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com