
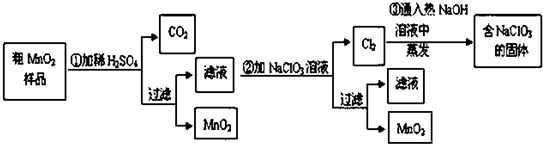
| 2.84g |
| 71g/mol |


 ���б�ˢ��ϵ�д�
���б�ˢ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��0.1 mol?L-1NaAlO2��Һ��Al3+��Na+��Cl-��NO3- |
| B���������������H2����Һ�У�NH4+��K+��SO42-��NO3- |
| C�����д���ClO-����Һ�У�K+��Na+��NO3-��SO42- |
| D��0.1mol/LFeCl3��Һ�У�Na+��NH4+��SCN-��SO42- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���٢ڢۢܢ� |
| B���ܢۢ٢ڢ� |
| C���ۢܢ٢ڢ� |
| D���ݢ٢ۢܢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Mg��Ħ������Ϊ24g |
| B�����ʵ����ĵ�λ��Ħ�� |
| C��1 mol O2���κ������µ������Ϊ22.4L |
| D����1 mol NaCl������뵽1Lˮ�У��õ�NaCl��Һ��Ũ�Ⱦ���1 mol?L-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ѡ�� | �� | �� | �� | ʵ����� | 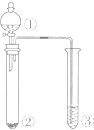 |
| A | Ũ���� | KMnO4 | AgNO3 | ˵������������������Ӧ������ɫ���� | |
| B | Ũ���� | ���� | ��ˮ | Ũ���������ˮ�ԡ������� | |
| C | ϡ���� | Na2SO3 | Ba��NO3��2��Һ | SO2������Ա��ξ��������ɰ�ɫ���� | |
| D | Ũ���� | Na2CO3 | Na2SiO3��Һ | ���ԣ����̼����� |
| A��A | B��B | C��C | D��D |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com