
【题目】汽车尾气的治理是减轻空气污染的有效途径。科学家研究发现TiO2的混凝土或沥青可以适度消除汽车尾气中的氮氧化物,其原理如下。下列关于“消除”过程的叙述错误的是

A. 部分光能转变为化学能
B. 消除总反应为:4NOx+(5-2x)O2+2H2O![]() 4HNO3
4HNO3
C. 使用纳米TiO2,产生的光生电子和空穴更多,NOx消除效率更高
D. 1 mol![]() 比1 mol羟基(·OH)多9NA个电子(NA为阿伏伽德罗常数)
比1 mol羟基(·OH)多9NA个电子(NA为阿伏伽德罗常数)
 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案科目:高中化学 来源: 题型:
【题目】下列溶液中,溶质的物质的量浓度为1molL-1 的是( )
A.将40gNaOH溶于1 L 水所得的溶液
B.往100mL2molL-1的NaNO3溶液中加入100 mL水所得的溶液
C.将16g CuSO4·5H2O溶于水配成100mL的溶液
D.含K+为2 molL-1的K2SO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是

选项 | ①中物质 | ②中物质 | 预测②中的现象 |
A. | 稀盐酸 | 碳酸钠与氢氧化钠的混合溶液 | 立即产生气泡 |
B. | 浓硝酸 | 用砂纸打磨过的铝条 | 产生红棕色气体 |
C. | 氯化铝溶液 | 浓氢氧化钠溶液 | 产生大量白色沉淀 |
D. | 草酸溶液 | 高锰酸钾酸性溶液 | 溶液逐渐褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黄铜矿不仅可用于火法炼铜,也可用于湿法炼铜,湿法可同时生产铜、磁性氧化铁和用于橡胶工业的一种固体物质A,流程如图:

(1)写出反应I的离子方程式________________________。
(2)工业生产中的过滤操作多采用倾析法分离出固体物质,下列适合用倾析法的有__________。
A.沉淀的颗粒较大 B.沉淀容易沉降 C.沉淀呈胶状 D.沉淀呈絮状
(3)在反应Ⅱ中,计算NaHCO3饱和溶液(其中CO32-平衡浓度为1.2×10-3 mol·L-1)可产生FeCO3沉淀时的最小Fe2+浓度是_________。(已知FeCO3的Ksp=3.0×10-11)
(4)反应Ⅲ是在设备底部鼓入空气,高温氧化锻烧法来制备磁性氧化铁,写出对应的化学方程式________________________________________。
(5)固体物质A的成分是_________(写名称),溶液B中所含溶质是__________(写化学式)。
(6)潮湿的FeCO3固体若不及时灼烧处理会在空气中逐渐变红褐色的Fe(OH)3固体,写出相关的化学方程式:_____________________________________________。
(7)本流程中可实现循环使用的物质除了水外,还有____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知Ca3(PO4)2与SiO2、C高温共热可以反应得到CaSiO3、P4蒸气和CO.反应如下:Ca3(PO4)2+SiO2+C![]() CaSiO3+P4↑+CO↑
CaSiO3+P4↑+CO↑
(1)配平该反应方程式,并标出电子转移方向和数目____________.
_____Ca3(PO4)2+_____SiO2+_____C![]() _____CaSiO3+_____P4↑+_____CO↑
_____CaSiO3+_____P4↑+_____CO↑
(2)该反应中被还原的元素是_____,氧化产物是_____.
(3)每消耗24.0g碳时,有_____个电子发生转移,生成P4_____g.
(4)反应所得混合气体,折算成标况下,其气体密度为_____g/L(保留两位小数).与该反应中涉及到的磷元素相同主族的氮元素,是造成水体富营养化的主要原因.若某污水中NH4Cl含量为180mg/L.
(5)写出NH4Cl的电子式_____.
(6)为除去废水中的NH4+,向103L该污水中加入0.1mol/LNaOH溶液,发生如下反应:NH4++OH﹣→NH3+H2O.则理论上需要NaOH溶液的体积为_____L(计算结果保留两位小数)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知溶液中存在平衡:Ca(OH)2(s)![]() Ca2+(aq)+2OH-(aq) △H<0,下列有关该平衡体系的说法正确的是( )
Ca2+(aq)+2OH-(aq) △H<0,下列有关该平衡体系的说法正确的是( )
①升高温度,平衡逆向移动
②向溶液中加入少量碳酸钠粉末能增大钙离子浓度
③恒温下向溶液中加入CaO,溶液的pH升高
④加热溶液,溶液的pH升高
⑤向溶液中加人Na2CO3溶液,其中固体质量增加
⑥向溶液中加入少量NaOH固体,Ca(OH)2固体质量不变
A. 仅①⑤ B. 仅①⑤⑥ C. 仅②③⑤ D. 仅①②⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
硼元素对植物生长及人体健康有着十分重要的作用,硼的化合物被广泛应用于新材料制备、生活生产等诸多领域。
(1)下列硼原子电子排布图表示的状态中,能量最低和最高的分别为________、________(填标号)
A.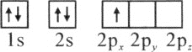
B.
C.
D.
(2)晶体硼单质能自发呈现出正二十面体的多面体外形,这种性质称为晶体的________。
(3)硼元素的简单氢化物BH3不能游离存在,常倾向于形成较稳定的B2H6或与其他分子结合。
①B2H6分子结构如图,则B原子的杂化方式为________。

②氨硼烷(NH3BH3)被认为是最具潜力的新型储氢材料之一,分子中存在配位键,提供孤电子对的成键原子是________,写出一种与氨硼烷互为等电子体的分子________(填化学式)。
(4)以硼酸(H3BO3)为原料可制得硼氢化钠(NaBH4),它是有机合成中的重要还原剂。
①H3BO3晶体中单元结构如图Ⅰ所示。各单元中的氧原子通过________氢键(用“A—B…C”表示,A、B、C表示原子)连结成层状结构,其片层结构如图Ⅱ所示,层与层之间以________(填作用力名称)相结合构成整个硼酸晶体。

②硼氢化钠中![]() 的键角大小是________,立体构型为________。
的键角大小是________,立体构型为________。
③根据上述结构判断下列说法正确的是________
a.H3BO3分子的稳定性与氢键有关
b.硼酸晶体有滑腻感,可作润滑剂
c.H3BO3分子中硼原子最外层为8e-稳定结构
d.含1mol H3BO3的晶体中有3 mol氢键
(5)磷化硼(BP)是受高度关注的耐磨材料,可作为金属表面的保护层,其结构与金刚石类似,晶胞结构如图所示。磷化硼晶胞沿z轴在平面的投影图中,B原子构成的几何形状是________;已知晶胞边长为a pm,则磷化硼晶体的密度是________g·cm-3(列出含a、NA的计算式即可)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在图(Ⅰ)所示的装置中,烧杯中盛放的是Ba(OH)2溶液,当从滴定管中逐渐加入某种溶液A时,溶液的导电性的变化趋势如图(Ⅱ)所示。

(1)滴加液体至图(Ⅱ)中曲线最低点时,灯泡可能熄灭,溶液A中含有的溶质可能是(填序号)__________。
①HCl ②H2SO4 ③NaHSO4 ④NaHCO3
(2)已知0.1 mol·L-1NaHSO4溶液中c(H+)=0.1 mol·L-1,请回答下列问题:
①写出NaHSO4在水溶液中的电离方程式_______________________________。
②NaHSO4属于________(填“酸”、“碱”或“盐”)。
③向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至中性,请写出发生反应的离子方程式:_______;在以上中性溶液中,继续滴加Ba(OH)2溶液_______,
(3)用一种试剂除去下列各物质中的杂质(括号内的物质),写出所用的试剂及反应的离子方程式。
Ⅰ.CaCl2(HCl):试剂______(,离子方程式___________;
Ⅱ.O2(CO2):试剂______,离子方程式____________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】衣康酸二甲酯常用于润滑油增稠剂、共聚物乳胶、改性醇酸树脂等。由3-甲基-3-丁烯酸合成衣康酸二甲酯的路线如下所示:

回答下列问题:
(1)B中的含氧官能团的名称是______________________,康酸的分子式为___________。
(2)反应①、⑤的反应类型分别是__________、____________,反应④所需的反应条件为___________。
(3)反应⑤的化学方程式为_________________________________。
(4)衣康酸的同分异构体中,含有碳碳双键,与NaHCO3溶液产生气体,且能发生银镜反应和水解反应的有__种。
(5)![]() 和苯甲醇可合成
和苯甲醇可合成 将以下合成路线补充完整(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂条件) ______________。
将以下合成路线补充完整(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂条件) ______________。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com