
【题目】(1)铁是人体必需的微量元素,目前市售补铁营养品较多,某研究性学习小组对补铁剂中铁的含量进行了测定。提供药品:FeCl2溶液(浅绿色)、FeCl3溶液(黄色)、铁粉、铜粉、KSCN溶液、氯水;仪器自选。
①将补铁剂中的Fe2+转化成Fe3+,结合你所选的试剂写出相关的离子方程式:______。
②若将Fe3+转化成Fe2+,结合你所选的试剂写出相关的离子方程式:__________。
(2)“服用维生素C,可使食物中的三价铁离子还原成二价铁离子”这句话指出维生素C在这一反应中做____剂,具有____性。
(3)某同学根据铁元素价态特点,提出这样一个观点:氯气与铁粉反应,当Cl2足量时生成FeCl3,当铁粉足量时产物是FeCl2,为验证该观点是否正确,该同学将一定质量铁粉与Cl2恰好完全反应得到一固体物质,然后通过实验确定其成分。探究过程如下:
①提出假设:
假设1:该固体物质是FeCl2。
假设2:该固体物质是_______。
②设计实验方案:
取少量固体物质于烧杯中,加适量水溶解,得到溶液A,然后取两份A溶液分别进行实验,实验现象与结论如下表:
实验方法 | 实验现象 | 结论 |
在A溶液中加KSCN溶液 | _______ | 固体物质中有FeCl3 |
在酸性高锰酸钾溶液中加少量A溶液 | 酸性高锰酸钾溶液颜色无明显变化 | _______ |
③根据上述实验结论,写出Cl2与铁粉加热时发生反应的化学方程式__________。
【答案】2Fe2++Cl2=2Fe3++2Cl- 2Fe3++Fe=3Fe2+或2Fe3++Cu=2Fe2++Cu2+ 还原 还原 FeCl3 溶液呈红色 固体物质中不含FeCl2 2Fe+3Cl2![]() 2FeCl3
2FeCl3
【解析】
(1)①氯水中的氯气可将亚铁离子氧化为铁离子,离子反应为:2Fe2++Cl2=2Fe3++2Cl-,故答案为:2Fe2++Cl2=2Fe3++2Cl-;
②若将Fe3+转化成Fe2+,可加入铁粉,反应的离子方程式为:2Fe3++Fe=3Fe2+,若加入铜粉,反应离子方程式:2Fe3++Cu=2Fe2++Cu2+,故答案为:2Fe3++Fe=3Fe2+或2Fe3++Cu=2Fe2++Cu2+;
(2)“服用维生素C,可使食物中的三价铁离子还原成二价铁离子”这句话指出维生素C在这一反应中做还原剂,具有还原性,故答案为:还原;还原;
(3)①由题给信息可知,产物可能为FeCl2或FeCl3,故答案为:FeCl3;
②铁离子和硫氰根离子反应生成血红色硫氰化铁,分别向A、B溶液中加KSCN溶液,溶液中含有氯化铁,铁离子和硫氰化钾反应反应而使溶液呈血红色,亚铁离子具有还原性,能被酸性高锰酸钾溶液氧化,如果向分别向KMnO4溶液中加入适量A、B溶液,KMnO4溶液颜色无明显变化,说明不含氯化亚铁,反应的方程式为2Fe+3Cl2![]() 2FeCl3。
2FeCl3。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】海水中溴元素以Br-形式存在,工业上用空气吹出法从海水中提取溴的工艺流程如图(见下页):
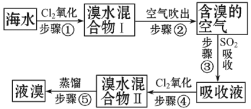
(1)步骤①反应的离子方程式是___。
(2)步骤③反应的化学方程式是___,从理论上考虑,下列也能吸收Br2的是___。
A.NaOH B.FeCl2 C.Na2SO3 D.H2O
(3)步骤⑤蒸馏的过程中,温度应控制在80℃~90℃。温度过高或过低都不利于生产,请解释原因:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以铁、硫酸、柠檬酸、双氧水、氨水等为原料可制备柠檬酸铁铵((NH4)3Fe(C6H5O7)2)。
(1)Fe基态核外电子排布式为___________;![]() 中与Fe2+配位的原子是________(填元素符号)。
中与Fe2+配位的原子是________(填元素符号)。
(2)NH3分子中氮原子的轨道杂化类型是____________;C、N、O元素的第一电离能由大到小的顺序为_______________。
(3)与NH![]() 互为等电子体的一种分子为_______________(填化学式)。
互为等电子体的一种分子为_______________(填化学式)。
(4)柠檬酸的结构简式见图。1 mol柠檬酸分子中碳原子与氧原子形成的σ键的数目为_________mol。
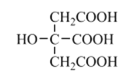
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某100mL溶液可能含有 Na+、NH4+、Fe3+、CO32-、SO42-、Cl-中的若干种,取该溶液进行连续实验,实验过程如图:(所加试剂均过量,气体全部逸出)下列说法正确的是

A. 若原溶液中不存在 Na+,则 c(Cl-)<0.1molL﹣1
B. 原溶液可能存在 Cl- 和 Na+
C. 原溶液中 c(CO32-)是 0.01molL﹣1
D. 原溶液一定存在 CO32-和SO42-,一定不存在 Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近,中国科学院大连化物所“CO2催化转化为CO的研究”获得新进展。如图是使用不同催化剂(NiPc和CoPc)时转化过程中的能量变化,下列说法不合理的是( )
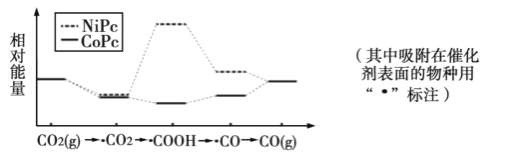
A.CO2经还原反应得到COOH
B.该研究成果将有利于缓解温室效应,并解决能源转化问题
C.相同基团的物种分别吸附在NiPc和CoPc表面,其能量可能不同
D.催化剂可以改变CO2转化为CO反应的焓变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、W的原子序数依次增大,Z原子2p轨道上有3个未成对电子,甲、乙、丙、丁、戊是这四种元素的两种或三种形成的化合物,75%的甲溶液常用于消毒,戊是Z和X组成的10电子分子,常温下己溶液显中性,它们有如下转化关系(反应条件已略去):
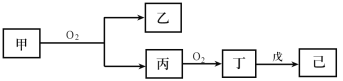
则下列说法中错误的是
A.四种元素原子半径由大到小的顺序为:Y>Z>W>X
B.可以用酸性KMnO4溶液鉴别甲和丙
C.己溶于水后促进了水的电离
D.W的氢化物不一定比Y的稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组设计了如图所示原电池装置(盐桥中吸附有饱和K2SO4溶液)。下列说法正确的是
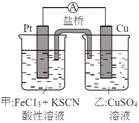
A.该原电池的正极反应是Cu2++2e-=Cu
B.甲烧杯中溶液的血红色逐渐变浅
C.盐桥中的SO42-流向甲烧杯
D.Cu电极质量减少,Pt电极质量增加
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有人设计出利用CH4和O2的反应,用铂电极在KOH溶液中构成原电池,电池的总反应类似于CH4在O2中燃烧,则下列说法正确的是( )
①每消耗1mol CH4,可以向外电路提供约![]()
![]() 的电量;
的电量;
②负极上CH4失去电子,电极反应式为: CH4-8e-+10OH—=CO32-+7H2O
③负极上是O2获得电子,电极反应式为![]() ;
;
④电池放电后,溶液pH不断升高
A.①②B.①③C.①④D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是实验室进行氨溶于水的“喷泉实验”的装置,下列叙述不正确的是( )

A.该实验说明氨气是一种极易溶于水的气体
B.进入烧瓶中的液体颜色由无色变为红色,说明氨水有碱性
C.氨水很稳定,将烧瓶中的红色溶液加热,颜色不会发生变化
D.形成“喷泉”的主要原因是氨气溶于水后,烧瓶内的气压小于大气压
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com