
【题目】下列反应属于离子反应的是
A.H2和O2反应生成水B.锌片投入稀硫酸中
C.双氧水(H2O2)分解制取O2D.高炉炼铁
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】可以由下列反应合成三聚氰胺:CaO+3C![]() CaC2+CO↑,CaC2+N2
CaC2+CO↑,CaC2+N2![]() CaCN2+C,CaCN2+2H2O = NH2CN+Ca(OH)2,NH2CN与水反应生成尿素[CO(NH2)2],尿素合成三聚氰胺。
CaCN2+C,CaCN2+2H2O = NH2CN+Ca(OH)2,NH2CN与水反应生成尿素[CO(NH2)2],尿素合成三聚氰胺。
(1)写出与Ca在同一周期且最外层电子数相同、内层排满电子的基态原子的电子排布式:______ ;CaCN2中阴离子为CN22-,与CN22-互为等电子体的分子有N2O和________(填化学式),由此可以推知CN22—的空间构型为________。
(2)三聚氰胺(![]() )俗称“蛋白精”。动物摄入三聚氰胺和三聚氰酸 (
)俗称“蛋白精”。动物摄入三聚氰胺和三聚氰酸 (![]() )后,三聚氰酸与三聚氰胺分子相互之间通过________结合,在肾脏内易形成结石。
)后,三聚氰酸与三聚氰胺分子相互之间通过________结合,在肾脏内易形成结石。
(3)CaO晶胞如图所示,CaO晶体中Ca2+的配位数为________ ,Ca2+采取的堆积方式为_______,O2-处于Ca2+堆积形成的空隙中;CaO晶体和NaCl晶体的晶格能分别为:CaO 3401 kJ·mol-1、NaCl 786 kJ·mol-1。导致两者晶格能差异的主要原因是__________。

(4)配位化合物K3[Fe(CN)n]遇亚铁离子会产生蓝色沉淀,因此可用于检验亚铁离子,已知铁原子的最外层电子数和配体提供电子数之和为14,求n= ______ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某固体试样A是由一定量的Al、Mg均匀组成的混合物,为验证混合物的组成,进行如下实验:
①取m g试样A,全部溶于0.5L 2mol·L-1稀硫酸溶液中,放出11.2 L气体(已换算成标准状况),同时生成溶液B;
②另取m g试样A,加入2mol·L-1的NaOH溶液,当加到100mL时,气体不再生成;
③往溶液B中加入2mol/L NaOH,至沉淀不再发生变化。
根据以上过程回答下列问题:
(1)溶液B中是否含有H+_____________(填“是”或“否”);
(2)写出②中发生反应的离子方程式____________________________________;
(3)下列能表示过程③产生的沉淀质量W与加入NaOH溶液体积V的关系是_____;
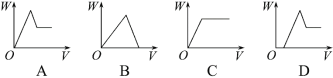
(4)m g试样A中含Mg的质量为________g;
(5)林同学通过查阅资料,发现浓硫酸与铝发生钝化,但与Mg能剧烈反应生成SO2,如果忽略钝化的反应过程,可以通过测定浓硫酸与固体试样反应产生的气体体积,来确定混合物A中镁的质量分数。
郭同学认为林同学的方案可行,但考虑到如果反应结束后硫酸未保持“浓”的状态,测定结果会____________(填“偏大”、“偏小”或“不变”),其依据是_______________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KMnO4 是一种氧化剂,实验室常用 KMnO4和浓盐酸反应制备 Cl2。下图是制备 NaClO溶液的装置图。
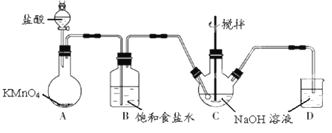
完成下列填空:
(1)KMnO4 稀溶液是一种常见消毒剂,其消毒机理与以下物质相似的是______(选填编号)。
a.75%酒精 b.双氧水 c.NaClO 溶液 d.硫磺皂
(2)B装置中饱和食盐水的作用是___________,D装置中NaOH的作用______________。
(3)实验操作过程中可调节__________以控制A 装置中产生 Cl2 的气流,C装置需控制反应温度在 0~5℃,实验中可将C 装置放入________________中。
II.测定 KMnO4纯度可用标准 Na2S2O3进行标定
(4)配制250 mL 0.1000 mol/L标准 Na2S2O3溶液,需准确称取Na2S2O3固体的质量为____g(精确到0.001)。
(5)取某 KMnO4 0.600g,酸化后用 0.1000 mol/L 标准 Na2S2O3溶液进行滴定,滴定至终点消耗 Na2S2O3溶液 20.00 mL,则该 KMnO4 产品的纯度是_________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式的书写中正确的是
A.氢氧化铁与盐酸反应:H++OH-=H2O
B.铁与盐酸反应:2Fe+6H+=2Fe3++3H2↑
C.氧化铜溶于稀硫酸:CuO+2H+=Cu2++H2O
D.向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O=Fe(OH)3↓+3H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式错误的是
A.铁与稀盐酸反应:2Fe+6H+=2Fe3++3H2↑
B.澄清石灰水与盐酸反应:OH-+H+=H2O
C.锌与氯化铜溶液反应:Zn+Cu2+=Zn2++Cu
D.硝酸钡溶液与稀硫酸反应:Ba2++SO42-=BaSO4↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在1L氯化铁和氯化铝的混合液中,Fe3+的物质的量浓度为0.4mol/L,Cl-的物质的量浓度为1.8 mol/L。要使Fe3+全部转化为沉淀分离出来,至少需要加入 4 mol/L NaOH溶液的体积为( )
A. 450mL B. 500mL C. 300mL D. 200mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值.下列说法正确的是( )
A. 高温下,0.2 mol Fe与足量水蒸气反应,生成的H2分子数目为0.3NA
B. 室温下,1 L pH=13的NaOH溶液中,由水电离的OH﹣离子数目为0.1NA
C. 氢氧燃料电池正极消耗22.4 L(标准状况)气体时,电路中通过的电子数目为2NA
D. 5NH4NO3![]() 2HNO3+4N2↑+9H2O反应中,生成28 g N2时,转移的电子数目为3.75NA
2HNO3+4N2↑+9H2O反应中,生成28 g N2时,转移的电子数目为3.75NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关胶体和溶液说法正确的是( )
A.氯化铁溶液能产生丁达尔现象
B.不同胶体溶液带不同的电荷
C.胶体具有丁达尔效应
D.某微粒大小介于10—12~10—9 cm之间,所以它是胶体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com