
【题目】氯乙烷跟相关有机化合物之间的转化如下图所示:
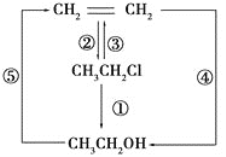
(1)写出各反应的化学方程式
①__________________________________________________,
②__________________________________________________,
③__________________________________________________,
④_________________________________________________,
⑤_______________________________________________。
(2)根据上述方程式回答下列问题:
A.上述化学反应的反应类型有____________________________。
B.证明CH3CH2Cl属于卤代烃的操作方法是___________________。
【答案】CH3CH2Cl+NaOH![]() CH3CH2OH+NaCl CH2=CH2+HCl
CH3CH2OH+NaCl CH2=CH2+HCl![]() CH3CH2Cl CH3CH2Cl+NaOH
CH3CH2Cl CH3CH2Cl+NaOH![]() CH2=CH2↑+NaCl+H2O CH2=CH2+H2O
CH2=CH2↑+NaCl+H2O CH2=CH2+H2O![]() CH3CH2OH CH3CH2OH
CH3CH2OH CH3CH2OH![]() CH2=CH2↑+H2O 取代反应、加成反应、消去反应 取少量样品于一试管中,再加适量的氢氧化钠的溶液并加热,待反应完全后向试管中加稀硝酸至溶液呈酸性后滴加AgNO3溶液,若有白色沉淀生产则证明为氯代烃
CH2=CH2↑+H2O 取代反应、加成反应、消去反应 取少量样品于一试管中,再加适量的氢氧化钠的溶液并加热,待反应完全后向试管中加稀硝酸至溶液呈酸性后滴加AgNO3溶液,若有白色沉淀生产则证明为氯代烃
【解析】
(1)①CH3CH2Cl转化为CH3CH2OH,可在NaOH水溶液中共热发生水解反应实现,其化学方程式是:CH3CH2Cl+NaOH![]() CH3CH2OH+NaCl;
CH3CH2OH+NaCl;
②CH2=CH2转化为CH3CH2Cl,可在催化剂作用下与HCl加成实现,其化学方程式是:CH2=CH2+HCl![]() CH3CH2Cl;
CH3CH2Cl;
③CH3CH2Cl转化为CH2=CH2,可在NaOH醇溶液中共热发生消去反应实现,其化学方程式是:CH3CH2Cl+NaOH![]() CH2=CH2↑+NaCl+H2O;
CH2=CH2↑+NaCl+H2O;
④CH2=CH2转化为CH3CH2OH,可在催化剂、加热、加压作用下与水加成实现,其化学方程式是:CH2=CH2+H2O![]() CH3CH2OH;
CH3CH2OH;
⑤CH3CH2OH转化为CH2=CH2,可在浓硫酸催化下迅速加热至170℃,发生消去反应而得,其化学方程式是:CH3CH2OH![]() CH2=CH2↑+ H2O;
CH2=CH2↑+ H2O;
(2)①上述化学反应的反应类型依次是①是水解反应或取代反应、②④是加成反应、③⑤是消去反应;
②CH3CH2Cl分子中C—Cl共价键在水溶液中不能电离形成Cl-,所以不能在氯乙烷中直接加入AgNO3溶液检验卤元素,而是将氯乙烷分子中C—Cl共价键断裂形成Cl-,再将溶液调节到酸性后加入AgNO3溶液来检验卤元素存在,证明CH3CH2Cl属于卤代烃的操作方法是取少量样品于一试管中,再加适量的氢氧化钠的溶液并加热,待反应完全后向试管中加稀硝酸至溶液呈酸性后滴加AgNO3溶液,若有白色沉淀生产则证明为氯代烃。


科目:高中化学 来源: 题型:
【题目】实验小组同学探究FeSO4分解反应并检验反应产物(加热及加持装置略)。下列有关FeSO4分解的说法不正确的是( )
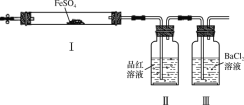
A.Ⅰ中固体变为红棕色,说明反应生成了Fe2O3
B.Ⅰ中反应需持续加热,说明FeSO4分解是吸热反应
C.Ⅱ中品红溶液颜色褪去,说明反应生成了SO2
D.Ⅲ中未产生白色沉淀,说明反应未生成SO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸和乙醇反应制取乙酸乙酯的装置如图所示:在试管里加入3mL乙醇,然后一边摇动,一边慢慢地加入2mL浓硫酸和2mL冰醋酸,用酒精灯小心均匀地加热10min,将产生的蒸气经长导管通入到小试管中溶液的液面上。回答下列问题:
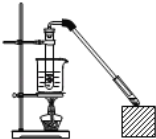
(1)乙酸的官能团是____(写名称)。制取乙酸乙酯的化学方程式为:___。
(2)①浓H2SO4的作用是____。
②小试管中的溶液是____,其作用是____(写出一种即可);
③长导管不插入液面以下的目的是____;
(4)实验中采取的加热方式称,这种加热方式的好处主要有____、___;
(5)反应生成的乙酸乙酯,其密度比水___(填“大”或“小”),有___气味。应从该分液漏斗的___(填编号,多填、少填均不得分)。
a.下部流出 b.上口倒出 c.都可以
(6)若实验室中温度过高,温度达170℃,副产物中主要有机产物是___(填名称)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴化钙是一种重要的化工原料,常见有![]() 和
和![]() 等结晶形式。某兴趣小组以废铁屑为原料制备
等结晶形式。某兴趣小组以废铁屑为原料制备![]() 的主要流程:
的主要流程:
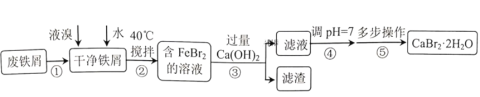
相关信息如下:
①![]() 吸湿性强。
吸湿性强。
②34℃时结晶得到![]() ,
,![]() 加热至210℃得到
加热至210℃得到![]() 。
。
请回答:
(1)步骤①的目的是去除废铁屑表面的油污,方法是________。
(2)实验室模拟海水提取溴的过程中,用苯萃取溶液中的溴,选出其正确操作并按顺序列出字母:涂凡士林→检漏→()→()→()→()→()→清洗干净。________
a.打开玻璃塞放气
b.打开旋塞放气
c.将溶液和苯转移至分液漏斗中,塞上玻璃塞
d.双手托住分液漏斗,右手压住玻璃塞,左手握住旋塞,上下颠倒振荡
e.右手压住玻璃塞,左手握住旋塞,将分液漏斗倒转振荡
f.置于铁架台铁圈上静置,打开玻璃塞,将旋塞拧开,放出下层液体
g.从下口放出溴的苯溶液
h.从上口倒出溴的苯溶液
(3)步骤④调pH=7,适宜加入的试剂是________,通过调节分液漏斗的活塞可以控制添加液体的速率。当溶液pH接近7时,滴加试剂的分液漏斗的活塞应如图中的________(填序号)所示。

(4)下列有关说法正确的是________。
A.步骤②反应控制在40℃左右,原因是防止反应过于剧烈并减少液溴挥发
B.步骤③滤渣成分只有![]() 、
、![]() 和
和![]()
C.为使![]() 快速结晶,可用冰水浴进行冷却
快速结晶,可用冰水浴进行冷却
D.步骤⑤包括蒸发浓缩、冷却结晶、过滤、洗涤、干燥等多步操作
(5)制得的![]() 可以通过如下步骤测定其纯度:①称取样品质量;②溶解;③滴入足量Na2CO3溶液,充分反应后过滤,洗涤,干燥;④称量。
可以通过如下步骤测定其纯度:①称取样品质量;②溶解;③滴入足量Na2CO3溶液,充分反应后过滤,洗涤,干燥;④称量。
若实验操作规范而测定结果偏低,其可能的原因是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,HF和CH3COOH的电离常数分别为3.5×10-4和1.7×10-5。将pH和体积均相同的NaF和CH3COONa溶液分别稀释,其pH随加水体积的变化如图所示。下列叙述正确的是
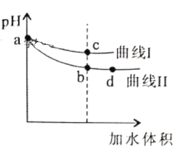
A.曲线I代表CH3COONa溶液
B.溶液中水的电离程度:c点>b点
C.从b点到d点,溶液中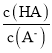 保持不变(其中HA、
保持不变(其中HA、![]() 分别代表相应的酸和酸根离子)
分别代表相应的酸和酸根离子)
D.相同体积a点的两溶液分别与HCl恰好反应后,溶液中![]() 相同
相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量混合气体在密封容器中发生如下反应:xA(g)+yB(g)![]() nC(g)。达到平衡后测得A气体的浓度为0.5mol/L;保持恒温下将密闭容器的容积扩大1倍,再达到平衡时,测得A的浓度为0.3 mol/L。则下列叙述正确的是
nC(g)。达到平衡后测得A气体的浓度为0.5mol/L;保持恒温下将密闭容器的容积扩大1倍,再达到平衡时,测得A的浓度为0.3 mol/L。则下列叙述正确的是
A.x+y<nB.该化学平衡向右移动
C.B的转化率增大D.A的物质的量增加
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:BF3和水反应生成氟硼酸(HBF4)和硼酸(H3BO3),一定条件下BF3与一定量水可形成![]() 晶体Q(
晶体Q(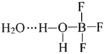 )。下列有关说法,正确的是
)。下列有关说法,正确的是
A.BF3和水反应生成氟硼酸和硼酸是氧化还原反应
B.BF3分子中,每个原子的最外层都具有8电子稳定结构
C.晶体Q中存在离子键、共价键、范德华力和氢键
D.H3BO3在水中只发生反应:![]() ,可知硼酸是一元酸
,可知硼酸是一元酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请用下列装置设计一个实验,证明Cl2的氧化性比I2的氧化性强。
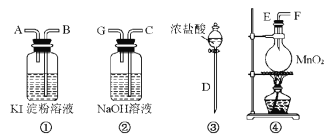
请回答下列问题:
(1)若气流从左到右,则上述仪器的连接顺序为D接E,______接_____,_____接____。
(2)圆底烧瓶中发生反应的化学方程式为____________。
(3)证明Cl2比I2的氧化性强的实验现象是_____________,反应的离子方程式是________。
(4)装置②的作用是___________。
(5)若要证明Cl2的氧化性比Br2强,则需做的改动是_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com