
【题目】NaCN超标的电镀废水可用两段氧化法处理:
(1)NaCN与NaClO反应,生成NaOCN和NaCl
(2)NaOCN与NaClO反应,生成Na2CO3、CO2、NaCl和N2
已知HCN(Ki=6.3×10-10)有剧毒;HCN、HOCN中N元素的化合价相同。
完成下列填空:
(1)第一次氧化时,溶液的pH应调节为____________(选填“酸性”、“碱性”或“中性”);原因是______________________。
(2)写出第二次氧化时发生反应的离子方程式。
_______________________________________
(3)处理100 m3含NaCN 10.3 mg/L的废水,实际至少需NaClO___g(实际用量应为理论值的4倍),才能使NaCN含量低于0.5 mg/L,达到排放标准。
(4)(CN)2与Cl2的化学性质相似。(CN)2与NaOH溶液反应生成_________、__________和H2O。
【答案】(1)碱性;防止生成HCN,造成人员中毒或污染空气。
(2)2OCN-+3ClO-=CO32-+CO2↑+3Cl-+N2↑
(3)14 900
(4)NaOCN、NaCN
【解析】
试题分析:(1)依据HCN的电离平衡常数可知HCN是极弱的酸,所以NaCN极易于酸反应生成HCN。为防止生成HCN,造成人员中毒或污染空气,因此第一次氧化时,溶液的pH应调节为碱性。
(2)NaOCN与NaClO反应,生成Na2CO3、CO2、NaCl和N2,首先确定反应物和生成物;再依据反应中氯元素的化合价从+1价降低到-1价,得到2个电子。N元素化合价从-3价升高到0价,失去3个电子,则根据电子得失守恒可知还原剂和氧化剂的物质的量之比是2:3,反应的离子方程式为2OCN-+3ClO-=CO32-+CO2↑+3Cl-+N2↑。
(3)NaCN被氧化的两个阶段氧化剂均为NaClO,所以可以合并一起进行计算,即反应物为NaCN和NaClO,生成物为:Na2CO3、CO2、NaCl和N2。参加反应的NaCN是![]() ,反应中C由+2价升高到+4价,N元素化合价从-3价升高到0价,即1molNaCN失去5mol电子,1mol次氯酸钠得到2mol电子,所以处理100m3含NaCN10.3mg/L的废水,实际至少需NaClO的质量为
,反应中C由+2价升高到+4价,N元素化合价从-3价升高到0价,即1molNaCN失去5mol电子,1mol次氯酸钠得到2mol电子,所以处理100m3含NaCN10.3mg/L的废水,实际至少需NaClO的质量为![]() g。
g。
(4)(CN)2与Cl2的化学性质相似,则根据氯气与氢氧化钠反应的方程式可知(CN)2与NaOH溶液反应生成NaOCN、NaCN和H2O。


科目:高中化学 来源: 题型:
【题目】具有水果香味的中性物质A可以发生下列变化:
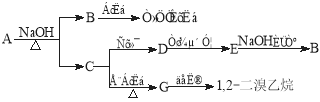
(1) 其中的弱酸是_____________________,G的结构简式为___________
(2) 写出下列变化的方程式:
A+NaOH→B+C的化学方程式:_____________________________________________
C→D的化学方程式:__________________________________________
D的银镜反应的离子方程式:_____________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高三一年的化学复习,学生要抓住两方面,一方面是教材,另一方面是历年的高考真题。每年的高考题,在教材中几乎都能找到影子,所以同学一定要紧紧抓住教材,根据《必修一》第三章和第四章的内容回答下列问题:
(1)实验3-1是取用钠单质的实验,用品有小刀, 、 、培养皿。
(2)金属铝及其化合物在日常的生产生活中,用途很广泛,氧化铝的用途 (举一例)。 氢氧化铝的用途 (举一例)。
(3)印刷铜箔电路板常用FeCl3溶液作为腐蚀液,写出反应的离子方程式 。
(4)漂白粉或漂粉精失效的原理为(请用化学方程式表示): 、 。
(5)石灰法是目前应用最广泛的工业废气脱硫法,过程如下:通过煅烧石灰石得到生石灰,以生石灰为脱硫剂,在吸收塔中与废气中的SO2反应而将硫固定,其产物可用作建筑材料。有关的反应化学方程式为:CaCO3![]() CaO + CO2 、 。
CaO + CO2 、 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】K2Cr2O7溶液中存在平衡:Cr2O72-(橙色)+H2O![]() 2CrO42-(黄色)+2H+。用K2Cr2O7溶液进行下列实验:
2CrO42-(黄色)+2H+。用K2Cr2O7溶液进行下列实验:
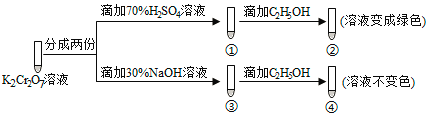
结合实验,下列说法不正确的是( )
A.①中溶液橙色加深,③中溶液变黄
B.②中Cr2O72-被C2H5OH还原
C.对比②和④可知K2Cr2O7酸性溶液氧化性强
D.若向④中加入70%H2SO4溶液至过量,溶液变为橙色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关表述正确的是( )
A.离子晶体一定含金属阳离子
B.非金属元素形成的单质一定是分子晶体
C.在共价化合物分子中各原子都形成8电子结构
D.共价键能存在于共价化合物中,也能存在于离子化合物中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2L的容器中放入4mol N2O5,发生如下反应:2N2O5(g)![]() 4NO2(g)+O2(g)。反应进行到5min时,测得N2O5转化了20%,
4NO2(g)+O2(g)。反应进行到5min时,测得N2O5转化了20%,
(1)5min时,剩余N2O5的物质的量;
(2)前5min,v(NO2)为多少;
(3)5min时,N2O5的物质的量占混合气体总物质的量的百分比(保留一位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I (1)某同学做如下实验,以检验反应中的能量变化。
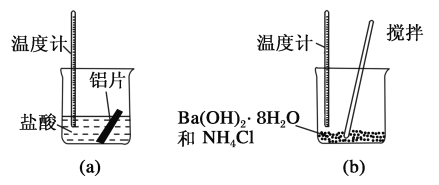
实验中发现反应后(a)中温度升高,由此可以判断(a)中反应是__________热反应;
(b)中温度降低, 根据能量守恒定律,(b)中反应物的总能量应该__________其生成物的总能量。
(2) 下列反应:①氢氧化钠与硫酸,②一氧化碳与氧气,
③八水合氢氧化钡与氯化铵,④金属铜与硝酸银。
其中(用序号填空): 能设计成原电池的反应是____________________。
II(1)有下列几种物质
A.金刚石和石墨 B.C2H6和C5H12 C. C2H4 和 C2H6
D.CH3CH2CH2CH3 和 CH3CH(CH3)2 E.35Cl和37Cl
属于同分异构体的是________;属于同素异形体的是________;
属于同系物的是________; 属于同位素的是________。
(2) 两种粒子的核外电子排布相同,核电荷数不同,则它们可能是________。
A.两种不同元素的原子 B.一定是两种不同的离子
C.同一元素的原子和离子 D.两种不同元素的原子和离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某高校曾以下列路线合成药物心舒宁(又名冠心宁),它是一种有机酸盐。
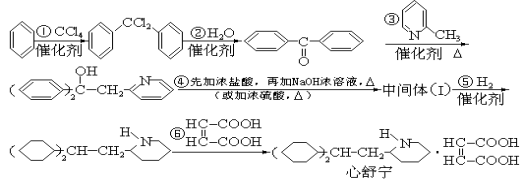
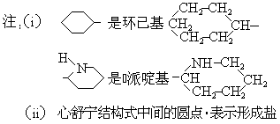
(1)心舒宁的分子式为 。
(2)中间体(Ⅰ)的结构简式是 。
(3)反应①~⑤中属于加成反应的是 (填反应代号).
(4)如果将⑤、⑥两步颠倒,则最后得到的是(写结构简式) .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com