
ЁОЬтФПЁПзюНќЕФбаОПЗЂЯжЃЌИДКЯбѕЛЏЮяЬњЫсУЬЃЈMnFe2O4ЃЉПЩвдгУгкШШЛЏбЇбЛЗЗжНтЫЎжЦЧтЃЌвђЖјЪмЕНаэЖрЗЂДяЙњМвЕФЧрэљЁЃMnFe2O4ЕФжЦБИСїГЬШчЯТЃК

(1)дСЯFe(NO3)nжаn=______ЃЌЭЖШыдСЯFe(NO3)nКЭMnЃЈNO3ЃЉ2ЕФЮяжЪЕФСПжЎБШгІЮЊ______ЁЃ
(2)ВНжшЖўжаЁАСЌајНСАшЁБЕФФПЕФЪЧ______ЃЛВНжшШ§жаЯДЕгИЩОЛЕФБъзМЪЧ______ЁЃ
(3)РћгУMnFe2O4ШШЛЏбЇбЛЗжЦЧтЕФЗДгІПЩБэЪОЮЊ:MnFe2O4![]() MnFe2O4Љx+
MnFe2O4Љx+![]() O2ЁќЁЂMnFe2O4Љx+xH2OЁњMnFe2O4+xH2ЁќЁЃЧыШЯецЗжЮіЩЯЪіСНИіЗДгІВЂЛиД№ЯТСаЮЪЬтЃК
O2ЁќЁЂMnFe2O4Љx+xH2OЁњMnFe2O4+xH2ЁќЁЃЧыШЯецЗжЮіЩЯЪіСНИіЗДгІВЂЛиД№ЯТСаЮЪЬтЃК
ЂйШєMnFe2O4Љxжаx=0.6ЃЌдђMnFe2O4ЉxжаFe2+еМШЋВПЬњдЊЫиЕФАйЗжТЪЮЊ______ЁЃ
ЂкИУШШЛЏбЇбЛЗжЦЧтЗЈЕФгХЕуга______ЃЈД№СНЕуМДПЩЃЉЁЃ
ЂлИУШШЛЏбЇбЛЗЗЈжЦЧтЩагаВЛзужЎДІЃЌНјвЛВНИФНјЕФбаОПЗНЯђЪЧ______ЁЃ
ЁОД№АИЁПn=3 242ЃК189 ГфЗжЗДгІЁЂГСЕэЭъШЋ ЯДЕгжССїГівКГЪжаад 60% ОпгаЙ§ГЬМђЕЅЁЂНкдМФмСПЁЂЮоЮлШОЁЂЮяСЯСЎМлВЂПЩбЛЗЪЙгУМАбѕЦјКЭЧтЦјдкВЛЭЌВНжшЩњГЩ,вђДЫВЛДцдкИпЮТЦјЬхЗжРыЕФЮЪЬтЕШгХЕу бАевКЯЪЪЕФДпЛЏМС,ЪЙMnFe2O4ЗжНтЮТЖШНЕЕЭЛђевЗжНтЮТЖШИќЕЭЕФбѕЛЏЮя
ЁОНтЮіЁП
Fe(NO3)3КЭMn(NO3)2ЛьКЯНСАшЃЌМгШыKOHШмвКЃЌПижЦpHЁн10.4ГСЕэFe3+ЁЂMn2+ЃЌЙ§ТЫЯДЕгГСЕэЃЌИЩдябаФЅПЩЕУMnFe2O4ЁЃОнДЫЗжЮіНтД№ЁЃ
(1)MnЮЊ+2МлЃЌдђMnFe2O4жаFeЕФЛЏКЯМлЮЊ+3МлЃЌдђFe(NO3)nжаn=3ЃЛгЩMnFe2O4жаПЩжЊЃКFeКЭMnЕФИіЪ§жЎБШЮЊ2ЁУ1ЃЌЫљвдFe(NO3)3гыMn(NO3)2 ЖўепЕФЮяжЪЕФСПжЎБШ 2ЁУ1ЃЌЫљвдЦфжЪСПжЎБШЮЊЃК242ЁС2ЁУ179=484ЁУ179ЃЌЙЪД№АИЮЊЃК3ЃЛ484ЁУ179ЃЛ
(2)СЌајНСАшЪЧЮЊСЫШУFe(NO3)nКЭMn(NO3)2ГфЗжЗДгІЃЌгЩгкШмвКЯдМюадЃЌдђЯДЕгжСЯДЕгвКЮЊжаадЪБЃЌЫЕУїГСЕэЩЯУЛгаШмвКжаЕФРызгЃЌМДГСЕэвбОЯДЕгИЩОЛЃЌЙЪД№АИЮЊЃКГфЗжЗДгІЛђГСЕэЭъШЋЃЛзюКѓвЛДЮЯДЕгвКГЪжаадЃЛ
(3)Ђйx=0.6ЪБЃЌЬњЕФзмМлЬЌЮЊ(4-0.6)ЁС2-2=4.8ЃЌЩш1mol MnFe2O4-0.6жаКЌFe2+ЁЂFe3+ЮяжЪЕФСПЗжБ№ЮЊamolЁЂbmolЃЌдђгаa+b=2ЃЌ2a+3b=4.8ЃЌСЊСЂНтЕУЃКa=1.2ЃЌb=0.8ЃЌдђ1mol MnFe2O4-0.6жаКЌFe2+ЕФЮяжЪЕФСПЮЊ1.2molЃЌдђFe2+еМЕФАйЗжТЪЮЊ![]() ЁС100%=60%ЃЌЙЪД№АИЮЊЃК60%ЃЛ
ЁС100%=60%ЃЌЙЪД№АИЮЊЃК60%ЃЛ
ЂкгЩСїГЬЭМПЩвдПДГіИУШШЛЏбЇбЛЗжЦЧтЗЈЙ§ГЬМђЕЅЁЂНкдМФмСПЁЂЮоЮлШОЁЂЮяСЯСЎМлВЂПЩбЛЗЪЙгУМАбѕЦјКЭЧтЦјдкВЛЭЌВНжшЩњГЩЃЌВЛДцдкИпЮТЦјЬхЗжРыЕФЮЪЬтЕШгХЕуЃЌЙЪД№АИЮЊЃКЙ§ГЬМђЕЅЁЂНкдМФмСПЁЂЮоЮлШОЁЂЮяСЯСЎМлВЂПЩбЛЗЪЙгУМАбѕЦјКЭЧтЦјдкВЛЭЌВНжшЩњГЩЃЌВЛДцдкИпЮТЦјЬхЗжРыЕФЮЪЬтЕШгХЕуЃЛ
ЂлвђИпЮТЯћКФНЯЖрЕФФмдДЃЌИУШШЛЏбЇбЛЗжЦЧтЗЈЕФИФНјПЩвдЭЈЙ§бАевКЯЪЪЕФДпЛЏМСЃЌЪЙMnFe2O4ЗжНтЮТЖШНЕЕЭЛђЗжНтЮТЖШИќЕЭЕФбѕЛЏЮяЃЌЙЪД№АИЮЊЃКбАевКЯЪЪЕФДпЛЏМСЃЌЪЙMnFe2O4ЗжНтЮТЖШНЕЕЭЛђЗжНтЮТЖШИќЕЭЕФбѕЛЏЮяЁЃ



| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГАрбЇЩњЭЈЙ§ЗжзщЪЕбщВтЖЈЫсМюЕЮЖЈЧњЯпЁЃ
ЪЕбщгУЦЗЃК0.1 molЁЄLЃ1HClШмвКЁЂ0.1 molЁЄLЃ1NaOHШмвКЁЂеєСѓЫЎЁЂpHМЦЁЂЫсЪНЕЮЖЈЙмЁЂМюЪНЕЮЖЈЙмЁЂЬњМмЬЈ(ДјЕЮЖЈЙмМа)ЁЂзЖаЮЦПЁЃМзЁЂввЁЂБћШ§зщЭЌбЇзЖаЮЦПжаЕФШмвКЫљШЁЬхЛ§ОљЮЊ20.00 mLЃЌЧвЫљгУЕФЪдМСЭъШЋЯрЭЌЃЌИљОнЪЕбщЫљЕУЕФЪ§ОнЛцжЦЕФЧњЯпЗжБ№ШчЭМжаaЁЂbЁЂcЫљЪОЃЌЦфжаввКЭБћСНзщЭЌбЇЕФВйзїЩЯЖМДцдкзХВЛзуЛђЪЇЮѓЁЃ
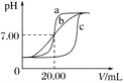
ЧыЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉЪЕбщЧАpHМЦгІгУБъзМШмвКНјаааЃзМЃЌШєНЋpHМЦЗХШыc(HЃЋ)ЃН0.0001 molЁЄLЃ1ЕФБъзМШмвКжааЃзМЃЌдђpHМЦЕФЖСЪ§гІЮЊ________ЁЃ
ЃЈ2ЃЉМззщЭЌбЇЕЮЖЈЪБбЁгУЕФЕЮЖЈЙмЮЊ________(ЬюЁАЫсЪНЁБЛђЁАМюЪНЁБ)ЕЮЖЈЙмЃЌзюКѓвЛДЮШѓЯДЕЮЖЈЙмгІбЁгУЪЕбщгУЦЗжаЕФ________НјааШѓЯДЁЃ
ЃЈ3ЃЉввзщЭЌбЇВйзїЩЯЕФВЛзужЎДІЪЧ________________________________________ЁЃ
ЃЈ4ЃЉдьГЩБћзщЭЌбЇЕФЧњЯпгыМззщЭЌбЇВЛЭЌЕФдвђПЩФмЪЧ________(ЬюзжФИ)ЁЃ
AЃЎгУД§зАвКШѓЯДзЖаЮЦП
BЃЎЕЮЖЈЪЙгУЕФЕЮЖЈЙмЕФМтзьВПЗждкЕЮЖЈЧАгаЦјХнЮДХХГіЃЌЕЮЖЈКѓЦјХнЯћЪЇ
CЃЎЕЮЖЈЧАКѓЖдЕЮЖЈЙмНјааЖСЪ§ЕФЪгЯпЗжБ№ШчЭМЫљЪО

ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГбаОПаЁзщРћгУШэУЬПѓ(жївЊГЩЗжЮЊMnO2ЃЌСэКЌгаЩйСПЬњЁЂТСЁЂЭЁЂФјЕШН№ЪєЛЏКЯЮя)зїЭбСђМСЃЌЭЈЙ§ШчЯТМђЛЏСїГЬМШЭбГ§ШМУКЮВЦјжаЕФSO2ЃЌгжжЦЕУЕчГиВФСЯMnO2(ЗДгІЬѕМўвбЪЁТд)ЁЃЯТСаЫЕЗЈВЛе§ШЗЕФЪЧ
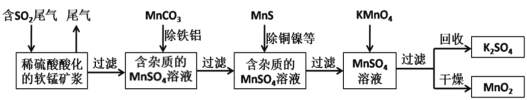
A.ЩЯЪіСїГЬжаЖрДЮЩцМАЕНЙ§ТЫВйзїЃЌЪЕбщЪвНјааЙ§ТЫВйзїЪБашгУЕНЕФЙшЫсбЮВФжЪвЧЦїгаЃКВЃСЇАєЁЂЩеБЁЂТЉЖЗ
B.гУMnCO3ФмГ§ШЅШмвКжаЕФAl3+КЭFe3+ЃЌЦфдвђЪЧMnCO3ЯћКФСЫШмвКжаЕФЫсЃЌДйНјAl3+КЭFe3+ЫЎНтЩњГЩЧтбѕЛЏЮяГСЕэ
C.ЪЕбщЪвгУвЛЖЈСПЕФNaOHШмвККЭЗгЬЊЪдвКОЭПЩвдзМШЗВтЖЈШМУКЮВЦјжаЕФSO2КЌСП
D.MnSO4ШмвКЁњMnO2Й§ГЬжаЃЌгІПижЦШмвКpHВЛФмЬЋаЁ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПдквЛЖЈЮТЖШЯТЃЌНЋЦјЬхXКЭЦјЬхY Иї0.16 molГфШы10 L КуШнУмБеШнЦїжаЃЌЗЂЩњЗДгІЃКXЃЈgЃЉ+ YЃЈgЃЉ![]() 2ZЃЈgЃЉ ЁїH < 0ЃЌвЛЖЮЪБМфКѓДяЕНЦНКтЁЃЗДгІЙ§ГЬжаВтЖЈЕФЪ§ОнШчЯТБэЁЃЯТСаЫЕЗЈе§ШЗЕФЪЧ
2ZЃЈgЃЉ ЁїH < 0ЃЌвЛЖЮЪБМфКѓДяЕНЦНКтЁЃЗДгІЙ§ГЬжаВтЖЈЕФЪ§ОнШчЯТБэЁЃЯТСаЫЕЗЈе§ШЗЕФЪЧ
t / min | 2 | 4 | 7 | 9 |
nЃЈYЃЉ/mol | 0.12 | 0.11 | 0.10 | 0.10 |
A.ЗДгІЧА2minЕФЦНОљЫйТЪvЃЈZЃЉ=2.0ЁС10-5 mol/ЃЈLЁЄminЃЉ
B.ЦфЫћЬѕМўВЛБфЃЌНЕЕЭЮТЖШЃЌЗДгІДяЕНаТЦНКтЧАvЃЈФцЃЉЃОvЃЈе§ЃЉ
C.ИУЮТЖШЯТДЫЗДгІЕФЦНКтГЃЪ§K=1.44
D.ЦфЫћЬѕМўВЛБфЃЌдйГфШы0.2 mol ZЃЌЦНКтЪБXЕФЮяжЪЕФСПХЈЖШМѕаЁ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПдкШнЛ§ЮЊ10LЕФУмБеШнЦїжаЃЌНјааШчЯТЗДгІЃКA(g)+2B(g)![]() C(g)+D(g)ЃЌзюГѕМгШы1.0mol AКЭ2.2mol BЃЌдкВЛЭЌЮТЖШЯТЃЌDЕФЮяжЪЕФСПn(D)КЭЪБМфtЕФЙиЯЕШчЭМ1.
C(g)+D(g)ЃЌзюГѕМгШы1.0mol AКЭ2.2mol BЃЌдкВЛЭЌЮТЖШЯТЃЌDЕФЮяжЪЕФСПn(D)КЭЪБМфtЕФЙиЯЕШчЭМ1.

ЪдЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉ800ЁцЪБЃЌ0ЁЋ5minФкЃЌвдBБэЪОЕФЦНОљЗДгІЫйТЪЮЊ ЃЎ
ЃЈ2ЃЉФмХаЖЯЗДгІДяЕНЛЏбЇЦНКтзДЬЌЕФвРОнЪЧ (ЬюзжФИ)ЃЎ
AЃЎШнЦїжабЙЧПВЛБф BЃЎЛьКЯЦјЬхжаc(A)ВЛБф
CЃЎ2vе§(B)=vФц(D) DЃЎc(A)=c(C)
ЃЈ3ЃЉШєзюГѕМгШы1.0mol AКЭ2.2mol BЃЌРћгУЭМжаЪ§ОнМЦЫу800ЁцЪБЕФЦНКтГЃЪ§K=__________ЃЌИУЗДгІЮЊ__________ЗДгІ(ЬюЁАЮќШШЁБЛђЁАЗХШШЁБ)ЃЎ
ЃЈ4ЃЉ700ЁцЪБЃЌФГЪБПЬВтЕУЬхЯЕжаЮяжЪЕФСПХЈЖШШчЯТЃКn(A)=1.1molЃЌn(B)=2.6molЃЌn(C)=0.9molЃЌn(D)=0.9molЃЌдђДЫЪБИУЗДгІ__________(ЬюЁАЯђе§ЗНЯђНјааЁБЁЂЁАЯђФцЗНЯђНјааЁБЛђЁАДІгкЦНКтзДЬЌЁБ)ЃЎ
ЃЈ5ЃЉдкДпЛЏМСзїгУЯТЃЌCOПЩгУгкКЯГЩМзДМЃКCO(g)+2H2(g)CH3OH(g)ШєдкКуЮТКубЙЕФЬѕМўЯТЃЌЯђУмБеШнЦїжаГфШы4mol COКЭ8mol H2ЃЌКЯГЩМзДМЃЌЦНКтЪБCOЕФзЊЛЏТЪгыЮТЖШЁЂбЙЧПЕФЙиЯЕШчЭМЫљЪОЃК

ЂйИУЗДгІЕФе§ЗДгІЪєгк__________ЗДгІЃЛ(ЬюЁАЮќШШЁБЛђЁАЗХШШЁБ)ЃЎ
Ђкдк0.1MpaЁЂ100ЁцЕФЬѕМўЯТЃЌИУЗДгІДяЕНЦНКтЪБШнЦїФкЦјЬхЕФЮяжЪЕФСПЮЊ molЁЃ
ШєдкКуЮТКуШнЕФЬѕМўЯТЃЌЯђЩЯЪіЦНКтЬхЯЕжаГфШы4mol COЃЌ8mol H2ЃЌгыдЦНКтзДЬЌЯрБШЃЌДяЕНЦНКтЪБCOзЊЛЏТЪ (ЬюЁАдіДѓЁБЃЌЁАВЛБфЁБЛђЁАМѕаЁЁБ)ЃЌЦНКтГЃЪ§K (ЬюЁАдіДѓЁБЃЌЁАВЛБфЁБЛђЁАМѕаЁЁБ)ЃЎ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЩшNAЮЊАЂЗќМгЕТТоГЃЪ§ЕФЪ§жЕЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧ
A.ГЃЮТЯТЃЌ23g NO2КЭN2O4ЕФЛьКЯЦјЬхКЌгаNAИібѕдзг
B.1L0.1molL-1ЕФАБЫЎКЌга0.1NAИіOHЈD
C.БъзМзДПіЯТЃЌNOКЭO2Иї11.2LЛьКЯЃЌЫљЕУЛьКЯЦјЬхЕФЗжзгзмЪ§ЮЊ0.75NA
D.1molFeгы1molCl2ГфЗжЗДгІЃЌзЊвЦ3NAИіЕчзг
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЂёЃЎИпЬњЫсМиЃЈK2FeO4ЃЉЪЧвЛжжаТаЭЁЂИпаЇЁЂЖрЙІФмТЬЩЋЫЎДІРэМСЃЌБШCl2ЁЂO2ЁЂClO2ЁЂKMnO4бѕЛЏадИќЧПЃЌЮоЖўДЮЮлШОЃЌЙЄвЕЩЯЪЧЯШжЦЕУИпЬњЫсФЦЃЌШЛКѓдкЕЭЮТЯТЃЌЯђИпЬњЫсФЦШмвКжаМгШыKOHжСБЅКЭЃЌЪЙИпЬњЫсМиЮіГіЁЃ
(1)ИЩЗЈжЦБИИпЬњЫсФЦЕФжївЊЗДгІЮЊЃК2FeSO4 + aNa2O2ЃН2Na2FeO4 + bX + 2Na2SO4 +cO2ЁќИУЗДгІжаЮяжЪXгІЪЧ__________ЃЌbгыcЕФЙиЯЕЪЧ_______________ЁЃ
(2)ЪЊЗЈжЦБИИпЬњЫсМиЗДгІЬхЯЕжагаСљжжЪ§СЃЃКFe(OH)3ЁЂClOЃЁЂOHЃЁЂFeO42-ЁЂClЃЁЂH2OЁЃ
ЂйаДГіВЂХфЦНЪЊЗЈжЦИпЬњЫсМиЕФРызгЗДгІЗНГЬЪНЃК__________________ЁЃ
ЂкУПЩњГЩ1mol FeO42-зЊвЦ_____________molЕчзгЃЌШєЗДгІЙ§ГЬжазЊвЦСЫ0.3molЕчзгЃЌдђЛЙдВњ[ЮяЕФЮяжЪЕФСПЮЊ_____________molЁЃ
ЂђЃЎвбжЊЃК2Fe3ЃЋЃЋ2IЃ=2Fe2ЃЋЃЋI2ЃЌ2Fe2ЃЋЃЋBr2=2Fe3ЃЋЃЋ2BrЃЁЃ
(3)КЌга1 mol FeI2КЭ2 mol FeBr2ЕФШмвКжаЭЈШы2 mol Cl2ЃЌДЫЪББЛбѕЛЏЕФРызгМАЦфЮяжЪЕФСПЪЧ_______________________________ЁЃ
(4)ШєЯђКЌa mol FeI2КЭb mol FeBr2ЕФШмвКжаЭЈШыc mol Cl2ЃЌЕБIЃЁЂFe2ЃЋЁЂBrЃЭъШЋБЛбѕЛЏЪБЃЌcЮЊ________________________________(гУКЌaЁЂbЕФДњЪ§ЪНБэЪО)ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПгУNAБэЪОАЂЗќМгЕТТоГЃЪ§ЕФжЕЃЌЯТСаЫЕЗЈДэЮѓЕФЪЧ
A.БъзМзДПіЯТЃЌвдШЮвтБШЛьКЯЕФЧтЦјКЭвЛбѕЛЏЬМЦјЬхЙВ8.96LЃЌдкзуСПбѕЦјжаГфЗжШМЩеЪБЯћКФбѕЦјЕФЗжзгЪ§ЮЊ0.2NA
B.гУЖшадЕчМЋЕчНтСђЫсЭШмвКЪБЃЌШєШмвКЕФpHжЕБфЮЊ1ЪБЃЌдђЕчМЋЩЯзЊвЦЕФЕчзгЪ§ФПЮЊNA
C.32.5 gаПгывЛЖЈСПХЈСђЫсЧЁКУЭъШЋЗДгІЃЌЩњГЩЦјЬхЕФЗжзгЪ§ЮЊ0.5NA
D.ЗДгІ3H2(g)ЃЋN2(g)![]() 2NH3(g)ЁЁІЄHЃНЃ92 kJЁЄmolЃ1ЃЌЕБЗХГіШШСП9.2 kJЪБзЊвЦЕчзг0.6NA
2NH3(g)ЁЁІЄHЃНЃ92 kJЁЄmolЃ1ЃЌЕБЗХГіШШСП9.2 kJЪБзЊвЦЕчзг0.6NA
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЩш![]() ДњБэАЂЗќМгЕТТоГЃЪ§ЕФжЕЁЃЯТСаЫЕЗЈВЛе§ШЗЕФЪЧ
ДњБэАЂЗќМгЕТТоГЃЪ§ЕФжЕЁЃЯТСаЫЕЗЈВЛе§ШЗЕФЪЧ
A.КЌ![]() ИіЭдзгЕФCuOКЭ
ИіЭдзгЕФCuOКЭ![]() ЕФЛьКЯЮяжЪСПЮЊ
ЕФЛьКЯЮяжЪСПЮЊ![]()
B.БъзМзДПіЯТЃЌ![]() бѕЦјзїбѕЛЏМСЪБзЊвЦЕчзгЪ§вЛЖЈЮЊ
бѕЦјзїбѕЛЏМСЪБзЊвЦЕчзгЪ§вЛЖЈЮЊ![]()
C.![]() ЬМЫсФЦШмвКжаДјЕчСЃзгЪ§вЛЖЈДѓгк
ЬМЫсФЦШмвКжаДјЕчСЃзгЪ§вЛЖЈДѓгк![]()
D.![]() ХЈСђЫсгызуСПаПСЃЗДгІЃЌВњЩњЕФЦјЬхЗжзгЪ§аЁгк
ХЈСђЫсгызуСПаПСЃЗДгІЃЌВњЩњЕФЦјЬхЗжзгЪ§аЁгк![]()
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com