
【题目】I.写出下列反应的化学方程式,标“*”的请写出离子反应方程式
(1)*向四羟基合铝酸纳溶液中通入过量的二氧化碳气体_________。
(2)*向氯化铝溶液中加入过量氨水_________。
(3)实验室利用浓氨水快速制取氨气_________。
(4)*实验室利用二氧化锰固体制取氯气_________。
(5)*将“84消毒液”和“洁厕灵”(主要成分为浓盐酸)混合产生有毒气体_________。
II.写出下列物质的电子式
(6)乙烷(C2H6) _________。
(7)氢氧化钠_________。
III.写出一氯丙烷(C3H7Cl)的结构简式_________。
【答案】 CO2+[Al(OH)4]-=Al(OH)3↓+HCO3- Al3++3NH3·H2O=Al(OH)3↓+3NH4+ NH3·H2O ![]() NH3↑+H2O MnO2+4H++2Cl-
NH3↑+H2O MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O C1O-+Cl-+2H+=Cl2↑+H2O
Mn2++Cl2↑+2H2O C1O-+Cl-+2H+=Cl2↑+H2O ![]()
![]() CH3CH2CH2Cl CH3CHClCH3
CH3CH2CH2Cl CH3CHClCH3
【解析】考查化学用语,I.(1)碳酸的酸性强于偏铝酸,因此通入过量的CO2,发生CO2+[Al(OH)4]-=Al(OH)3↓+HCO3-;(2)反应生成氢氧化铝沉淀,离子反应方程式为Al3++3OH-=Al(OH)3↓+3NH4+;(3)利用NaOH固体或生石灰与水放出大量的热,使NH3·H2O分解成NH3,化学反应方程式为NH3·H2O![]() NH3↑+H2O;(4)利用MnO2与浓盐酸反应生成氯气,即离子方程式为MnO2+4H++2Cl-
NH3↑+H2O;(4)利用MnO2与浓盐酸反应生成氯气,即离子方程式为MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O;(5)“84”消毒液的成分是NaClO,洁厕灵的主要成分是浓盐酸,两者混合发生Cl-+ClO-+2H+=Cl2↑+H2O;II.(6)乙烷的电子式为
Mn2++Cl2↑+2H2O;(5)“84”消毒液的成分是NaClO,洁厕灵的主要成分是浓盐酸,两者混合发生Cl-+ClO-+2H+=Cl2↑+H2O;II.(6)乙烷的电子式为![]() ;(7)NaOH属于离子化合物,其电子式为
;(7)NaOH属于离子化合物,其电子式为![]() ;III.C3H8的结构简式为CH3CH2CH3,有两种不同的氢原子,一氯代物有2种,即CH3CH2CH2Cl、CH3CHClCH3。
;III.C3H8的结构简式为CH3CH2CH3,有两种不同的氢原子,一氯代物有2种,即CH3CH2CH2Cl、CH3CHClCH3。


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:
【题目】两种微粒,它们的质子数和电子数相等。对这两种微粒关系的下列叙述不正确的是( )
A.它们可能是两种不同的分子B.它们可能是两种不同的原子
C.它们可能是两种不同的离子D.可能一种是分子,另一种是离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述:①我国科学家在世界上第一次人工合成结晶牛胰岛素;②最早发现电子的是英国科学家道尔顿;③创造联合制碱法的是我国著名科学家侯德榜;④首先制得氧气的是法国科学家拉瓦锡;⑤有机物的元素定量分析最早是由牛顿提出的,其中正确的是( )
A.只有①
B.①和③
C.①②③
D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需要0.1mol/LNaOH溶液450mL和0.5mol/L硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题:
(1)容量瓶不能用于(填序号).
A.配制一定体积准确浓度的标准溶液
B.贮存溶液
C.测量容量瓶规格以下的任意体积的液体
D.用来加热溶解固体溶质
(2)根据计算用托盘天平称取NaOH的质量为g.在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度0.1mol/L(填“大于”“等于”或“小于”,下同).若NaOH溶液在转移至容量瓶时,洒落了少许,则所得溶液浓度0.1mol/L.
(3)根据计算得知,所需质量分数为98%、密度为1.84g/cm3的浓硫酸的体积为mL(计算结果保留一位小数)配制过程中需先在烧杯中将浓硫酸进行稀释,稀释时操作方法是 . 在配制过程中,下列操作中,能引起误差偏高的有(填代号).
①未等稀释后的H2SO4溶液冷却至室温就转移到容量瓶中
②定容时,加蒸馏水超过刻度线,又用胶头滴管吸出
③定容摇匀后,发现液面低于刻度线,又用胶头滴管加蒸馏水至刻度线
④定容时,俯视刻度线.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种短周期元素在周期表中的位置如图,其中只有M为金属元素.下列说法不正确的是( ) 
A.原子半径Z<M
B.Y的最高价氧化物对应水化物的酸性比X的弱
C.X的最简单气态氢化物的热稳定性比Z的小
D.Z位于元素周期表中第2周期第ⅥA族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组为了探究甲烷和氯气反应的情况,设计了几个实验。
请填写下列空白:
[实验一]用如图所示装置,收集一试管甲烷和氯气的混合气体,光照后观察到,量筒内形成一段水柱,认为有氯化氢生成。
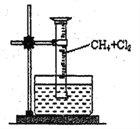
(1)该反应的反应类型为_____________________。
(2)该反应的化学方程式为(只写第一步)______________。
(3)水槽中盛放的液体应为_______。(填标号)
A.水 B.饱和石灰水 C.饱和食盐水 D.饱和NaHCO3溶液
(4)该实验的实验现象为:____________、_____________、试管壁上出现油状液滴
(5)该油状液滴中含有的有机产物共有_______种。
[实验二]收集一试管甲烷和氯气的混合气体,光照反应后,滴加AgNO3溶液,看到有白色沉锭生成,认为有氯化氢生成。
(6)你认为该实验设计得出的结论是否正确的______,若不正确,理由是:_________________。
[实验三]步骤一:收集半试管氯气,加入10mL蒸馏水,充分振荡,采用DIS系统的pH传感器测溶液的pH(下同),测得pH=3.26
步骤二:收集一试管甲垸和氯气的混合气体(各占50%),在40W的日光灯下光照6min后,加入l0mL蒸馏水,充分振荡,测得pH=1.00。
(7)判断该反应中有氯化氢生成的依据是__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是周期表中的一部分,根据A~I在周期表中的位置,用元素符号或化学式回答下列问题:
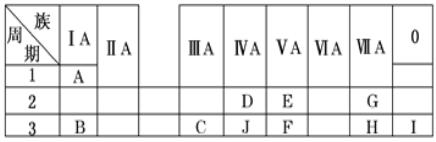
(1)表中元素,化学性质最不活泼的是________,只有负价而无正价的元素是________。(填元素符号)
(2)最高价氧化物的水化物酸性最强的是________,呈两性的是________。
(3)在B、C、E、F中,原子半径最大的是________。
(4)写出B与C两种元素的最高价氧化物对应的水化物相互反应的化学方程式:________。
(5)与C元素同族的第5周期元素X的价电子排布式________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质应用与其性质密切相关,下列说法错误的是( )
A.硅胶可防止食物受潮是由于其具有吸水性
B.葡萄糖用于医疗输液是因为它属于强电解质
C.Na2CO3可用作食用碱,因为Na2CO3的水溶液显碱性
D.酸性重铬酸钾用于检查酒驾是利用其强氧化性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com