
| A、温度计的水银球应插入蒸馏烧瓶中的自来水中 |
| B、冷凝管中的水流方向是从下口进入,上口排出 |
| C、实验中需要在蒸馏烧瓶中加入几粒碎瓷片,防止出现暴沸现象 |
| D、蒸馏烧瓶必须垫石棉网 |
 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案科目:高中化学 来源: 题型:
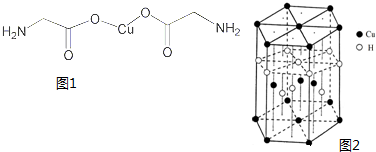 (1)亚铜离子(Cu+)基态时的价电子排布式表示为
(1)亚铜离子(Cu+)基态时的价电子排布式表示为查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1mol |
| B、0.5mol |
| C、0.15mol |
| D、0.25mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
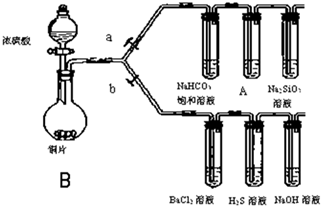 根据要求完成下列各小题实验目的.(如图a、b为弹簧夹,加热及固定装置已略去)
根据要求完成下列各小题实验目的.(如图a、b为弹簧夹,加热及固定装置已略去)| 滴加的溶液 | 氯水 | 氨水 |
| 沉淀的化学式 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用浓FeCl3溶液和NaOH溶液混合制备Fe(OH)3胶体 |
| B、将混有少量HCl的CO2通入饱和NaHCO3溶液中除去HCl |
| C、用湿润的pH试纸测定等浓度的Na2CO3和Na2SO3溶液的pH大小 |
| D、用AgNO3溶液鉴别Na2SO4溶液与NaCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
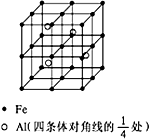 第四周期过渡元素Fe、Ti可与C、H、N、O形成多种化合物.
第四周期过渡元素Fe、Ti可与C、H、N、O形成多种化合物.查看答案和解析>>
科目:高中化学 来源: 题型:
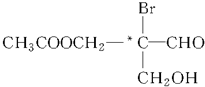 下列有机物分子中带“*”碳原子就是手性碳原子.该有机物分别发生下列反应,生成的有机物分子中含有手性碳原子的是( )
下列有机物分子中带“*”碳原子就是手性碳原子.该有机物分别发生下列反应,生成的有机物分子中含有手性碳原子的是( )| A、与乙酸发生酯化反应 |
| B、在稀硫酸作用下水解 |
| C、与银氨溶液作用发生银镜反应 |
| D、催化剂作用下与H2反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com