
【题目】回答下列问题
(1)乙醇沸点是78℃,能与水以任意比例混溶.乙醚的沸点为34.6℃,难溶于水,在饱和Na2CO3溶液中几乎不溶,乙醚极易燃烧.实验室制乙醚的反应原理是:2CH3CH2OH ![]() CH3CH2OCH2CH3+H2O ①反应中应加入沸石,其作用是;
CH3CH2OCH2CH3+H2O ①反应中应加入沸石,其作用是;
②反应中温度计的位置是;
③该装置制得乙醚中可能含有大量的副产物乙烯,化学方程式: .
(2).苯和甲烷是两类烃的代表物质,回答下列问题: ①苯在常温常压下呈态.
②苯和甲烷中含碳量较高的是 .
③写出甲烷在氧气中燃烧的化学方程式 . 若将等物质的量的苯和甲烷分别燃烧,耗氧量较大的是 .
④写出苯与溴单质反应的化学方程式 .
【答案】
(1)防止瀑沸;插入反应物液面以下,但不能触及瓶底;CH3CH2OH ![]() CH2=CH2↑+H2O
CH2=CH2↑+H2O
(2)液;苯;CH4+2O2 ![]() CO2+2H2O;苯;
CO2+2H2O;苯;
【解析】解:(1)①反应中应加入沸石,其作用是防止液体瀑沸; 所以答案是:防止瀑沸;②温度计测量的是混合液的温度,所以温度计水银球应该插入反应物液面以下,但不能触及瓶底;
所以答案是:插入反应物液面以下,但不能触及瓶底;③乙醇在浓硫酸作用下加热到170℃就可以生成乙烯,化学方程式为:CH3CH2OH ![]() CH2=CH2↑+H2O;
CH2=CH2↑+H2O;
所以答案是:CH3CH2OH ![]() CH2=CH2↑+H2O;
CH2=CH2↑+H2O;
(2.)①苯在常温常压下呈液态;所以答案是:液;②根据其最简式判断含碳量高低,甲烷的分子式和最简式都是CH4 , 苯的最简式为CH,则苯中含碳量高;
所以答案是:苯;③甲烷燃烧生成二氧化碳和水,反应方程式为:CH4+2O2 ![]() CO2+2H2O,苯燃烧方程式为:C6H6+7.5O2
CO2+2H2O,苯燃烧方程式为:C6H6+7.5O2 ![]() 6 CO2+3H2O,则将等物质的量的苯和甲烷分别燃烧,耗氧量较大的是苯;
6 CO2+3H2O,则将等物质的量的苯和甲烷分别燃烧,耗氧量较大的是苯;
所以答案是:CH4+2O2 ![]() CO2+2H2O;苯④在溴化铁或者铁作催化剂条件下,苯和液溴发生取代反应,反应方程式为:
CO2+2H2O;苯④在溴化铁或者铁作催化剂条件下,苯和液溴发生取代反应,反应方程式为:  ;
;
所以答案是:  .
.


 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案科目:高中化学 来源: 题型:
【题目】下列各组物质既不属于同系物,也不属于同分异构体的是( )
A. 邻氯甲苯和对氯甲苯 B. 一氯甲烷和二氯乙烷
C. 乙酸和硬脂酸 D. 蔗糖和麦芽糖
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列A、B、C、D是中学常见的混合物分离或提纯的基本装置.
请根据混合物分离或提纯的原理,回答在下列实验中需要使用哪种装置.将A、B、C、D 填入适当的空格中.
(1)分离植物油和水;
(2)除去粗盐中的泥沙;
(3)与海水晒盐原理相似的是;
(4)用四氯化碳碘水中提取碘;
(5)分离CCl4(沸点:76.75℃)和甲苯(沸点:110.6℃)的混合物 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取1.43gNa2CO3xH2O溶于水配成10mL溶液,然后逐滴滴入稀盐酸直至没有气体放出为止,用去盐酸2.0mL,并收集到112mL CO2(标准状况).试计算:
(1)CO2的物质的量
(2)Na2CO3xH2O的物质的量.
(3)x的值.
(4)所用稀盐酸的物质的浓度.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组比值为1∶2的是( )
A. 0.1mol/L与0.2mol/L醋酸溶液,c(H+)之比
B. 0.lmol/LNa2CO3溶液,c(CO32-)与c(Na+)之比
C. pH=10的Ba(OH)2溶液与氨水,溶质的物质的量浓度之比
D. pH=3的硫酸与醋酸溶液,c(SO42-)与c(CH3COO-)之比
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列实验装置或操作进行相应实验,能达到实验目的是( ) 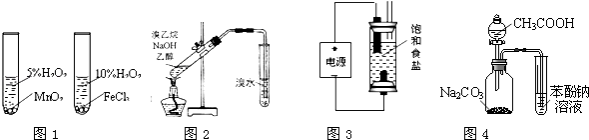
A.用图1装置验证比较不同催化剂对反应速率的影响
B.用图2所示装置检验溴乙烷与NaOH醇溶液共热产生的乙烯
C.用图3装置制备少量含NaClO的消毒液
D.利用图4装置证明酸性:CH3COOH>H2CO3>苯酚
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现将有铜的印刷线路板浸入120mL氯化铁浓溶液中,有9.6g铜被腐蚀掉.取出印刷线路板,向溶液中加入8.4g铁粉,经充分反应,溶液中还存在4.8g不溶解的物质.(设溶液体积不变,且不考虑金属离子水解).请回答下列问题:
(1)充分反应后,溶液中存在4.8g不溶物的成分为(用化学式表示).
(2)充分反应后溶液中一定不存在的金属离子为 .
(3)比较Fe2+、Fe3+、Cu2+的氧化性大小: .
(4)试计算最后溶液中Fe2+离子的物质的量浓度mol/L.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】固体氧化物燃料电池是以固体氧化锆﹣氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2﹣)在其间通过.该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应,下列判断正确的是( ) 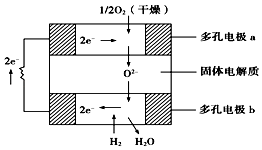
A.有O2参加反应的a极为电池的负极
B.b极的电极反应式为H2+O2﹣﹣2e﹣═H2O
C.a极对应的电极反应式为O2+2H2O+4e﹣═4OH﹣
D.氧化锆的作用是让电子在电池内部通过
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)一I3-(aq),某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法不正确的是( )
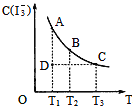
A. 反应I2(aq)+I-(aq)=I3-(aq)△H<0
B. 若温度为T1、T2反应的平衡常数分别为K1、K2,则K1>K2
C. 若反应进行到状态D时,一定有v正>v逆
D. 状态A与状态B相比,状态A的c(I2)大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com