
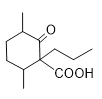
【题目】化合物G是一种药物合成中间体,其合成路线如下:
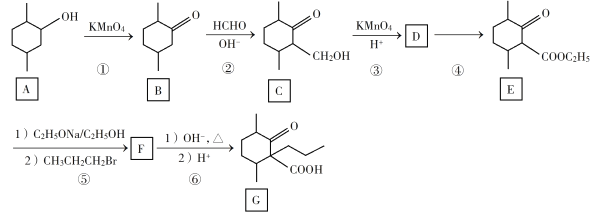
回答下列问题:
(1)C中的官能团名称是________________。
(2)碳原子上连有4个不同的原子或基团时,该碳称为手性碳。在B的结构简式中,用星号(*)标出B中的手性碳_____________________。
(3)写出具有六元环结构、且环上只有1个取代基,并能与NaOH溶液发生反应的C的同分异构体的结构简式______________。(不考虑立体异构,只需写出2个)
(4)反应④所需的试剂和条件是____________________。
(5)②、⑤的反应类型是____________________。
(6)写出F到G的反应方程式_____________ 、_______________。
(7)乙酸苯甲酯(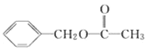 )是一种常用香料,设计以甲苯和乙酸为原料制备乙酸苯甲酯的合成路线:__________(无机试剂任选)。
)是一种常用香料,设计以甲苯和乙酸为原料制备乙酸苯甲酯的合成路线:__________(无机试剂任选)。
【答案】羟基、羰基 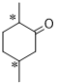
 C2H5OH/浓硫酸 加热 加成反应;取代反应
C2H5OH/浓硫酸 加热 加成反应;取代反应  + OH-
+ OH-![]()
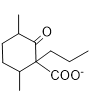 +C2H5OH
+C2H5OH 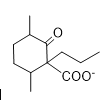 +H+
+H+![]()

【解析】
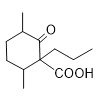
A发生氧化反应生成B,B发生加成反应生成C,C发生氧化反应生成D,根据E结构简式知,D为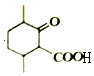 ,D发生酯化反应生成E,F先发生碱性条件下水解然后酸化得到G,根据E、G结构简式知,E发生取代反应生成F,F为
,D发生酯化反应生成E,F先发生碱性条件下水解然后酸化得到G,根据E、G结构简式知,E发生取代反应生成F,F为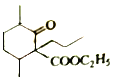 ;
;
(7)甲苯与液溴在光照条件下发生取代反应生成![]() ,然后在氢氧化钠水溶液、加热条件下发生水解反应生成
,然后在氢氧化钠水溶液、加热条件下发生水解反应生成![]() ,最后与乙酸发生酯化反应生成
,最后与乙酸发生酯化反应生成![]() 。
。
(1)C的结构简式为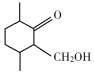 ,含有官能团名称是羟基、羰基;
,含有官能团名称是羟基、羰基;
(2)B的结构简式为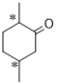 ,其中带*碳原子为手性碳;
,其中带*碳原子为手性碳;
(3) C的结构简式为 ,其同分异构体的条件是:具有六元环结构、且环上只有1个取代基,并能与NaOH溶液发生反应,说明含有羧基或酯基,则满足条件的同分异构体的结构简式可能是
,其同分异构体的条件是:具有六元环结构、且环上只有1个取代基,并能与NaOH溶液发生反应,说明含有羧基或酯基,则满足条件的同分异构体的结构简式可能是![]() 、
、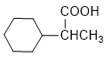 、
、![]() 或
或![]() 等;
等;
(4)反应④为D发生酯化反应生成E,所需的试剂和条件是C2H5OH/浓硫酸并加热;
(5) B发生加成反应生成C,说明反应②为加成反应;E发生取代反应生成F,说明反应⑤的反应类型是取代反应;
(6) F→G的反应方程式包括 + OH-
+ OH-![]()
 +C2H5OH和
+C2H5OH和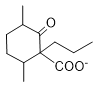 +H+
+H+![]()
 ;
;
(7)甲苯与液溴在光照条件下发生取代反应生成![]() ,然后在氢氧化钠水溶液、加热条件下发生水解反应生成
,然后在氢氧化钠水溶液、加热条件下发生水解反应生成![]() ,最后与乙酸发生酯化反应生成
,最后与乙酸发生酯化反应生成![]() ,合成路线流程图为:
,合成路线流程图为: 。
。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】某实验小组用下列装置制备溴苯,下列说法错误的是( )
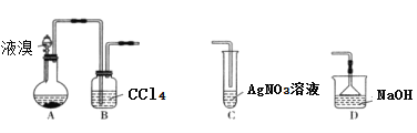
A.装置A中长玻璃导管仅起导气作用,装置B中的实验现象是CCl4由无色变橙色
B.若装置B后连接装置C,装置C中生成淡黄色沉淀,可证明装置A中发生取代反应
C.若装置B后连接装置D,则装置D的作用是吸收尾气
D.向反应后的装置A中加入NaOH溶液,振荡静置,下层为无色油状液体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨是人类科学技术发展史上的一项重大突破,解决了地球上因粮食不足导致的饥饿和死亡问题,这也充分说明了含氮化合物对人类生存的巨大意义。回答下列问题
(1)工业上用氢气和氮气直接合成氨,写出反应的化学方程式_______________。氨气极易溶于水,水溶液显 _____性,能使酚酞溶液变____色,使湿润的红色石蕊试纸变_____色。
(2)氮的氧化物有多种,一氧化氮和二氧化氮都是大气污染物。氨气在催化剂作用下可被氧化生成一氧化氮,一氧化氮气体与空气变___色,原因是__________(用化学方程式表示);二氧化氮易溶于水并与水反应,此反应的氧化剂是_______,还原剂是______,氧化剂和还原剂的质量之比为______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是![]()
A.![]() 相等的
相等的![]() 溶液、
溶液、![]() 溶液和
溶液和![]() 溶液中,溶质浓度大小关系是:
溶液中,溶质浓度大小关系是:![]()
B.![]() 的
的![]() 溶液加水稀释,溶液中
溶液加水稀释,溶液中![]() 减小
减小
C.![]() 溶液与等体积
溶液与等体积![]() 溶液混合后,溶液的
溶液混合后,溶液的![]()
D.![]() 的
的![]() 溶液中
溶液中![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在隔绝空气的条件下,某同学将一块部分被氧化的钠块用一张已除去氧化膜、并用针刺一些小孔的铝箔包好,然后放入盛满水且倒置于水槽中的容器内。待钠块反应完全后,在容器中仅收集到1.12 L氢气(标准状况),此时测得铝箔质量比反应前减少了0.27 g,水槽和容器内溶液的总体积为2.0 L,溶液中NaOH的浓度为0.050 mol·L-1(忽略溶液中离子的水解和溶解的氢气的量)。
(1)写出该实验中发生反应的化学方程式:_____________ _____________ _____________
(2)试通过计算确定该钠块中钠元素的质量分数为_________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溶液X中可能含有K+、Mg2+、Al3+、AlO、SiO、CO、SO、SO中的若干种离子。某同学对该溶液进行了如下实验:

下列判断正确的是( )
A. 气体甲一定是纯净物 B. 沉淀甲是硅酸和硅酸镁的混合物
C. K+、AlO和SiO一定存在于溶液X中 D. CO和SO一定不存在于溶液X中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Al-Ag2O电池是一种可用作水下动力的优良电源,其原理如图所示。该电池工作时总反应式为2Al+3Ag2O+2NaOH=2NaAlO2+6Ag+H2O,则下列说法错误的是 ( )。
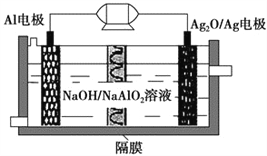
A. 工作时正极发生还原反应,且正极质量逐渐减小
B. 当电极上生成1.08 g Ag时,电路中转移的电子为0.1 mol
C. Al电极的反应式为Al-3e-+4OH-=AlO2-+2H2O
D. 工作时电解液中的Na+移向Ag2O/Ag电极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】类比推理是学习化学的重要的思维方法,下列陈述Ⅰ及类比推理陈述Ⅱ均正确的是( )
陈述Ⅰ | 类比推理陈述Ⅱ | |
A | 单质的熔点Br2 < I2 | 单质的熔点Li < Na |
B | 工业上电解熔融的Al2O3得到铝单质 | 工业上电解熔融的MgO得到镁单质 |
C | 还原性:I- > Br- | 还原性:P3- > N3- |
D | 溶解度:CaCO3<Ca(HCO3)2 | 溶解度:Na2CO3<NaHCO3 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,将气体 X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应:X(g)+Y(g) ![]() 2Z(g) ΔH<0。一段时间后达到平衡,反应过程中测定的数据如表,下列说法正确的是
2Z(g) ΔH<0。一段时间后达到平衡,反应过程中测定的数据如表,下列说法正确的是

A.反应前2min的平均速率v(Z)<2.0×103mol·L-1·min-1
B.其他条件不变,降低温度,反应达到新平衡前:v(逆)>v(正)
C.保持其他条件不变,起始时向容器中充入0.32mol气体X和0.32mol气体Y,到达平衡时,c(Z)>0.24mol·L-1
D.该温度下此反应的平衡常数:K=1.44
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com