
【题目】如图所示为科学家正在研发的新型电池,该电池容量大,电流稳定等多方面优点。该电池的电池总反应式为:Na(1-x)MO2+NaxCn![]() NaMO2+nC,下列说法正确的是( )
NaMO2+nC,下列说法正确的是( )
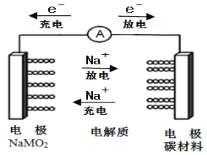
A.电池充电时,NaMO2电极为阳极
B.放电时,负极反应式:NaMO2-xe-=Na(1-x)MO2+xNa+
C.电解质可以选用无水乙醇
D.充电时,阳极反应式为:nC+xNa++xe-=NaxCn
 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案科目:高中化学 来源: 题型:
【题目】海水电池常用在海上浮标等助航设备中,其示意图如图所示。电池反应为2Li+2H2O=2LiOH+H2↑。电池工作时,下列说法错误的是( )

A.金属锂作负极
B.电子从锂电极经导线流向镍电极
C.海水作为电解质溶液
D.可将电能转化为化学能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸锶(SrSO4)在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是
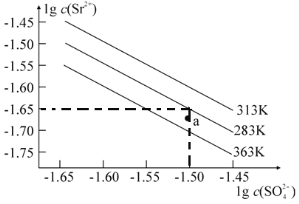
A.283K时,图中a点对应的溶液是不饱和溶液
B.温度一定时,Ksp(SrSO4)随c(SO42-)的增大而减小
C.283 K下的SrSO4饱和溶液升温到363K后变为不饱和溶液
D.三个不同温度中,363 K时Ksp(SrSO4)最大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用反应6NO2+8NH3=7N2+12H2O构成电池的装置如图所示。此方法既能实现有效清除氮氧化物的排放,减轻环境污染,又能充分利用化学能。下列说法正确的是( )

A.该装置将化学能转化为电能
B.电极B为正极
C.电极A的反应式为:2NH3-6e-=N2+6H+
D.当有4.48LNO2被处理时,转移0.8mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C三种短周期元素,原子序数依次增大,三种元素原子序数之和为36,A、C同族,B2+离子核外有10个电子,回答下列问题:
(1)A、B、C三种元素的符号分别是_________、_________、_________
(2)A、B、C之间任取两种能形成多种化合物,其中属于共价化合物的化学式分别为_________、___________
(3)分别写出A、B的电子排布式:A_________、B________
(4)写出C的价电子轨道排布图:________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫、氮的氧化物是形成酸雨的主要原因,一种比较常用的方法是用NH3处理氮的氧化物(NxOy)。完成下列问题。
(1)已知:①2NO(g)=N2(g)+O2(g) △H=-177kJ/mol
②4NH3(g)+3O2(g)=2N2(g)+6H2O(g) △H=-1253.4kJ/mol
则用NH3处理NO生成氮气和气态水的热化学方程式为__。
(2)已知:N2(g)+3H2(g)![]() 2NH3(g) △H<0。不同温度下,向三个一样的容器中投入相同的反应物进行反应,测得不同压强下平衡混合物中NH3的物质的量分数如图所示。
2NH3(g) △H<0。不同温度下,向三个一样的容器中投入相同的反应物进行反应,测得不同压强下平衡混合物中NH3的物质的量分数如图所示。

①M点的v正__Q点的v正(填“>”“<”或“=”),原因是__。
②维持10MPa、T3℃的条件不变,要提高H2的转化率,可以采取的措施是__(任写一条)。
③图中三条曲线对应的温度T1、T2、T3由高到低的顺序为___。
④恒温恒容条件下,能说明反应N2(g)+3H2(g)![]() 2NH3(g)达到平衡状态的是__(填选项字母)
2NH3(g)达到平衡状态的是__(填选项字母)
A.![]() 保持不变
保持不变
B.3molH-H键断裂的同时,有2molN-H键断裂
C.2v(N2)=v(NH3)
D.反应器中的压强不再发生变化
⑤T3温度下,将1molN2和3molH2充入2L的恒容密闭容器中反应,一段时间后达到N点的平衡状态,则反应的平衡常数为K=__(结果保留2位小数),M点与Q点对应的平衡常数大小关系为M__Q(填“>”“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把铝粉和四氧化三铁粉配成铝热剂,分成两等份。一份在高温下恰好完全反应后,再与足量盐酸起反应;另一份放入足量的烧碱溶液中充分反应;前后两种情况下生成的气体的质量比是
A.8:9B.2:3C.3:4D.4:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向100 mLBaCl2、AlCl3、FeCl3的混合溶液A中,逐滴加入Na2SO4和NaOH的混合溶液B,产生的沉淀和加入混合溶液B的体积关系如下图所示:

(1)加入B溶液110 mL时,溶液中的沉淀是______,溶液中的溶质是__________。
(2)从90 mL至100mL之间加入10mL B溶液时发生的离子反应方程式是:Ba2++ SO42—=BaSO4↓,Al(OH)3+ OH— =AlO2— +2H2O,溶液B中Na2SO4与NaOH的物质的量浓度之比为____;
(3)计算A溶液中AlCl3的物质的量浓度,_______________写出计算过程)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com