
【题目】在36 g碳不完全燃烧所得气体中,CO占![]() 体积,CO2占
体积,CO2占![]() 体积。且有:
体积。且有:
C(s)+![]() O2(g)===CO(g) ΔH=-110.5 kJ·mol-1
O2(g)===CO(g) ΔH=-110.5 kJ·mol-1
CO(g)+![]() O2(g)===CO2(g) ΔH=-283 kJ·mol-1
O2(g)===CO2(g) ΔH=-283 kJ·mol-1
与这些碳完全燃烧相比,损失的热量是
A. 172.5 kJ B. 1 149 kJ C. 283 kJ D. 517.5 kJ
科目:高中化学 来源: 题型:
【题目】对室温下c(H+)相同、体积相同的醋酸和盐酸两种溶液分别采取下列措施,有关叙述正确的是
A. 加适量的醋酸钠晶体后,两溶液的c(H+)均减小
B. 使温度都升高20℃后,两溶液的c(H+)均不变
C. 加水稀释2倍后,两溶液的c(H+)均增大
D. 加足量的锌充分反应后,两溶液中产生的氢气一样多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】管道工人曾经用浓氨水检查氯气管道是否漏气。已知能发生如下反应(在有水蒸气存在的条件下):2NH3+3Cl2=6HCl+N2。下列说法错误的是( )
A.若管道漏气,遇氨就会产生白烟
B.该反应属于复分解反应
C.该反应属于氧化还原反应
D.该反应中Cl2是氧化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋植物如海带、海藻中含有丰富的碘元素,主要以碘化物形式存在。有一化学课外小组用海带 为原料制取少量碘单质,他们将海带灼烧成灰,用水浸泡一段时间(让碘化物充分溶解在水中), 得到海带灰悬浊液,然后按以下实验流程提取单质碘:
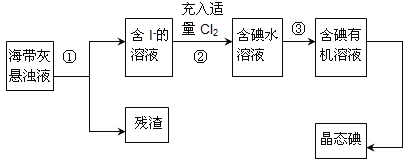
(1)指出提取碘的过程中有关的实验操作名称:①_______,③_______。
(2)操作③中所用的有机试剂可以是________(填序号)A.四氯化碳 B.乙醇,简述选择其理由________。
(3)操作过程③可以分解为如下几步:
A.检验分液漏斗活塞和上口的玻璃塞是否漏液;
B.把50mL碘水和15mL 有机溶剂(你所选的)加入分液漏斗中,并盖好玻璃塞;
C.倒转漏斗用力振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正;
D.把盛有溶液的分液漏斗放在铁架台的铁圈中;
E.静置、分层。
F.将漏斗上口的玻璃塞打开或使塞上的凹槽与漏斗上口的小孔对准;
G.旋开活塞,用烧杯接收下层溶液;
H.从分液漏斗上口倒出上层液体;
①上述F步操作的目的是:____;
②最后碘的有机溶液是通过_____获得(填“漏斗上口”或“漏斗下口”)。
(4)从含碘的有机溶液中提取碘和回收有机溶液,还需要经过蒸馏,观察如图所示实验装置,指出其错误之处并加以改正_____。
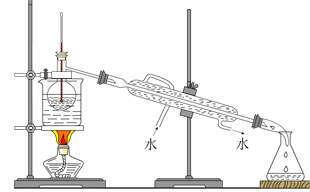
(5)进行上述蒸馏操作时,使用水浴的原因是 _______,最后晶态碘在________里聚集。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaCl溶液中混有Na2SO4、CaCl2溶液和淀粉胶体,选择适当的试剂和方法从中提纯出NaCl晶体。相应的实验过程如图:
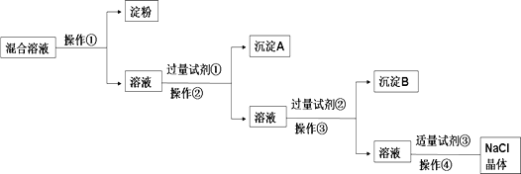
(1)写出上述实验过程中所用试剂:试剂①____;试剂③____。
(2)判断试剂①已过量的方法是:_____。
(3)操作①是利用半透膜进行分离提纯,操作①的实验结果:淀粉___(填“能”或“不能”)透过半透膜。
(4)操作④的名称是____,其中玻璃棒的作用是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)现有下列10种物质:①盐酸 ②石墨 ③Mg ④CaO ⑤H2SO4 ⑥Ca(OH)2 溶液 ⑦酒精 ⑧NaHCO3 ⑨CO2 ⑩Na2CO310H2O。其中,属于非电解质有___,属于电解质的____。
(2)下列方程式中属于氧化还原反应的是___。
①2H2+O2![]() 2H2O ②CuO+H2
2H2O ②CuO+H2![]() Cu+H2O
Cu+H2O
③NH4HCO3![]() NH3↑+H2O↑+CO2↑ ④2CO+O2
NH3↑+H2O↑+CO2↑ ④2CO+O2![]() 2CO2
2CO2
⑤H2O(g)+C![]() H2+CO ⑥Ba(OH)2+H2SO4===BaSO4↓+2H2O
H2+CO ⑥Ba(OH)2+H2SO4===BaSO4↓+2H2O
(3)19g某二价金属氯化物(ACl2)中含有0.4molCl-,则A的相对原子质量=___。
(4)写出NaHCO3的电离方程式__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①2SO2(g)+O2(g)=2SO3(g)ΔH=-196.6 kJ·mol-1,②2NO(g)+O2(g)===2NO2(g) ΔH=-113.0 kJ·mol-1。下列热化学方程式正确的是
A. NO2(g)+SO2(g) ![]() SO3(s)+NO(g) ΔH=-41.8 kJ·mol-1
SO3(s)+NO(g) ΔH=-41.8 kJ·mol-1
B. SO3(g)+NO(g) ![]() NO2(g)+SO2(g) ΔH=+41.8 kJ·mol-1
NO2(g)+SO2(g) ΔH=+41.8 kJ·mol-1
C. NO2(g)+SO2(g) ![]() SO3(g)+NO(g) ΔH=-77.4 kJ·mol-1
SO3(g)+NO(g) ΔH=-77.4 kJ·mol-1
D. NO2(g)+SO2(g) ![]() SO3(g)+NO(g) ΔH=-183.6 kJ·mol-1
SO3(g)+NO(g) ΔH=-183.6 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲胺铅碘(CH3NH3PbI3)可用作全固态钙钛矿敏化太阳能电池的敏化剂,该物质可由甲胺(CH3NH2)、PbI2及HI为原料来合成。请回答下列问题:
(1)制取甲胺的反应为CH3OH(g)+NH3(g)===CH3NH2(g)+H2O(g),已知该反应中相关化学键的键能数据如下表所示:

则该反应的△H=___________kJ·mol-1
(2)工业上利用水煤气合成甲醇的反应为CO(g)+2H2(g)![]() CH3OH(g) △H<0。一定温度下,向体积为2L的密闭容器中加人CO和H2,5min末反应达到化学平衡状态,测得各组分浓度如下表所示。
CH3OH(g) △H<0。一定温度下,向体积为2L的密闭容器中加人CO和H2,5min末反应达到化学平衡状态,测得各组分浓度如下表所示。

①0~5min内,用CO表示的平均反应速率为___________。
②既能加快反应速率,又能提高氢气转化率的措施有___________(答一条即可)。
③能说明上述反应已达化学平衡状态的是___________(填字母)。
A.v正(CO)=2v逆(H2)
B.混合气体密度保持不变
C.反应容器内压强保持不变
D.混合气体的平均摩尔质量不变
(3)PbI2可由Pb3O4和HI反应制备,反应的化学方程式为___________。
(4)常温下PbI2饱和溶液中c(I-)=2.0×10-3mol·L-1,则Ksp(PbI2)=___________;已知Ksp(PbS)=4.0×10-28,则反应PbI2(s)+S2-(aq)![]() PbS(s)+2I-(aq)的平衡常数K=___________。
PbS(s)+2I-(aq)的平衡常数K=___________。
(5)HI的分解反应曲线和液相法制备HI的反应曲线分别如图1和图2所示:

①反应H2(g)+I2(g)![]() 2HI(g)的△H___________(填“>”或“<")0。
2HI(g)的△H___________(填“>”或“<")0。
②将SO2通入碘水中会发生反应:SO2+I2+2H2O===4H++SO42-+2I-,I2+I-![]() I3-。图2中曲线b所代表的微粒是___________(填微粒符号)。
I3-。图2中曲线b所代表的微粒是___________(填微粒符号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】偏二甲肼(C2H8N2)是一种高能燃料,燃烧产生的巨大能量可作为航天运载火箭的推动力.下列叙述正确的是()
A. 偏二甲肼(C2H8N2)的摩尔质量为60g
B. 6.02×1023个偏二甲肼(C2H8N2)分子的质量为60g
C. 1mol偏二甲肼(C2H8N2)的质量为60g/mol
D. 6g偏二甲肼(C2H8N2)含有NA个偏二甲肼(C2H8N2)分子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com