
【题目】为了探究FeSO4和Cu(NO3)2的混合物中各组分的含量,现设计如下流程:
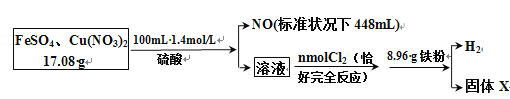
通过计算得出:
(1)原混合物中FeSO4的质量分数约为_______。
(2)通入的 n(Cl2) =________ mol。
(3)生成的H2在标准状况下的体积是________mL。
(4)固体X质量是________g。
【答案】89%0.03522400.56
【解析】
根据题中流程可知,步骤②中加入铁粉产生了氢气,说明前面的酸过量,步骤①中有氯气与亚铁离子反应,说明溶液中有亚铁离子,17.08g的FeSO4和Cu(NO3)2的混合物与0.14mol硫酸混合,由于亚铁离子过量,硝酸根全部被还原为NO,据此计算得硝酸铜的质量及消耗掉的氢离子的物质的量,同时根电子得失守恒可计算出溶液中生成的铁离子的物质的量,根据氯气的物质的量可计算出溶液中亚铁离子的物质的量,并由此计算出溶液中铁离子的总物质的量,根据溶液中的氢离子及8.96g铁粉可计算出氢气的体积和X的值。
(1)根据题中流程可知,步骤②中加入铁粉产生了氢气,说明前面的酸过量,步骤①中有氯气与亚铁离子反应,说明溶液中有亚铁离子,17.08g的FeSO4和Cu(NO3)2的混合物与0.14mol硫酸混合,硝酸根全部被还原为NO,NO的物质的量为![]() mol=0.02mol,根据氮元素守恒,样品中Cu(NO3)2的质量为188g/mol×0.01mol=1.88g,所以FeSO4的质量为17.08g﹣1.88g=15.2g,其物质的量为0.1mol,原混合物中FeSO4的质量分数为
mol=0.02mol,根据氮元素守恒,样品中Cu(NO3)2的质量为188g/mol×0.01mol=1.88g,所以FeSO4的质量为17.08g﹣1.88g=15.2g,其物质的量为0.1mol,原混合物中FeSO4的质量分数为![]() ×100%=89%;
×100%=89%;
(2)根据方程式3Fe2++8H++2NO3﹣(稀)═3Fe3++2NO↑+4H2O
3mol 8mol 2×22.4L
n(Fe2+) n(H+) 448mL
所以n(Fe2+)=0.03mol,n(H+)=0.08mol,则溶液中亚铁离子的物质的量为0.1mol﹣0.03mol=0.07mol,根据方程式2Fe2++Cl2═2Fe3++2Cl﹣,可得氧化亚铁离子需要氯气的物质的量为0.035mol;
(3)根据铁元素守恒,溶液中铁离子的物质的量为0.1mol,根据反应2Fe3++Fe═3Fe2+,可得消耗铁的物质的量为0.05mol即质量为2.8g,溶液中n(H+)=0.14mol×2﹣0.08mol=0.2mol,结合反应2H++Fe═H2↑+Fe2+,生成的氢气为0.1mol,其体积为2.44L=2240mL;
(4)可得消耗铁的物质的量为0.1mol即质量为5.6g,则剩余铁的质量为8.96g﹣5.6g﹣2.8g=0.56g。


 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案科目:高中化学 来源: 题型:
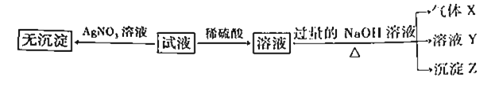
【题目】某试液中只可能含有K+、NH4+、Fe2+、Al3+、Cl﹣、SO42﹣、CO32﹣、AlO2﹣ 中的若干种离子,离子浓度均为 0.1molL﹣1.某同学进行了如下实验:

下列说法正确的是( )
A. 无法确定原试液中是否含有 Al3+、 Cl﹣
B. 滤液 X 中大量存在的阳离子有 NH4+、 Fe2+和 Ba2+
C. 无法确定沉淀 C 的成分
D. 原溶液中存在的离子为 NH4+、 Fe2+、 Cl﹣、 SO42﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用如下装置制取氯气,并用氯气进行实验。回答下列问题:

(1)A中盛有浓盐酸,B中盛有MnO2,写出反应的化学方程式_____________。
(2)D中放入浓H2SO4,其目的是_____________________________。
(3)E中为红色干布条,F中为红色湿布条,可观察到的现象是___________,对比E和F中现象的差异可得出的结论及解释是________________________________。
(4)G处的现象是____________________________________。
(5)画出H处尾气吸收装置图并注明试剂____________。
(6)家庭中常用消毒液(主要成分NaClO)与洁厕灵(主要成分盐酸)清洁卫生。某品牌消毒液包装上说明如下图。

①“与洁厕灵同时使用”会产生有毒的氯气,写出反应的离子方程式__________。
②需“密闭保存”的原因____________________________________________。
(7)现在有一种名为“净水丸”的产品也能对饮用水进行快速的杀菌消毒,药丸通常分内外两层。外层的优氯净Cl2Na(NCO)3先与水反应,生成次氯酸起杀菌消毒作用;几分钟后,内层的亚硫酸钠(Na2SO3)溶出,可将水中的余氯(次氯酸等)除去。亚硫酸钠将水中多余次氯酸除去的离子反应方程式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用图示装置制备KClO溶液,再与KOH、Fe(NO3)3溶液反应制备高效净水剂K2FeO4。

<查阅资料>Cl2与KOH溶液在20℃以下反应生成KClO,在较高温度下则生成KClO3;
K2FeO4易溶于水,微溶于浓KOH溶液,在0℃~5℃的强碱性溶液中较稳定。
(1)仪器a的名称:__________;装置C中三颈瓶置于冰水浴中的目的是_____________。
(2)装置B吸收的气体是__________,装置D的作用是___________________________。
(3)C中得到足量KClO后,将三颈瓶上的导管取下,依次加入KOH溶液、Fe(NO3)3溶液,水浴控制反应温度为25℃,搅拌1.5 h,溶液变为紫红色(含K2FeO4),该反应的离子方程式为________________________。再加入饱和KOH溶液,析出紫黑色晶体,过滤,得到K2FeO4粗产品。
(4)K2FeO4粗产品含有Fe(OH)3、KCl等杂质,其提纯步骤为:
①将一定量的K2FeO4粗产品溶于冷的3 mol/L KOH溶液中。
②过滤。
③________________________________________________________。(补充完整)
④搅拌、静置、过滤,用乙醇洗涤2~3次。
⑤在真空干燥箱中干燥。
(5)称取提纯后的K2FeO4样品0.2200 g于烧杯中,加入强碱性亚铬酸盐溶液,反应后再加稀硫酸调节溶液呈强酸性,配成250 mL溶液,取出25.00 mL放入锥形瓶,用0.01000 mol/L的(NH4)2Fe(SO4)2溶液滴定至终点,重复操作2次,平均消耗(NH4)2Fe(SO4)2溶液30.00 mL。涉及主要反应为:Cr(OH)4-+FeO42- = Fe(OH)3↓+CrO42-+OH-,2CrO42-+2H+![]() Cr2O72-+H2O,Cr2O72-+6Fe2++14H+ = 6Fe3++2Cr3++7H2O,则该K2FeO4样品的纯度为____________。
Cr2O72-+H2O,Cr2O72-+6Fe2++14H+ = 6Fe3++2Cr3++7H2O,则该K2FeO4样品的纯度为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是某学校购买的硫酸试剂标签上的部分内容.据此下列说法正确的是( )

A. 该硫酸的物质的量浓度为1.84mol/L
B. 1mol Zn与足量的该硫酸反应产生2gH2
C. 配制200mL 4.6mol/L的稀硫酸需取该硫酸50mL
D. 该硫酸与等体积的水混合所得溶液的物质的量浓度等于9.2mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用电子式表示下列离子化合物的形成过程:
BaCl2_____________________________;
NaF__________________________________;
MgS________________________________;
K2O_________________________________。
(学法题)请归纳物质电子式的书写及用电子式表示化合物的形成过程应注意哪些问题(至少两点)_______、__________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
Ⅰ.形式一:(由粒子数推断)![]() 、
、![]() 、
、![]() 、D、E 5种粒子(分子或离子),它们分别含10个电子,已知它们有如下转化关系:①
、D、E 5种粒子(分子或离子),它们分别含10个电子,已知它们有如下转化关系:①![]() ;②
;②![]() 。据此,回答下列问题:写出
。据此,回答下列问题:写出![]() 、
、![]() 的化学式:____、______、
的化学式:____、______、
Ⅱ. 形式二:(由元素原子结构推断)A、B、C、D、E、F的原子序数依次增大,它们都是同周期的元素。已知:A、C、F 三种原子最外层共有11个电子,且这三种元素的最高价氧化物的水化物之间两两皆能反应,均生成盐和水;D元素原子的最外层电子数比次外层电子数少4;E元素原子次外层电子数比最外层电子数多2。
(1)写出下列元素的符号:A________,B________,E________
(2)F在元素周期表中的位置为___________________________________
(3)写出C的单质和A的最高价氧化物的水化物反应的离子方程式_______
(4)元素的非金属性为(原子的得电子能力):E________F(填“强于”或“弱于”),请以E、F为例列举元素非金属性强弱的比较方法__________________________________________________(至少2条)
通过Ⅱ的解题你认为推断出本题各元素的关键环节为___________
III.形式三:(由元素位置推断)下表为元素周期表的一部分:
族 周期 | ||||||||
1 | ① | |||||||
2 | ② | |||||||
3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
(1)请画出元素⑦的离子结构示意图________________。
(2)写出元素⑤在周期表中的位置______________。
(3)②、③、⑥的离子半径由大到小的顺序为_________________________。
(4)⑤、⑥、⑦的最高价氧化物对应水化物酸性由强到弱的顺序是______。
(5)①、②、③三种元素可形成既含离子键又含极性共价键的化合物,写出该化合物的电子式:____________________。该化合物与④的最高价氧化物反应的离子方程式为____________________。
(6)请你预测:如果发现了原子序数为116号元素,它在周期表中的位置是第________周期_______族,它属于_____元素(填“金属”或“非金属”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某强酸性无色溶液中可能含下表中的若干种离子。
阳离子 | Mg2+、NH4+、Ba2+、Al3+、Fe2+ |
阴离子 | SiO32-、MnO4-、Cl-、NO3-、SO32-、 |
实验Ⅰ:取少量该试液进行如下实验。
实验Ⅱ:为了进一步确定该溶液的组成,取100mL原溶液,向该溶液中滴加1mol·L-1的NaOH溶液,产生沉淀的质量与氢氧化钠溶液体积的关系如图所示。

回答下列问题:
(1)不进行实验就可以推断出,上表中的离子一定不存在的有____________种。
(2)通过实验Ⅰ可以确定该溶液中一定存在的阴离子是________________。
(3)写出实验Ⅱ的图像中BC段对应的离子方程式:_______________________________________________________________。
(4)A点对应的固体质量为____________g。
(5)该溶液中阴离子的浓度为____________mol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com