
����Ŀ��������ʯ(Fe2O3)Ϊ��ʼ�����һϵ�з�Ӧ���Եõ�Fe3[Fe(CN)6]2��Fe(SCN)3����ش��������⣺
(1)д��Fe��ԭ�ӽṹʾ��ͼ_____________________��Oԭ�Ӻ�����ӹ����ʾʽΪ______��
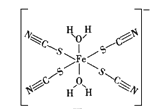
(2)KSCN�Ǽ���Fe3+���Լ�֮һ����SCN-��Ϊ�ȵ������һ�ַ���Ϊ__________����ͼ��SCN��Fe3+�γɵ�һ�������ӣ��������������е���λ��(�Լ�ͷ��ʾ)_______��
(3)K3[Fe(CN)6]������Fe3+��CN֮��ļ���Ϊ__________���û�ѧ���ܹ��γɵ�ԭ����_______��
(4)K3[Fe(CN)5NO]�����Ԫ���У����ڵڶ����ڵ�Ԫ�صĵ�һ��������С�����˳����_____���������ԭ��������С��Ԫ������Ԫ���γɵ���Է�������Ϊ92�ķ��㻯�����У�����ԭ�ӵ��ӻ����������_________��
(5)������ͨ���Ѫ��(K4[Fe(CN)6])��Һ�У��õ���Ѫ��(K3[Fe(CN)6])��д���ñ仯�Ļ�ѧ����ʽ______��
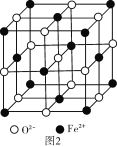
(6)FeO�����ṹ��ͼ2��ʾ��FeO������Fe2+��λ��Ϊ____�����þ����߳�Ϊacm����þ����ܶ�Ϊ___g/cm3(����٤��������ֵΪNA)��
���𰸡�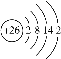
![]() CO2��N2O��CS2��COS
CO2��N2O��CS2��COS 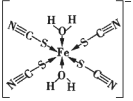 ��λ�� CN���ṩ�¶Ե��ӣ�Fe3+�ܽ��ܹ¶Ե���(��Fe3+�пչ��) C��O��N sp2��sp3�ӻ� 2K4[Fe(CN)6]+Cl2=2K3[Fe(CN)6]+2KCl 6
��λ�� CN���ṩ�¶Ե��ӣ�Fe3+�ܽ��ܹ¶Ե���(��Fe3+�пչ��) C��O��N sp2��sp3�ӻ� 2K4[Fe(CN)6]+Cl2=2K3[Fe(CN)6]+2KCl 6 ![]()
��������
(1)Fe��26��Ԫ�أ����ݺ�������Ų��ɵ���ԭ�ӽṹʾ��ͼ��O��8��Ԫ�أ�����ԭ�Ӻ���������˳����������ĵ������ɵ�����ӹ����ʾʽ��
(2)ԭ�Ӹ�������Ҽ۵�������ȵķ��ӻ�����Ϊ�ȵ����壻��λ����һ��ԭ�ӵ������ṩ���Ӷ�������һ��ԭ�ӹ��õĹ��ۼ���
(3)������ԭ���пչ���������Ӻ��й¶Ե���ʱ�����γ���λ����
(4)�������ͬ����Ԫ��ΪC��N��O�����ݵ�һ�����ܵݱ�����жϣ����������ԭ��������С��Ԫ����C��C����Ԫ���γɵ���Է�������Ϊ92�ķ��㻯�������ʽ��C7H8���ṹ��ʽΪ![]() �������γɵĿռ乹�ͺͷ��ӽṹ�ж��ӻ����ͣ�
�������γɵĿռ乹�ͺͷ��ӽṹ�ж��ӻ����ͣ�
(5)������+2�۵���������+3�۵��������ݵ��ӵ�ʧ�غ���д��ѧ����ʽ��
(6) ����������Ϊ���ģ���X��Y��Z��������и�Ӷ�ȷ������������λ�����þ����ܶ���=![]() ���㡣
���㡣
(1) Fe��26��Ԫ�أ����ݺ�������Ų����ɣ��ɵ���ԭ�ӽṹʾ��ͼΪ��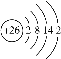 ��O��8��Ԫ�أ����ݹ���ԭ����֪O�Ĺ����ʾʽ�ǣ�
��O��8��Ԫ�أ����ݹ���ԭ����֪O�Ĺ����ʾʽ�ǣ�![]() ��
��
(2)SCN-�к���3��ԭ�ӣ�����۵�������16����SCN-��Ϊ�ȵ������һ�ַ���ΪCO2��N2O��CS2��COS�ȣ�����SCN��Fe3+�γɵ�һ�������ӵĽṹʾ��ͼ��֪��Fe3+���������ӣ�SCN-��H2O����λ�壬Fe3+����λ����6��Fe3+��SCN-��Sԭ��֮�估Fe3+��H2O��Oԭ��֮���γ���λ��������������ʾ��λ��Ϊ ��
��
(3) K3[Fe(CN)6]������Fe3+��CN-֮��Ļ�ѧ������Ϊ��λ����Fe3+�пչ�����ܽ��ܹ¶Ե��ӣ�CN-���ṩ�¶Ե��ӣ��������γ���λ����
(4)�������ͬ���ڵڶ�����Ԫ��ΪC��N��O����һ�����ܴ����ң����������ƣ���C��С��Nԭ��2p����������Ϊ�ȶ�����һ�����ܸ���O���ڶ����ڵ�Ԫ�صĵ�һ��������С�����˳����C��O��N���������ԭ��������С��Ԫ��ΪCԪ�أ�Cԭ���γ�8�����ȶ��ṹ���γɵ���Է���������92�ķ����廯�����Ǽױ���������̼ԭ����sp2�ӻ�����Ϊsp3�ӻ����ʼױ���Cԭ�ӵ��ӻ���ʽ��sp2��sp3�ӻ���
(5)������+2�۵���������+3�۵��������Է�Ӧ����ʽΪ��2K4[Fe(CN)6]+Cl2=2K3[Fe(CN)6]+2KCl��
(6)����������Ϊ���ģ���X��Y��Z��������и���ͼƬ֪������������λ��Ϊ6���þ������������Ӹ���=8��![]() +6��
+6��![]() =4��O2-���ӵĸ�����12��
=4��O2-���ӵĸ�����12��![]() +1=4�����ڸþ�����ܶ�����=
+1=4�����ڸþ�����ܶ�����= g/cm3��
g/cm3��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ĵ�����(HN3)��һ�����ᣬ��������25mL 0.1 mol/L NaOH��Һ�м���0.2 mol/L HN3��Һ���μӹ����е�pHֵ�ı仯����(��Һ���ʱ������仯���Բ���)����ͼ������˵����ȷ���ǣ� ��
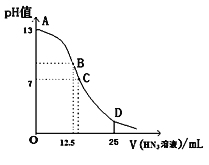
A. �õζ�������Ӧ�ü�����ָʾ��
B. ��B��pH=8����c(HN3)=(10-6��10-8 )mol/L
C. ��D��Ӧ��Һ�д��ڹ�ϵ��c(HN3)>c(Na+)>c(N3-)
D. ������A��B��C�Ĺ����У���ˮ���������c(OH-)����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�������£���1mol��CO��1molˮ����ͨ�������з���������Ӧ��
CO��H2O![]() CO2��H2���ﵽƽ����CO2Ϊ0.6mol����ͨ��0.4molˮ�������ִﵽƽ���CO2�����ʵ���Ϊ
CO2��H2���ﵽƽ����CO2Ϊ0.6mol����ͨ��0.4molˮ�������ִﵽƽ���CO2�����ʵ���Ϊ
A. ����0.6mol B. ����1mol
C. ����0.6mol����1mol D. ����1mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ⱦ��NOͨ���ú�Ce4+����Һ���գ�����HNO2��NO3-�������õ�ⷨ����������Һ�е�HNO2ת��Ϊ�����ʣ�ͬʱ����Ce4+����ԭ����ͼ��ʾ������˵����ȷ����

A. H+�����ҽ�������
B. Ce4+�ӵ��۵�c���������ҿ�ѭ��ʹ��
C. �����ĵ缫��Ӧʽ��2HNO2+6H++6e��===N2��+4H2O
D. ���ü���ȼ�ϵ����Ϊ��Դ�������ı�״����33.6 L����ʱ�������Ͽ�ת��2mol HNO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����![]() ���Ȼ���XCl2 0.95g�����Һ������1mol/L����������Һ20mL���ܰ���������ȫ�����������Լ��㣺
���Ȼ���XCl2 0.95g�����Һ������1mol/L����������Һ20mL���ܰ���������ȫ�����������Լ��㣺
(1)X��������Ϊ_________��
(2)��X�ĺ���������Ϊ12����47.5gXCl2���������ӵ����ʵ�����________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1����������ֱ����ȡ�����ƣ��������ǣ�___________________��
��2��������ʾ�����Ż�ʱ����CO2���ΪѰ��ԭ���������̽��ʵ�飺A����ȼ�ճ��е�����ȼ��Ѹ������ʢ��CO2�ļ���ƿ�С����Կ����������ɫ�������������̣�����Ϩ�����ƿ�ײ��к�ɫ���壬ƿ���ϸ��Ű�ɫ���壻B������ƿ�м�����������ˮ�������ˣ���ֽ�����º�ɫ���壬��ҺΪ��ɫ��C��ȡ������Һ������֧�Թ��У����һ֧�Թ��еμ�һ�η�̪��Һ����Һ��죬��ڶ�֧�Թ��еμӳ���ʯ��ˮ����Һ����ǡ�д��ʵ��C�г���ʯ��ˮ����ǵĻ�ѧ����ʽ��____________����������ʵ����ʵ�ж�ʵ��B�е���ɫ��Һ��________������ԡ��������ԡ����ߡ����ԡ�������������ʵ����ʵд�������ڵ�ȼ��������CO2��Ӧ��ѧ����ʽ��_______________��
��3���ý�ͷ�ιܽ����Ƶı�����ˮ�������뺬�з�̪����������ϡ��Һ�У����ε�һ����ʱ����ɫͻȻ��ȥ���Իش��������⣬�������������ԭ�ٿ�������ˮ�����ԣ�������������Һ�к�ʹ��Һ��ɫ����Ҳ������_________����Ƴ�һ������֤����ɫ��ȥ��ԭ���Ǣٻ��_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
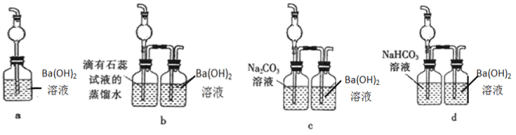
����Ŀ����ͼ��һ��ʵ������ȡ������������Ϊԭ�Ͻ���һϵ�з�Ӧ��װ�ã��ش��������⡣����֪����MnO2+4HCl(Ũ) ![]() MnCl2+2H2O+Cl2��,��Cl2+SO2+2H2O��2HCl+H2SO4,�� Ba(OH)2+CO2��BaCO3��+H2O��
MnCl2+2H2O+Cl2��,��Cl2+SO2+2H2O��2HCl+H2SO4,�� Ba(OH)2+CO2��BaCO3��+H2O��

��1���a����������___��
��2��װ��D������ɫ���������ԭ��___________��
��3��Eװ�õ�Ӳ�ʲ�������ʢ��̼�ۣ�����������ԭ��Ӧ�������ΪCO2��HCl����д��E�з�Ӧ�Ļ�ѧ����ʽ_______��
��4��F�����ձ���Һ������___����С���û�С�����ɫ������
��5��Fװ����ȷ��E����Ӧ����CO2������Ϊ��֤��CO2�Ĵ��ڣ�Ҫ��Fװ�ý��и��죬����װ�÷���Ҫ�����___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)��ʵ֤��������Ƴ�ԭ��صķ�Ӧͨ���Ƿ��ȷ�Ӧ�����л�ѧ��Ӧ�������Ͽ�����Ƴ�ԭ��ص���__________��
A��C(s)+H2O(g)=CO(g)+H2(g) ��H>0
B��2H2(g)+O2(g)=2H2O(1) ��H<0
C��NaOH(aq)+HC1(aq)=NaC1(aq)+H2O(1) ��H<0
(2) ��KOH��ҺΪ�������Һ�������⣨1����ѡ��Ӧ���һ��ԭ��أ��为���ĵ缫��ӦʽΪ_______��

(3) ���ԭ���ڻ�ѧ��ҵ�����Ź㷺��Ӧ�á��ֽ�����Ƶ�ԭ���ͨ����������ͼ�е�������������aΪ���Һ��X��Y��Ϊ���Ե缫����
����aΪCuSO4��Һ������ʱ�Ļ�ѧ��Ӧ����ʽΪ___________________��
������⺬��0.04molCuSO4��0.04molNaCl�Ļ����Һ400ml������������������672 mL����״���£�ʱ����Һ��c��H+�� = _____�����������Һ������䣩��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Կ��淴Ӧ4NH3��g��+ 5O2��g��![]() 4NO��g��+ 6H2O��g��������������ȷ����
4NO��g��+ 6H2O��g��������������ȷ����
A. �ﵽ��ѧƽ��ʱ��4������O2��= 5������NO��
B. ����λʱ��������x mol NO��ͬʱ������x mol NH3 ����Ӧ�ﵽƽ��״̬
C. �ﵽ��ѧƽ��ʱ�����������������������Ӧ���ʼ��٣��淴Ӧ��������
D. ��ѧ��Ӧ���ʹ�ϵ�ǣ�2������NH3��= 3������H2O��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com