
ΓΨΧβΡΩΓΩ““θΘΥ°―νΥα(ΑΔΥΨΤΞΝ÷) «ΡΩ«Α≥Θ”Ο“©Έο÷°“ΜΓΘ Β―ι “Ά®ΙΐΥ°―νΥαΫχ––““θΘΜ·÷Τ±ΗΑΔΥΨΤΞΝ÷ΒΡ“Μ÷÷ΖΫΖ®»γœ¬ΘΚ
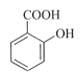 +(CH3CO)2O
+(CH3CO)2O![]()
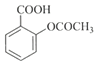 +CH3COOH
+CH3COOH
Υ°―νΥα Υατϊ ““θΘΥ°―νΥα
Υ°―νΥα | ¥ΉΥατϊ | ““θΘΥ°―νΥα | |
»έΒψ/Γφ | 157~159 | -72~74 | 135~138 |
œύΕ‘ΟήΕ»/(g/cm3) | 1.44 | 1.10 | 1.35 |
œύΕ‘Ζ÷Ή”÷ ΝΩ | 138 | 102 | 180 |
Β―ιΙΐ≥ΧΘΚ‘Ύ100 mLΉΕ–ΈΤΩ÷–Φ”»κΥ°―νΥα6.9 gΦΑ¥ΉΥατϊ10 mLΘ§≥δΖ÷“ΓΕ· ΙΙΧΧεΆξ»Ϊ»ήΫβΓΘΜΚ¬ΐΒΈΦ”0.5 mL≈®ΝρΥαΚσΦ”»»Θ§Έ§≥÷ΤΩΡΎΈ¬Ε»‘Ύ70ΓφΉσ”“Θ§≥δΖ÷Ζ¥”ΠΓΘ…‘άδΚσΫχ––»γœ¬≤ΌΉςΘΚ
ΔΌ‘Ύ≤ΜΕœΫΝΑηœ¬ΫΪΖ¥”ΠΚσΒΡΜλΚœΈοΒΙ»κ100 mLάδΥ°÷–Θ§Έω≥ωΙΧΧεΘ§Ιΐ¬ΥΓΘ
ΔΎΥυΒΟΫαΨߥ÷ΤΖΦ”»κ50 mL±ΞΚΆΧΦΥα«βΡΤ»ή“ΚΘ§»ήΫβΓΔΙΐ¬ΥΓΘ
Δέ¬Υ“Κ”Ο≈®―ΈΥαΥαΜ·Κσά以ΓΔΙΐ¬ΥΒΟΙΧΧεΓΘ
ΔήΙΧΧεΨ≠¥ΩΜ·ΒΟΑΉ…ΪΒΡ““θΘΥ°―νΥαΨßΧε5.4 gΓΘ
ΜΊ¥πœ¬Ν–Έ ΧβΘΚ
(1)ΗΟΚœ≥…Ζ¥”Π÷–ΉνΚΟ≤…”Ο__________Φ”»»(Χν±ξΚ≈)ΓΘ
A. ΨΤΨΪΒΤ B.»»Υ°‘Γ C.ΟΚΤχΒΤ D.Βγ¬·
(2)œ¬Ν–≤ΘΝß“«Τς÷–Θ§ΔΌ÷––η Ι”ΟΒΡ”–________(Χν±ξΚ≈)ΓΘ
(3)ΔΌ÷––η Ι”ΟάδΥ°Θ§ΡΩΒΡ «_________________________ΓΘ
(4)ΔΎ÷–ΒΡ÷ς“ΣΜ·―ßΖ¥”ΠΖΫ≥Χ Ϋ «ΘΚ____________________ΓΘ
(5)Δή≤…”ΟΒΡ¥ΩΜ·ΖΫΖ®ΈΣ____________ΓΘ
(6)±Ψ Β―ιΒΡ≤ζ¬ ΈΣ_________%ΓΘ
ΓΨ¥πΑΗΓΩB BD Ι≤ζΈο≥δΖ÷Έω≥ωΘ§ΧαΗΏ≤ζ¬ ![]() +NaHCO3
+NaHCO3![]()
![]() +CO2Γϋ+H2O ÷ΊΫαΨß 60
+CO2Γϋ+H2O ÷ΊΫαΨß 60
ΓΨΫβΈωΓΩ
(1)ΒΆ”Ύ100ΓφΒΡΦ”»»–η“ΣΥ°‘ΓΦ”»»ΘΜ
(2)ΔΌ÷–≤ΌΉςΈΣΙΐ¬ΥΘ§–η“ΣΒΡ≤ΘΝß“«Τς”–≤ΘΝßΑτΓΔΤ’Ά®¬©ΕΖΓΔ…’±≠ΘΜ
(3)““θΘΥ°―νΥα‘Ύ≥ΘΈ¬œ¬ «ΙΧΧεΘ§«“‘ΎάδΥ°÷–»ήΫβΕ»Ϋœ–ΓΘΜ
(4)±ΞΚΆΧΦΥα«βΡΤ”κ““θΘΥ°―νΥαΖΔ…ζΗ¥Ζ÷ΫβΖ¥”ΠΖ≈≥ωCO2ΤχΧεΘΜ
(5)ΙΧΧεΨ≠¥ΩΜ·ΖΫΖ®ΈΣ÷ΊΫαΨßΘΜ
(6)œ»ΗυΨί“―÷ΣΝΩΦΤΥψ¥ΉΥατϊΓΔΥ°―νΥαΒΡΈο÷ ΒΡΝΩΘ§ΫαΚœΖ¥”Π÷–Έο÷ œϊΚΡΙΊœΒΘ§≈–Εœ ≤Ο¥Έο÷ ΙΐΝΩΘ§‘Ό“‘≤ΜΉψΝΩΒΡΈο÷ ΈΣ±ξΉΦΦΤΥψΖ¥”Π≤ζ…ζΒΡ““θΘΥ°―νΥαΒΡ÷ ΝΩΘ§ΉνΚσΗυΨί
≤ζ¬ =![]() ΓΝ100%Ϋχ––ΦΤΥψΓΘ
ΓΝ100%Ϋχ––ΦΤΥψΓΘ
(1)ΒΆ”Ύ100ΓφΒΡΦ”»»–η“ΣΥ°‘ΓΦ”»»Θ§ΗΟΚœ≥…Έ¬Ε»ΈΣ70ΓφΉσ”“Θ§Υυ“‘ΗΟΚœ≥…Ζ¥”Π÷–”Π≤…”Ο»»Υ°‘ΓΘ§AΓΔCΓΔDΦ”»»Έ¬Ε»ΕΦΗΏ”Ύ100ΓφΘ§Ι Κœάμ―Γœν «BΘΜ
(2)ΔΌ÷–≤ΌΉςΈΣΖ÷άκΡ―»ή–‘ΒΡΙΧΧε”κ“ΚΧεΜλΚœΈοΒΡΖΫΖ®Θ§ΗΟ≤ΌΉς «Ιΐ¬ΥΘ§Ιΐ¬Υ–η“ΣΒΡ≤ΘΝß“«Τς”–≤ΘΝßΑτΓΔΤ’Ά®¬©ΕΖΓΔ…’±≠Θ§ΆΦ Ψ“«ΤςA «Ζ÷“Κ¬©ΕΖΘ§B «…’±≠Θ§C «»ίΝΩΤΩΘ§D «Τ’Ά®¬©ΕΖΘ§Υυ“‘―Γ»ΓBD“«ΤςΘ§Κœάμ―Γœν «BDΘΜ
(3)““θΘΥ°―νΥα‘Ύ≥ΘΈ¬œ¬ «ΙΧΧεΘ§«“‘ΎάδΥ°÷–»ήΫβΕ»Ϋœ–ΓΘ§ΈΣΝΥΫΒΒΆΤδ»ήΫβΕ»≤Δ≥δΖ÷Έω≥ω““θΘΥ°―νΥαΙΧΧε(ΫαΨß)Θ§Υυ“‘ΔΌ÷––η Ι”ΟάδΥ°Θ§Φ¥ΔΌ÷– Ι”ΟάδΥ°Θ§ΡΩΒΡ «≥δΖ÷Έω≥ω““θΘΥ°―νΥαΙΧΧεΘΜ
(4)”…”Ύτ»ΥαΒΡΥα–‘±»ΧΦΥα«ΩΘ§Υυ“‘ΧΦΥα«βΡΤ”κ““θΘΥ°―νΥαΖΔ…ζΗ¥Ζ÷ΫβΖ¥”ΠΖ≈≥ωCO2ΓΔH2OΘ§Ά§ ±ΒΟΒΫ““θΘΥ°―νΥαΡΤ―ΈΘ§ΗΟΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΈΣΘΚ![]() +NaHCO3
+NaHCO3![]()
![]() +CO2Γϋ+H2OΘΜ
+CO2Γϋ+H2OΘΜ
(5)ΙΧΧεΨ≠¥ΩΜ· ±Ω…ΗυΨίΈο÷ ΒΡ»ήΫβΕ» ήΈ¬Ε»ΒΡ”Αœλ±δΜ·Ϋœ¥σΘ§Εχ‘”÷ »ήΫβΕ» ήΈ¬Ε»ΒΡ”Αœλ±δΜ·≤Μ¥σΘ§œ»≈δ÷Τ≥…ΗΏΈ¬œ¬±ΞΚΆ»ή“ΚΘ§»ΜΚσΫΒΈ¬ΫαΨßΘ§ΫΪΈω≥ωΒΡΨßΧε‘Ό»ήΫβ‘Ύ“ΜΕ®ΒΡ’τΝσΥ°÷–ΒΟΒΫΤδΗΏΈ¬œ¬±ΞΚΆ»ή“ΚΘ§‘ΌΫΒΈ¬ΫαΨßΘ§’β÷÷ΖΫΖ®ΈΣ÷ΊΫαΨßΘ§Υυ“‘Δή≤…”ΟΒΡ¥ΩΜ·ΖΫΖ®ΈΣ÷ΊΫαΨßΘΜ
(6)¥ΉΥατϊ÷ ΝΩm[(CH3CO)2O]=10 mLΓΝ1.10 g/mL=11 gΘ§ΤδΈο÷ ΒΡΝΩ «n[(CH3CO)2O]=![]() =0.108 molΘ§6.9 gΥ°―νΥαΒΡΈο÷ ΒΡΝΩ «n(Υ°―νΥα)=
=0.108 molΘ§6.9 gΥ°―νΥαΒΡΈο÷ ΒΡΝΩ «n(Υ°―νΥα)=![]() =0.05 molΘ§”…”ΎΕΰ’ΏΖ¥”Π ±ΒΡΈο÷ ΒΡΝΩΒΡ±» «1ΘΚ1Θ§Υυ“‘¥ΉΥατϊΙΐΝΩΘ§“Σ“‘≤ΜΉψΝΩΒΡΥ°―νΥαΈΣ±ξΉΦΦΤΥψΖ¥”Π≤ζ…ζΒΡ““θΘΥ°―νΥαΘ§‘ράμ¬έ…œ…ζ≥…““θΘΥ°―νΥαΒΡΈο÷ ΒΡΝΩ «0.05 molΘ§Τδ÷ ΝΩm(““θΘΥ°―νΥα)=0.05 molΓΝ180 g/mol=9.0 gΘ§Υυ“‘““θΘΥ°―νΥαΒΡ≤ζ¬ ΈΣΘΚ
=0.05 molΘ§”…”ΎΕΰ’ΏΖ¥”Π ±ΒΡΈο÷ ΒΡΝΩΒΡ±» «1ΘΚ1Θ§Υυ“‘¥ΉΥατϊΙΐΝΩΘ§“Σ“‘≤ΜΉψΝΩΒΡΥ°―νΥαΈΣ±ξΉΦΦΤΥψΖ¥”Π≤ζ…ζΒΡ““θΘΥ°―νΥαΘ§‘ράμ¬έ…œ…ζ≥…““θΘΥ°―νΥαΒΡΈο÷ ΒΡΝΩ «0.05 molΘ§Τδ÷ ΝΩm(““θΘΥ°―νΥα)=0.05 molΓΝ180 g/mol=9.0 gΘ§Υυ“‘““θΘΥ°―νΥαΒΡ≤ζ¬ ΈΣΘΚ![]() ΓΝ100%=60%ΓΘ
ΓΝ100%=60%ΓΘ


 ΩΎΥψΧβΩ®Φ””Π”ΟΧβΦ·―ΒœΒΝ–¥πΑΗ
ΩΎΥψΧβΩ®Φ””Π”ΟΧβΦ·―ΒœΒΝ–¥πΑΗ ΉέΚœΉ‘≤βœΒΝ–¥πΑΗ
ΉέΚœΉ‘≤βœΒΝ–¥πΑΗ
| ΡξΦΕ | ΗΏ÷–ΩΈ≥Χ | ΡξΦΕ | ≥θ÷–ΩΈ≥Χ |
| ΗΏ“Μ | ΗΏ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ“Μ | ≥θ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏΕΰ | ΗΏΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θΕΰ | ≥θΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏ»ΐ | ΗΏ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ»ΐ | ≥θ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–ΗυΨί Β―ι≤ΌΉςΚΆœ÷œσΥυΒΟ≥ωΒΡΫα¬έ¥μΈσΒΡ «
―Γœν | Β―ι≤ΌΉς | Β―ιœ÷œσ | Ϋα¬έ |
A | œρ»ή“ΚX÷–œ»ΒΈΦ”œΓœθΥαΘ§‘ΌΒΈΦ”Ba(NO3)2»ή“Κ | ≥ωœ÷ΑΉ…Ϊ≥ΝΒμ | »ή“ΚX≤Μ“ΜΕ®Κ§”–SO42Θ≠ |
B | œρFeCl3ΘΪ3KSCN | ΧεœΒ―’…ΪΈό±δΜ· | KCl≤ΜΡή ΙΗΟΤΫΚβ“ΤΕ· |
C | œρ≈®Ε»ΨυΈΣ0.1molΓΛLΘ≠1NaOHΚΆNaIΜλΚœ»ή“Κ÷–ΒΈΦ”…ΌΝΩAgNO3»ή“Κ | ≥ωœ÷ΜΤ…Ϊ≥ΝΒμ | Ksp(AgCl)>Ksp(AgI) |
D | œρΝΫΖίΒΑΑΉ÷ »ή“Κ÷–Ζ÷±πΒΈΦ”±ΞΚΆNaCl»ή“ΚΚΆCuSO4»ή“Κ | Ψυ”–ΙΧΧεΈω≥ω | ΒΑΑΉ÷ ΨυΖΔ…ζ±δ–‘ |
A.AB.BC.CD.D
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ‘Ύa L Al2(SO4)3ΚΆ(NH4)2SO4ΒΡΜλΚœ»ή“Κ÷–Φ”»κb mol BaCl2Θ§«ΓΚΟ Ι»ή“Κ÷–ΒΡSO42-Άξ»Ϊ≥ΝΒμΘΜ»γΦ”»κΉψΝΩ«ΩΦν≤ΔΦ”»»Ω…ΒΟΒΫc mol NH3Θ§‘ρ‘≠»ή“Κ÷–Al3ΘΪΒΡ≈®Ε»(mol/L)ΈΣ
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΗΜ¬μΥαΘ®Ζ¥ ΫΕΓœ©ΕΰΥαΘ©”κFe2+–Έ≥…ΒΡ≈δΚœΈοΓΣΓΣΗΜ¬μΥαΧζ”÷≥ΤΓΑΗΜ―ΣΧζΓ±Θ§Ω…”Ο”Ύ÷ΈΝΤ»±Χζ–‘ΤΕ―ΣΓΘ“‘œ¬ «Κœ≥…ΗΜ¬μΥαΧζΒΡ“Μ÷÷ΙΛ“’¬ΖœΏΘΚ
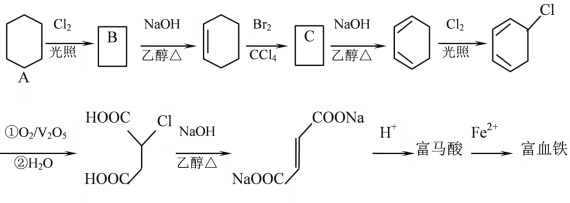
ΜΊ¥πœ¬Ν–Έ ΧβΘΚ
Θ®1Θ©AΒΡΜ·―ßΟϊ≥ΤΈΣΘΚ_________________Θ§”…A…ζ≥…BΒΡΖ¥”Πάύ–ΆΈΣΘΚ___________
Θ®2Θ©CΒΡΫαΙΙΦρ ΫΈΣΘΚ______________Θ§Φ”»» ±Θ§C”κNaOHΒΡ““¥Φ»ή“ΚΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΈΣΘΚ___________
Θ®3Θ©ΗΜ¬μΥαΒΡΫαΙΙΦρ ΫΈΣΘΚ___________
Θ®4Θ©Φλ―ιΗΜ―ΣΧζ÷– «ΖώΚ§”–Fe3+ΒΡ Β―ι≤ΌΉς≤Ϋ÷η «ΘΚ___________
Θ®5Θ©ΗΜ¬μΥαΈΣΕΰ‘Στ»ΥαΘ§1molΗΜ¬μΥα”κΉψΝΩ±ΞΚΆNaHCO3»ή“ΚΖ¥”ΠΩ…Ζ≈≥ω_______L CO2Θ®±ξΩωΘ©ΘΜΗΜ¬μΥαΒΡΆ§Ζ÷“λΙΙΧε÷–Θ§Ά§ΈΣΕΰ‘Στ»ΥαΒΡΜΙ”–Θ®–¥≥ωΫαΙΙΦρ ΫΘ©ΘΚ___________ΓΔ___________ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν––π ω’ΐ»ΖΒΡ «( )
A.ΕΓ¥ΦΒΡΆ§Ζ÷“λΙΙΧε![]() ≤ΜΚ§ΝΔΧε“λΙΙ
≤ΜΚ§ΝΔΧε“λΙΙ![]() ”–7÷÷
”–7÷÷
B.ΟόΓΔΥΩΓΔΥήΝœΦΑΚœ≥…œπΫΚΆξ»Ϊ»Φ…’ΕΦ÷Μ…ζ≥…CO2ΚΆH2O
C.C6H5Li+CO2ΓζC6H5COOLiΦ»≤Μ τ”ΎΦ”≥…Ζ¥”Π“≤≤Μ τ”Ύ»Γ¥ζΖ¥”Π
D.““œ©Ρή ΙδεΥ°Ά …ΪΓΔ““¥ΦΡή ΙΥα–‘KMnO4»ή“ΚΆ …ΪΘ§ΖΔ…ζΒΡΖ¥”Πάύ–ΆœύΆ§
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–ΙΊ”Ύ≥ΘΦϊ”–ΜζΈοΒΡΥΒΖ®÷–’ΐ»ΖΒΡ «Θ® Θ©
![]() ΟόΜ®ΓΔ≤œΥΩΚΆΨέ““œ©ΒΡ÷ς“Σ≥…Ζ÷ΕΦ «œΥΈ§ΥΊ
ΟόΜ®ΓΔ≤œΥΩΚΆΨέ““œ©ΒΡ÷ς“Σ≥…Ζ÷ΕΦ «œΥΈ§ΥΊ
![]() ΦΉΆιΓΔ““¥ΦΚΆ““Υα‘Ύ“ΜΕ®ΧθΦΰœ¬ΕΦΡήΖΔ…ζ»Γ¥ζΖ¥”Π
ΦΉΆιΓΔ““¥ΦΚΆ““Υα‘Ύ“ΜΕ®ΧθΦΰœ¬ΕΦΡήΖΔ…ζ»Γ¥ζΖ¥”Π
![]() Β»÷ ΝΩΒΡ““ΆιΓΔ““œ©ΓΔ±Ϋ≥δΖ÷»Φ…’Θ§œϊΚΡ―θΤχΒΡΝΩ”…ΕύΒΫ…Ό
Β»÷ ΝΩΒΡ““ΆιΓΔ““œ©ΓΔ±Ϋ≥δΖ÷»Φ…’Θ§œϊΚΡ―θΤχΒΡΝΩ”…ΕύΒΫ…Ό
![]() ≥ΐ»Ξ““Υα““θΞ÷–≤–ΝτΒΡ““ΥαΘ§Φ”ΙΐΝΩ±ΞΚΆNa2CO3»ή“Κ’ώΒ¥ΚσΘ§Ψ≤÷ΟΖ÷“Κ
≥ΐ»Ξ““Υα““θΞ÷–≤–ΝτΒΡ““ΥαΘ§Φ”ΙΐΝΩ±ΞΚΆNa2CO3»ή“Κ’ώΒ¥ΚσΘ§Ψ≤÷ΟΖ÷“Κ
![]() ±ΫΖ÷Ή”÷–Κ§”–ΧΦΧΦΥΪΦϋΚΆΒΞΦϋΘ§Φ»ΡήΖΔ…ζΦ”≥…Ζ¥”ΠΘ§“≤ΡήΖΔ…ζ»Γ¥ζΖ¥”Π
±ΫΖ÷Ή”÷–Κ§”–ΧΦΧΦΥΪΦϋΚΆΒΞΦϋΘ§Φ»ΡήΖΔ…ζΦ”≥…Ζ¥”ΠΘ§“≤ΡήΖΔ…ζ»Γ¥ζΖ¥”Π
![]() ·”ΆΖ÷ΝσΚΆΟΚΒΡΗ…Νσ τ”ΎΈοάμ±δΜ·Θ§ ·”ΆΒΡΝ―Μ·ΓΔΝ―ΫβΕΦ τ”ΎΜ·―ß±δΜ·
·”ΆΖ÷ΝσΚΆΟΚΒΡΗ…Νσ τ”ΎΈοάμ±δΜ·Θ§ ·”ΆΒΡΝ―Μ·ΓΔΝ―ΫβΕΦ τ”ΎΜ·―ß±δΜ·
A.ΔΌΔίΔόB.ΔΎΔέΔήC.ΔΌΔΎΔέD.ΔΎΔήΔί
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ“ΜΑψΝρΖέΚ§”–SΘ®ΒΞ–±Θ©ΚΆSΘ®’ΐΫΜΘ©ΝΫ÷÷Ά§ΥΊ“λ–ΈΧεΓΘ“―÷Σ≥ΘΈ¬œ¬ΘΚ
ΔΌSΘ®ΒΞ–±Θ©ΘΪO2Θ®gΘ© =SO2Θ®gΘ© ΠΛHΘΫΘ≠297.16 kJ/mol
ΔΎSΘ®’ΐΫΜΘ©ΘΪO2Θ®gΘ© = SO2Θ®gΘ© ΠΛHΘΫΘ≠296.83 kJ/mol
œ¬Ν–ΥΒΖ®¥μΈσΒΡ «Θ® Θ©
A.SΘ®gΘ©ΘΪO2Θ®gΘ©=SO2Θ®gΘ© ΠΛHΘΫΘ≠Q3 kJ/mol Q3> 297.16
B.ΒΞ–±ΝρΉΣ±δΈΣ’ΐΫΜΝρΒΡΡήΝΩ±δΜ·Ω…”Ο»γΆΦ±μ Ψ
C.≥ΘΈ¬œ¬ΒΞ–±Νρ±»’ΐΫΜΝρΈ»Ε®
D.ΒΞ–±ΝρΉΣΜ·ΈΣ’ΐΫΜΝρΒΡΖ¥”Π «Ζ≈»»Ζ¥”Π
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ Β―ι “≥Θ”ΟΒΡΦΗ÷÷ΤχΧεΖΔ…ζΉΑ÷Ο»γΆΦAΓΔBΓΔCΥυ ΨΘΚ
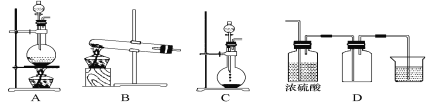
ΔΌ Β―ι “Ω…“‘”ΟBΜρCΉΑ÷Ο÷Τ»ΓΑ±ΤχΘ§»γΙϊ”ΟCΉΑ÷ΟΘ§Ά®≥Θ Ι”ΟΒΡ“©ΤΖ «___ΓΘ
ΔΎΤχΧεΒΡ–‘÷ «ΤχΧε ’Φ·ΖΫΖ®―Γ‘ώΒΡ÷ς“Σ“άΨίΓΘœ¬Ν––‘÷ ”κ ’Φ·ΖΫΖ®ΈόΙΊΒΡ «___Θ®Χν–ρΚ≈Θ§œ¬Ά§Θ©ΘΜ
AΘ°ΟήΕ» BΘ°―’…Ϊ CΘ°»ήΫβ–‘ DΘ°»»Έ»Ε®–‘ EΘ°”κ―θΤχΖ¥”Π
Δέ»τ”ΟAΉΑ÷Ο”κDΉΑ÷ΟœύΝ§÷Τ»Γ≤Δ ’Φ·XΤχΧεΘ§‘ρXΩ…Ρή «œ¬Ν–ΤχΧε÷–ΒΡ___ΓΘ
AΘ°CO2 BΘ°NO CΘ°Cl2 DΘ°H2
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩH2NCOONH4 «ΙΛ“Β”…Α±ΤχΚœ≥…ΡρΥΊΒΡ÷–Φδ≤ζΈοΓΘ‘Ύ“ΜΕ®Έ¬Ε»œ¬ΓΔΧεΜΐ≤Μ±δΒΡΟή±’»ίΤς÷–ΖΔ…ζΖ¥”ΠH2NCOONH4(s)![]() 2NH3(g)+CO2(g),ΡήΥΒΟςΗΟΖ¥”Π¥οΒΫΤΫΚβΉ¥Χ§ΒΡ «ΔΌΟΩ…ζ≥…34g NH3ΒΡΆ§ ±œϊΚΡ44g CO2 ΔΎΜλΚœΤχΧεΒΡΤΫΨυœύΕ‘Ζ÷Ή”÷ ΝΩ≤Μ±δ ΔέNH3ΒΡΧεΜΐΖ÷ ΐ±Θ≥÷≤Μ±δ ΔήΜλΚœΤχΧεΒΡΟήΕ»±Θ≥÷≤Μ±δ Δίc(NH3):c(CO2)=2:1
2NH3(g)+CO2(g),ΡήΥΒΟςΗΟΖ¥”Π¥οΒΫΤΫΚβΉ¥Χ§ΒΡ «ΔΌΟΩ…ζ≥…34g NH3ΒΡΆ§ ±œϊΚΡ44g CO2 ΔΎΜλΚœΤχΧεΒΡΤΫΨυœύΕ‘Ζ÷Ή”÷ ΝΩ≤Μ±δ ΔέNH3ΒΡΧεΜΐΖ÷ ΐ±Θ≥÷≤Μ±δ ΔήΜλΚœΤχΧεΒΡΟήΕ»±Θ≥÷≤Μ±δ Δίc(NH3):c(CO2)=2:1
A. ΔΌΔέΔί B. ΔΌΔέΔή C. ΔΎΔή D. ΔΌΔή
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com