
【题目】明矾石的主要成分是K2SO4·Al2(SO4)3·2Al2O3·6H2O,还含有少量Fe2O3杂质。利用明矾石制备氢氧化铝的流程如下:

(1)焙烧炉中发生反应的化学方程式为2Al2(SO4)3+3S![]() 2Al2O3+9SO2,该反应的氧化剂是_______。若生成l molAl2O3,则转移的电子数为__________________。
2Al2O3+9SO2,该反应的氧化剂是_______。若生成l molAl2O3,则转移的电子数为__________________。
(2)熟料溶解时,反应的离子方程式为___________________________________________。
(3)母液中溶质主要成分的化学式为_____________________________________________。
(4)将标准状况下1.12L炉气通入100mL 0.5mol·L-1NaOH溶液中,得到一种酸性溶液,则该溶液中各种离子浓度由大到小的排列顺序为____________________________。
(5)检验废渣中主要成分的方法是_____________________________________________________(写出操作步骤、现象及结论)。
【答案】Al2(SO4)3 3.612×1024 Al2O3+3H2O+2OH-=2[Al(OH)4]- K2SO4、Na2SO4 c(Na+)>c(HSO3-)>c(H+)>c(SO32-)>c(OH-) 取少量废渣,加入适量稀H2SO4,溶解后滴加KSCN溶液,溶液变红色,说明废渣中含有Fe2O3
【解析】
(1)根据方程式可知,反应中硫元素化合价由Al2(SO4)3中+6价降低为SO2中+4价,得到2个电子,发生还原反应,所以Al2(SO4)3是氧化剂。反应中硫元素化合价由0价升高为SO2中+4价,硫单质为还原剂,生成1molAl2O3需要硫的物质的量为1mol×![]() =1.5mol,所以转移电子的物质的量为1.5mol×4=6mol,转移电子数目为6mol×6.02×1023mol-1=3.612×1024。
=1.5mol,所以转移电子的物质的量为1.5mol×4=6mol,转移电子数目为6mol×6.02×1023mol-1=3.612×1024。
(2)氧化铝是两性氧化物,能溶于氢氧化钠溶液中,所以由工艺流程可知,熟料溶解为氧化铝与氢氧化钠溶液反应生成偏铝酸钠,反应离子方程式为Al2O3+3H2O+2OH-=2[Al(OH)4]-。
(3)由工艺流程可知,熟料溶解所得的溶液中含有K+、Na+、SO42-、[Al(OH)4]-、OH-等,加硫酸调pH值,[Al(OH)4]-转化为Al(OH)3沉淀而析出,母液中离子主要有K+、Na+、SO42-,因此含有溶质为K2SO4、Na2SO4。
(4)标准状况下1.12L二氧化硫的物质的量为1.12L÷22.4L/mol=0.05mol,n(NaOH)=0.1L×0.5mol/L=0.05mol,即n(SO2): n(NaOH)=0.05mol:0.05mol=1:1,故反应后溶液中溶质为NaHSO3。溶液呈酸性,说明HSO3-的电离程度大于其水解程度,同时水电离生成氢离子,所以溶液中c(H+)>c(SO32-)。HSO3-电离程度不大,故c(HSO3-)>c(H+),溶液c(OH-)等于水电离生成,浓度很小,因此溶液中离子浓度由大到小的排列顺序为c(Na+)>c(HSO3-)>c(H+)>c(SO32-)>c(OH-)。
(5)由工艺流程可知,废渣的主要成分为Fe2O3,可以通过检验铁离子来检验氧化铁。即取少量废渣,加入适量盐酸溶解,再滴加KSCN溶液,若溶液被红色,说明废渣中含有Fe2O3。


 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案科目:高中化学 来源: 题型:
【题目】(1)下列物质在固态时,属于分子晶体的有_________,属于原子晶体的________,属于离子晶体的有__________(以上均填序号)
①金刚石 ②氩 ③水晶 ④水银 ⑤氟化钙 ⑥P4 ⑦苯
(2)某常见固体能导电,质软,它可能属于__________
A.分子晶体 B.原子晶体 C.离子晶体 D.金属晶体 E.混合晶体
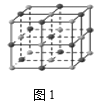
(3)在氯化钠晶体(见图1)中,每个钠离子与__________个最近且等距离的氯离子以________ 键相结合,与每个氯离子最近的且等距离的氯离子有 _______ 个。由于晶体中离子按一定的规律排列,必然造就了一颗完美晶体特定的几何外形,其中氯化钠单晶的宏观外形为_______ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以A、B为原料制备线型高分子化合物M和抗凝血药N的一种路线如下(部分反应条件和试剂略去):

已知:I. 烃A的密度是相同条件下H2密度的14倍;
I.![]()
II. ![]()
请回答下列问题:
(1)B的化学名称为____。F的结构简式为______。
(2)N中含氧官能团的名称为 _______。
(3)D→E的反应类型为_____。
(4)I的核磁共振氢谱中有_______组吸收峰。G分子中最多有____个原子共平面。
(5)B+C→M的化学方程式为_______。
(6)同时满足下列条件的J的同分异构体有_____种(不考虑立体异构)。
①苯环上连有2个取代基
②1mol该物质与足量的NaHCO3反应,生成2molCO2
(7)参照上述信息和合成路线,以HO![]() CH3和(CH3CO)2O为起始原料(其他无机试剂任选),设计制备
CH3和(CH3CO)2O为起始原料(其他无机试剂任选),设计制备![]() 的合成路线 _______。
的合成路线 _______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,Na2CO3和NaHCO3的混合溶液中c(![]() )、c(
)、c(![]() )与pH的关系如图所示[假设c(Na2CO3)+c(NaHCO3)=0.100 mol·L-1]。下列说法正确的是( )
)与pH的关系如图所示[假设c(Na2CO3)+c(NaHCO3)=0.100 mol·L-1]。下列说法正确的是( )

A.图中E点溶液表示浓度均为0.05 mol·L-1的Na2CO3和NaHCO3溶液混合后所得到的溶液
B.pH=10的溶液中:c(H+)+c(Na+)+c(H2CO3)=c(OH-)+c(![]() )
)
C.pH=11的溶液中:c(![]() )<c(
)<c(![]() )
)
D.向E点溶液中加入等体积0.100 mol·L-1的NaOH溶液,c(![]() )与c(
)与c(![]() )之和保持不变
)之和保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】.按要求写出下列化学方程式或离子方程式。
(1)铝与氢氧化钠溶液反应的离子方程式_________________________________
(2)7.80g乙炔气体完全燃烧生成二氧化碳和液态水,放出389.9kJ的热量,写出反应的热化学方程式_______________________________
(3)氢氧燃料电池是最常见的燃料电池,电解质溶液通常是KOH溶液,写出负极电极反应式______________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以苯和乙炔为原料合成化工原料E的路线如下:

回答下列问题:
(1)以下有关苯和乙炔的认识正确的是 ______
![]() 苯和乙炔都能使溴水褪色,前者为化学变化,后者为物理变化
苯和乙炔都能使溴水褪色,前者为化学变化,后者为物理变化
![]() 苯和乙炔在空气中燃烧都有浓烟产生
苯和乙炔在空气中燃烧都有浓烟产生
![]() 苯与浓硝酸混合,水浴加热55~60℃,生成硝基苯
苯与浓硝酸混合,水浴加热55~60℃,生成硝基苯
![]() 聚乙炔是一种有导电特性的高分子化合物
聚乙炔是一种有导电特性的高分子化合物
(2)A的名称 ______。
(3)生成B的化学方程式为 ______,反应类型是 ______。
(4)C的结构简式为 ______ ,C的分子中一定共面的碳原子最多有 ______ 个。
(5)与D同类别且有二个六元环结构(环与环之间用单键连接)的同分异构体有______种,请任写两种同分异构体的结构简式:______。
(6)参照上述合成路线,设计一条以乙炔和必要试剂合成环丙烷的路线: ______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】E具有果香味,由常见有机物合成E的路线如图,请回答:

(1)反应①的反应类型_______,C的名称________,F中含氧官能团名称________;
(2)检验物质F所用的试剂为_____。C转化为D所用的试剂可以是__________。
(3)下列关于物质B的说法正确的是________。
A.B为苯的同系物
B.常温常压下物质B呈气态
C.一定条件下,1 mol B最多能与4 mol H2发生加成
D.B既能使KMnO4溶液褪色又能使Br2/CCl4 溶液褪色
(4) E在氢氧化钠溶液中水解的化学方程式是___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】辉铜矿是一种重要的铜矿石,主要含有硫化亚铜(Cu2S),还有Fe2O3、SiO2及一些不溶性杂质。一种以辉铜矿石为原料制备硝酸铜晶体的工艺流程如下:

已知:部分金属阳离子生成氢氧化物沉淀的pH范围如下表所示(开始沉淀的pH按金属离子浓度为1.0mol/L计算)
离子 | 开始沉淀的pH | 完全沉淀的pH |
Fe3+ | 1.1 | 3.2 |
Mn2+ | 8.3 | 9.8 |
Cu2+ | 4.4 | 6.4 |
回答下列问题
(1)浸取后得到的浸出液中含有CuSO4、MnSO4。写出浸取时产生CuSO4、MnSO4反应的化学方程式__________。
(2)调节pH的目的是___________,pH的调节范围为___________。
(3)生成MnCO3沉淀的离子方程式为___________。
(4)操作A为___________。
(5)由辉铜矿制取铜的反应过程可以表示为:
2Cu2S(s)+3O2(g)═ 2Cu2O(s)+ 2SO2(g)△H=﹣768.2kJ/mol
2Cu2O(s)+ Cu2S(s)═ 6Cu(s)+ SO2(g)△H=" +116.0" kJ/mol
则由Cu2S与O2加热反应生成Cu的热化学方程式为___________。
(6)若用含85% Cu2S(Mr=160)的辉铜矿来制备无水Cu(NO3)2,假设浸取率为95%,调节pH时损Cu 3%,蒸氨过程中有5%未转化为CuO,其它过程中无损耗,则1.6 kg这样的辉铜矿最多能制备__________mol无水Cu(NO3)2。(计算结果精确到小数点后1位)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原电池原理的发现极大地推进了现代化的进程,改变了人们的生活方式。关于下图所示原电池的说法 不正确的是 ( )
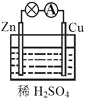
A.该装置将化学能转化为电能
B.反应一段时间后溶液的pH会增大
C.铜片上发生的反应是Cu2+ + 2e-=Cu
D.该装置使氧化反应和还原反应分别在两个不同的区域进行
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com