
【题目】在下述转化关系中,已知B、D都是淡黄色固体,且A与D为单质,并可反应生成离子化合物。试回答:
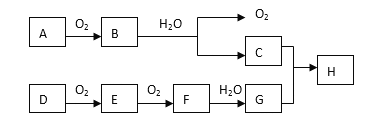
(1) G的化学式为________;
(2)写出B的电子式______________。
(3)写出B +水→C的化学反应方程式_______。
(4)B和E反应也可生成H,则该反应的化学方程式为____。
【答案】H2SO4 ![]() 2Na2O2+2H2O=4NaOH+O2↑ Na2O2 +SO2=Na2SO4
2Na2O2+2H2O=4NaOH+O2↑ Na2O2 +SO2=Na2SO4
【解析】
常见淡黄色固体有Na2O2和S,其中B能与水反应生成氧气,则B为Na2O2,A为Na,C为NaOH,D可以与氧气连续反应,则D为S,E为SO2,F为SO3,G为H2SO4,G与NaOH发生中和反应生成H为Na2SO4,然后根据题目要求写出相应物质的化学式、电子式或相应反应的方程式。
根据上述推断可知A是Na,B是Na2O2,C是NaOH,D是S,E是SO2,F是SO3,G是H2SO4,H为Na2SO4。
(1)根据上述推断可知G是硫酸,则G的化学式为H2SO4;
(2) B是Na2O2,Na2O2是离子化合物,两个O原子通过一对共用电子对结合,每个Na原子失去1个电子形成Na+,每个O原子再获得一个电子形成O22-,O22-与2个Na+通过离子键结合,故该物质的电子式为![]() ;
;
(3)过氧化钠与水反应产生氢氧化钠和氧气,反应的方程式为:2Na2O2+2H2O=4NaOH+O2↑;
(4) Na2O2具有强的氧化性,SO2具有还原性,二者发生氧化还原反应产生硫酸钠,根据电子守恒、原子守恒,可得该反应的化学方程式为Na2O2 +SO2=Na2SO4。


科目:高中化学 来源: 题型:
【题目】有周期表序数前20 的A、B、C、D、E五种元素,原子序数E<C<D<A<B;E原子是最外电子层有4个电子;A-离子和B+离子的核外电子层结构相同;D的气态氢化物的化学式为H2D,D在其最高价氧化物中的质量分数为40%,且D原子核内质子数和中子数相等;C的原子序数比D少5,比B少8。
(1)各元素的名称为A_____、B_____、C_____、D_____、E_____。
(2)D元素位于第____周期____族。
(3)五种元素最高价氧化物的水化物中,酸性最强的是___(写化学式下同),碱性最强的是____。
(4)写出C元素的单质与水反应的离子方程式______。
(5)写出B元素的氧化物的电子式________。
(6)写出E元素的氢化物的结构式________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某气态烃A在标准状况下的密度为1.25g/L,其产量可以用来衡量一个国家的石油化工发展水平。B和D都是生活中常见的有机物,D能跟碳酸氢钠反应,F有香味。它们之间的转化关系如下图所示:
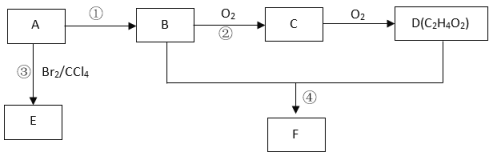
(1)A的结构式为__________________,B中官能团的电子式为______________________, D中官能团的名称为_________________。
(2)反应①的反应类型是_________,反应③的化学方程式为_____________________。
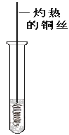
(3)反应②在Cu做催化剂的条件下进行,该实验的步骤是将红亮的铜丝置于酒精灯上加热,待铜丝变为黑色时,迅速将其插入到装有B的试管中(如图所示)。重复操作2-3次,观察到的现象是_________________。该反应的化学方程式为___________。
(4)D与碳酸氢钠溶液反应的离子方程式为_____________。
(5)B、D在浓硫酸的作用下实现反应④,实验装置如下图所示:

试管1中装药品的顺序为先取__________(填“B”、“D”、“浓硫酸”,下同),再加入_______________,最后加入____________。图中X的化学式为___,其作用是____________________________。浓硫酸的作用是_________________________。该反应的化学方程式为_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于硫的说法不正确的是( )
A.试管内壁附着的硫可用二硫化碳溶解除去
B.游离态的硫存在于火山喷口附近或地壳的岩层里
C.单质硫既有氧化性,又有还原性
D.硫在空气中的燃烧产物是二氧化硫,在过量纯氧中的燃烧产物是三氧化硫
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,不能按![]() (“→”表示一步完成)的关系相互转化的是( )
(“→”表示一步完成)的关系相互转化的是( )
选项 | a | b | c |
A | Fe | FeCl2 | FeCl3 |
B | Si | SiO2 | SiF4 |
C | HNO3 | NO | NO2 |
D | Al | Al2O3 | Al(OH)3 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫—碘循环分解水制氢主要涉及下列反应:
Ⅰ.SO2+2H2O+I2===H2SO4+2HI;Ⅱ.2HI![]() H2+I2 ;Ⅲ.2H2SO4===2SO2+O2+2H2O。
H2+I2 ;Ⅲ.2H2SO4===2SO2+O2+2H2O。
(1)分析上述反应,下列判断正确的是________。
a.反应Ⅲ易在常温下进行
b.反应Ⅰ中SO2氧化性比HI强
c.循环过程中需补充H2O
d.循环过程产生1 mol O2的同时产生1 mol H2
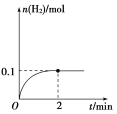
(2)一定温度下,向1 L密闭容器中加入1 mol HI(g),发生反应Ⅱ,H2物质的量随时间的变化如图所示。0~2 min内的平均反应速率v(HI)=________。该温度下,H2(g)+I2(g)![]() 2HI(g)的平衡常数K=________。相同温度下,若开始加入HI(g)的物质的量是原来的2倍,则________是原来的2倍。
2HI(g)的平衡常数K=________。相同温度下,若开始加入HI(g)的物质的量是原来的2倍,则________是原来的2倍。
a.平衡常数
b.HI的平衡浓度
c.达到平衡的时间
d.平衡时H2的体积分数
(3)实验室用Zn和稀硫酸制取H2,反应时溶液中水的电离平衡________移动(填“向左”“向右”或“不”);若加入少量下列试剂中的________,产生H2的速率将增大。
a.NaNO3 b.CuSO4
c.Na2SO4 d.NaHSO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酰氯(NOCl,熔点:-64.5 ℃,沸点:-5.5 ℃)是一种黄色气体,遇水易反应生成一种无氧酸和两种氮的常见氧化物。亚硝酰氯应用广泛,可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成。
(1)甲组同学拟制备原料气NO和Cl2,制备装置如图所示,为制备纯净干燥的气体,补充右表中缺少的药品。
装置Ⅰ | 装置Ⅱ | ||
蒸馏烧瓶中 | A仪器中 | ||
制备纯净的Cl2 | MnO2 | ①______ | ②______ |
制备纯净的NO | Cu | ③______ | ④______ |
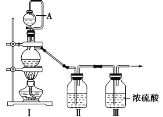
(2)乙组同学对甲组同学制取NO的装置略加改良,结合甲组制得的Cl2共同制备NOCl,装置如图所示:
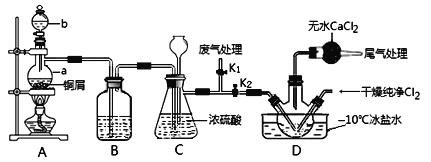
①仪器b的名称为________________。
②组装好实验装置后应先______________,然后依次装入药品。此实验关键操作有两点:一是将Cl2充满D装置的三颈瓶中;二是A中反应开始时要先关闭K2,打开K1,待NO充满装置后再关闭K1,打开K2。这两步操作中充满的目的都是__________________________________________________。
③若C装置中压强过大,可以观察到的现象是_________________________。
④装置D中冰盐水的作用是__________________。
(3)亚硝酰氯(NOCl)纯度的测定:将所得亚硝酰氯(NOCl)产品13.10g溶于水,配制成250mL溶液;取出25.00mL,以K2CrO4溶液为指示剂,用0.8mol·L-1AgNO3标准溶液滴定至终点,消耗标准溶液的体积为 22.50mL。(已知:Ag2CrO4为砖红色固体)
①亚硝酰氯(NOCl)与水反应的化学方程式为_________________________。
②亚硝酰氯(NOCl)的质量分数为______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com