
| A、蒸馏烧瓶中要放入碎瓷片防止暴沸 |
| B、温度计的水银球放在支管口稍下位置,不能插入液面 |
| C、冷凝水应该是下进上出,与蒸汽的流向相反 |
| D、开始蒸馏时,应该先加热,再开冷凝水;蒸馏完毕,应该先关冷凝水再撤酒精灯 |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
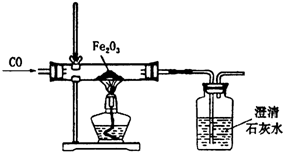 某课外活动小组在实验室条件下探究CO与Fe2O3反应的产物情况,实验设计如图所示.
某课外活动小组在实验室条件下探究CO与Fe2O3反应的产物情况,实验设计如图所示.| 加热时间/min | 0 | 10 | 60 | 120 | 130 |
| 固体质量/g | 24.0 | 23.2 | 21.6 | 16.8 | 16.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:
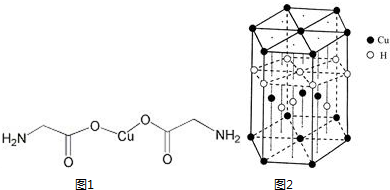 锂-磷酸氧铜电池正极的活性物质是Cu4O(PO4)2,可通过下列反应制备:2Na3PO4+4CuSO4+2NH3?H2O=Cu4O(PO4)2↓+3Na2SO4+(NH4)2SO4+H2O
锂-磷酸氧铜电池正极的活性物质是Cu4O(PO4)2,可通过下列反应制备:2Na3PO4+4CuSO4+2NH3?H2O=Cu4O(PO4)2↓+3Na2SO4+(NH4)2SO4+H2O查看答案和解析>>
科目:高中化学 来源: 题型:
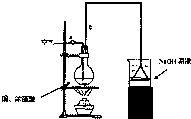 某学生课外学习活动小组针对教材中铜与浓硫酸反应,提出了研究“能够与铜反应的硫酸的最低浓度是多少?”的问题,并设计了如下方案进行实验:
某学生课外学习活动小组针对教材中铜与浓硫酸反应,提出了研究“能够与铜反应的硫酸的最低浓度是多少?”的问题,并设计了如下方案进行实验:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氢氟酸保存在塑料盖的玻璃瓶中 |
| B、氯水盛放在棕色细口瓶中 |
| C、液臭盛放在用橡皮塞的玻璃瓶中 |
| D、固态碘放在棕色的细口瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①中水的电离程度最小,③中水的电离程度最大 |
| B、将①④混合,若c(CH3COO-)>c(H+),则混合液一定呈碱性 |
| C、将四份溶液分别稀释到原体积相同倍数后,溶液的pH:③>④,②>① |
| D、将②③混合,若pH=7,则消耗溶液的体积:②>③ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com