
【题目】硼及其化合物在工业上有许多用途.以铁硼矿(主要成分为Mg2B2O5H2O和Fe3O4 , 还有少量Fe2O3、FeO、CaO、Al2O3和SiO2等)为原料制备硼酸(H3BO3)的工艺流程如图所示: 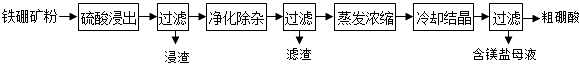
回答下列问题:
(1)写出Mg2B2O5H2O与硫酸反应的化学方程式 . 为提高浸出速率,除适当增加硫酸浓度外,还可采取的措施有(写出两条).
(2)利用的磁性,可将其从“浸渣”中分离.“浸渣”中还剩余的物质是(化学式).
(3)“净化除杂”需先加H2O2溶液,作用是 . 然后在调节溶液的pH约为5,目的是
(4)“粗硼酸”中的主要杂质是(填名称).
(5)以硼酸为原料可制得硼氢化钠(NaBH4),它是有机合成中的重要还原剂,其电子式为 .
(6)单质硼可用于生成具有优良抗冲击性能硼钢.以硼酸和金属镁为原料可制备单质硼,用化学方程式表示制备过程 .
【答案】
(1)Mg2B2O5?H2O+2H2SO4![]() 2H3BO3+2MgSO;提高反应温度或减小铁硼矿粉粒径
2H3BO3+2MgSO;提高反应温度或减小铁硼矿粉粒径
(2)Fe3O4; SiO2、CaSO4
(3)将亚铁离子氧化为铁离子;使铁离子、铝离子形成氢氧化物沉淀而除去
(4)七水硫酸镁
(5)
(6)2H3BO3![]() B2O3+3H2O、B2O3+3Mg
B2O3+3H2O、B2O3+3Mg ![]() 2B+3MgO
2B+3MgO
【解析】解:以铁硼矿(主要成分为Mg2B2O5H2O和Fe3O4,还有少量Fe2O3、FeO、CaO、Al2O3和SiO2等)为原料制备硼酸(H3BO3),由流程可知,加硫酸溶解只有SiO2不溶,CaO转化为微溶于水的CaSO4,“净化除杂”需先加H2O2溶液,将亚铁离子转化为铁离子,调节溶液的pH约为5,使铁离子、铝离子均转化为沉淀,则滤渣为氢氧化铝、氢氧化铁,然后蒸发浓缩、冷却结晶、过滤分离出H3BO3,(1)Mg2B2O5H2O与硫酸反应的化学方程式Mg2B2O5H2O+2H2SO4 ![]() 2H3BO3+2MgSO4,为提高浸出速率,除适当增加硫酸浓度浓度外,还可采取的措施有提高反应温度或减小铁硼矿粉粒径等,所以答案是:Mg2B2O5H2O+2H2SO4
2H3BO3+2MgSO4,为提高浸出速率,除适当增加硫酸浓度浓度外,还可采取的措施有提高反应温度或减小铁硼矿粉粒径等,所以答案是:Mg2B2O5H2O+2H2SO4 ![]() 2H3BO3+2MgSO4;提高反应温度或减小铁硼矿粉粒径;(2)利用Fe3O4的磁性,可将其从“浸渣”中分离.“浸渣”中还剩余的物质是SiO2、CaSO4,所以答案是:Fe3O4;SiO2、CaSO4;(3)“净化除杂”需先加H2O2溶液,作用是将亚铁离子氧化为铁离子.然后在调节溶液的pH约为5,目的是使铁离子、铝离子形成氢氧化物沉淀而除去,
2H3BO3+2MgSO4;提高反应温度或减小铁硼矿粉粒径;(2)利用Fe3O4的磁性,可将其从“浸渣”中分离.“浸渣”中还剩余的物质是SiO2、CaSO4,所以答案是:Fe3O4;SiO2、CaSO4;(3)“净化除杂”需先加H2O2溶液,作用是将亚铁离子氧化为铁离子.然后在调节溶液的pH约为5,目的是使铁离子、铝离子形成氢氧化物沉淀而除去,
所以答案是:将亚铁离子氧化为铁离子;使铁离子、铝离子形成氢氧化物沉淀而除去;(4)最后浓缩结晶时硫酸镁易结合水以晶体析出,则“粗硼酸”中的主要杂质是七水硫酸镁,所以答案是:七水硫酸镁; (5)NaBH4为离子化合物,含离子键、共价键,其电子式为  ,所以答案是:
,所以答案是:  ;(6)以硼酸和金属镁为原料可制备单质硼的化学方程式为2H3BO3
;(6)以硼酸和金属镁为原料可制备单质硼的化学方程式为2H3BO3 ![]() B2O3+3H2O、B2O3+3Mg
B2O3+3H2O、B2O3+3Mg ![]() 2B+3MgO,所以答案是:2H3BO3
2B+3MgO,所以答案是:2H3BO3 ![]() B2O3+3H2O、B2O3+3Mg
B2O3+3H2O、B2O3+3Mg ![]() 2B+3MgO.
2B+3MgO.


科目:高中化学 来源: 题型:
【题目】实验中需2mol/L的Na2CO3溶液950mL,配制时应选用的容量瓶的规格和称取的Na2CO3质量分别为
A.1000mL , 212gB.950mL , 201.4gC.500mL , 286gD.1000mL, 201.4g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用下述装置制取氯气,并用氯气进行下列实验。看图回答下列问题:

(1)装置中B仪器的名称:___________,E中为红色湿布条,可观察到的现象是_______。
(2)洗气装置C是为了除去Cl2中的HCl气体,D是为了干燥Cl2,则C、D中应分别放入下列溶液中的C______________;D______________。
①NaOH溶液 ②饱和食盐水 ③AgNO3溶液 ④浓H2SO4
(1)实验室常用MnO2和浓盐酸制取Cl2,请写出化学方程式:_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对于“摩尔”的说法和理解正确的是( )
A. 摩尔是国际科学界建议采用的一种物理量
B. 摩尔可以把微观粒子与可称量物质联系起来
C. 摩尔是物质的量的单位,简称摩,符号为mol
D. 国际上规定,0.012kg碳原子所含有的碳原子数目为1摩
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用O2将HCl转化为Cl2 , 可提高效益,减少污染.
(1)传统上该转化通过如图1所示的催化循环实现.其中,反应①为:2HCl(g)+CuO(s)H2O(g)+CuCl2(s)△H1 , 反应②生成1molCl2(g)的反应热为△H2 , 则总反应的热化学方程式为(反应热用△H1和△H2表示). 
(2)新型RuO2催化剂对上述HCl转化为Cl2的总反应具有更好的催化活性. ①实验测得在一定压强下,总反应的HCl平衡转化率随温度变化的αHCl~T曲线如图2,则总反应的△H0(填“>”、“=”或“<”);A、B两点的平衡常数K(A)与K(B)中较大的是 .
②在上述实验中若压缩体积使压强增大,画出相应αHCl~T曲线的示意图,并简要说明理由:
③下列措施中,有利于提高αHCl的有 .
A.增大n(HCl) B.增大n(O2)
C.使用更好的催化剂 D.移去H2O
(3)一定条件下测得反应过程中n(Cl2)的数据如下:
t/min | 0 | 2.0 | 4.0 | 6.0 | 8.0 |
n(Cl2)/10﹣3mol | 0 | 1.8 | 3.7 | 5.4 | 7.2 |
计算2.0~6.0min内以HCl的物质的量变化表示的反应速率(以molmin﹣1为单位,写出计算过程).
(4)Cl2用途广泛,写出用Cl2制备漂白粉的化学反应方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列应用或事实与胶体的性质没有关系的是( )
A. 在氯化铝溶液中逐滴加入氨水溶液,制取氢氧化铝沉淀
B. 用石膏或盐卤点制豆腐
C. 尿毒症患者做“血液透析”
D. 水泥生产厂用电网除尘
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将下列装置如图连接,D、F、X、Y、E 都是铂电极,C是铁电极.甲,乙,丙三个装置中电解前后溶液的体积都是500mL.将电源接通后,向乙中滴入酚酞试液,在F极附近显红色.下列说法不正确的是( ) 
A.电源B 极的名称是负极,丁中Y极附近颜色变深
B.乙装置中电解一段时间后,加入0.2mol盐酸则可以恢复原来的浓度
C.设甲池中溶液的体积在电解前后都是500ml,当乙池所产生气体的体积为4.48L(标准状况)时,甲池中所生成物质的物质的量浓度为0.2mol/L
D.甲装置中电解反应的总化学方程式是:CuSO4+Fe ![]() Cu+FeSO4
Cu+FeSO4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com