
【题目】已知某无色透明溶液中仅含有包括Na+和CH3COO﹣在内的四种离子.
请回答下列问题.
(1)该溶液中的溶质可能有三种情况,请分别写出各种情况的化学式:①②; ③ .
(2)25℃,若由0.1mol/L的CH3COOH溶液与0.1mol/L的NaOH溶液等体积混合,测得混合溶液的pH=8,则c(CH3COOH)+c(H+)的精确值为mol/L.
(3)若该溶液的pH=8,则c(Na+)﹣c(CH3COO﹣)的精确值为mol/L.
(4)当溶液中各离子浓度大小的顺序为c(CH3COO﹣)>c(Na+)>c(H+)>c(OH﹣)时,则该溶液可能是(填序号);
A.由0.1mol/L的CH3COONa溶液与0.1mol/L的CH3COOH溶液等体积混合而成
B.由0.1mol/L的CH3COOH溶液与0.1mol/L的NaOH溶液等体积混合而成
C.由0.2mol/L的CH3COONa溶液与0.1mol/L的HCl溶液等体积混合而成
D.由0.2mol/L的CH3COOH溶液与0.1mol/L的NaOH溶液等体积混合而成
(5)常温下,将a mol/L的CH3COOH溶液与0.01mol/L的NaOH溶液等体积混合,反应平衡后溶液中c(Na+)=c(CH3COO﹣),用含a的代数式表示CH3COOH的电离平衡常数Ka= .
【答案】
(1)CH3COONa,CH3COONa和CH3COOH,CH3COONa和NaOH
(2)1×10﹣6
(3)9.9×10﹣7
(4)A,D
(5)![]()
【解析】解:(1)能电离出醋酸根离子的物质可以是醋酸和醋酸钠,能电离出钠离子的物质可以是氢氧化钠和醋酸钠,所以当溶液中含有Na+和CH3COO﹣在以及OH﹣、H+时,溶液中溶质的组成可以是:①CH3COONa、CH3COONa和CH3COOH、CH3COONa和NaOH,
所以答案是:CH3COONa;CH3COONa和CH3COOH;CH3COONa和NaOH;
(2)25℃,若由0.1mol/L的CH3COOH溶液与0.1mol/L的NaOH溶液等体积混合,测得混合溶液的pH=8,由质子守恒可知:c(CH3COOH)+c(H+)=c(OH﹣)=1×10﹣6,
所以答案是:1×10﹣6;
(3)溶液中存在电荷守恒c(Na+)+c(H+)=c(CH3COO﹣)+c(OH﹣),所以c(Na+)﹣c(CH3COO﹣)=c(OH﹣)﹣c(H+)= ![]() mol/L﹣10﹣8 mol/L=(10﹣6﹣10﹣8)mol/L=9.9×10﹣7,
mol/L﹣10﹣8 mol/L=(10﹣6﹣10﹣8)mol/L=9.9×10﹣7,
所以答案是:9.9×10﹣7;
(4)A.等浓度的CH3COONa和醋酸混合溶液中,醋酸的电离程度大于醋酸根离子的水解程度,所以离子的浓度大小为:c(CH3COO﹣)>c(Na+)>c(H+)>c(OH﹣),故符合;
B.醋酸钠溶液中,钠离子浓度大于醋酸根浓度,故不符合;
C.由0.2mol/L的CH3COONa溶液与0.1mol/L的HCl溶液等体积混合而成,得到物质的量浓度相等的醋酸、醋酸钠和氯化钠,钠离子浓度大于醋酸根浓度,故不符合;
D.由0.2mol/L的CH3COOH溶液与0.1mol/L的NaOH溶液等体积混合而成,得到等物质的量浓度的醋酸和醋酸钠,醋酸的电离程度大于醋酸根离子的水解程度,所以离子的浓度大小为:c(CH3COO﹣)>c(Na+)>c(H+)>c(OH﹣),故符合;
故选:AD;
(5)常温下,将a mol/L的CH3COOH溶液与0.01mol/L的NaOH溶液等体积混合,反应平衡后溶液中c(Na+)=c(CH3COO﹣),根据电荷守恒得c(OH﹣)=c(H+),溶液呈中性,又电离平衡常数Ka= ![]() ,c(H+)=10﹣7mol/L,c(Na+)=c(CH3COO﹣)=0.005mol/L,c(CH3COOH)=
,c(H+)=10﹣7mol/L,c(Na+)=c(CH3COO﹣)=0.005mol/L,c(CH3COOH)= ![]() mol/L,则Ka=
mol/L,则Ka= ![]() ,
,
所以答案是: ![]() .
.
【考点精析】通过灵活运用弱电解质在水溶液中的电离平衡,掌握当弱电解质分子离解成离子的速率等于结合成分子的速率时,弱电解质的电离就处于电离平衡状态;电离平衡是化学平衡的一种,同样具有化学平衡的特征.条件改变时平衡移动的规律符合勒沙特列原理即可以解答此题.


 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源: 题型:
【题目】下列各组离子能在同一溶液中大量共存的是
A.Ba2+、Na+、、Cl-、SO42-B.H+、K+、NO3-、CO32-
C.H+、Cu2+、、Cl-、SO42-D.Ag+ 、Na+、NO3-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究大气中含硫化合物(主要是H2S和SO2)的转化具有重要意义。
(1)H2S资源化利用途径之一是回收能量并得到单质硫,如图为质子膜H2S燃料电池的示意图。
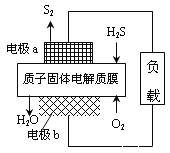
①电极a为电池的_______极,电极b上发生的电极反应为:______________________。
②每17gH2S参与反应,有_____molH+经质子膜进入_____极区。
(2)低浓度SO2废气的处理是工业难题,目前常用的方法如下:
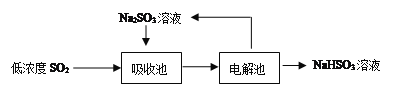
①Na2SO3溶液吸收SO2的化学方程式是____________________________________。
②如果用含等物质的量溶质的下列各溶液分别吸收SO2,则理论吸收量最多的是(____)
A.Na2SO3B.Na2S C.Ba(NO3)2 D.酸性KMnO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,反应H2(g)+CO2(g)H2O(g)+CO(g)的平衡常数K= ![]() .该温度下在体积均为10L的三个密闭容器中分别加入反应物,起始加入量如图所示:下列判断不正确的是( )
.该温度下在体积均为10L的三个密闭容器中分别加入反应物,起始加入量如图所示:下列判断不正确的是( )
起始量 | 甲 | 乙 | 丙 |
H2 (mol) | 1 | 2 | 2 |
CO2(mol) | 1 | 1 | 2 |
A.反应开始时,甲中的反应速率最慢,丙中的反应速率最快
B.平衡时,甲和丙中CO2的转化率相等,均是60%
C.平衡时,乙中H2的转化率大于60%
D.平衡时,丙中c(H2)是0.08 molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】相同温度下,体积均为1L的两个恒容密闭容器中发生可逆反应:A(g)+2B(g)2C(g)△H=a kJmol﹣1 . (a>0),实验测得起始、平衡时的有关数据如下表所示,下列叙述错误的是( )
容器 | 起始时各物质的物质的量/mol | 达到平衡时 | ||
A | B | C | ||
① | 1 | 2 | 0 | 吸收热量:0.25akJ |
② | 0.5 | 1 | 1 | 吸收热量:Q kJ |
A.容器①、②中反应的平衡常数相等
B.平衡时,两个容器中C的体积分数均约为18%
C.容器②中达到平衡时吸收的热量Q=0.25a kJ
D.若其他条件不变,把容器①的体积改为2L,则平衡时吸收的热量小于0.25a kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应属于离子反应的是
A.氢气还原氧化铜生成水和铜
B.石灰石高温分解生成氧化钙和二氧化碳
C.盐酸滴加到石灰石固体上
D.实验室加热高锰酸钾制氧气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某再回收利用公司对一厨房铁铝合金废旧家具进行回收利用,其流程如下图所示:
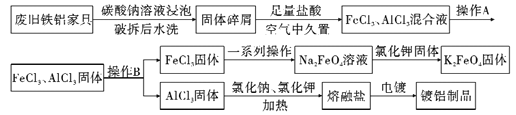
请回答下列问题:
(1)流程中加碳酸钠溶液浸泡的目的是_______________;在空气中久置的目的是_________________。
(2)同条件下Na2FeO4溶解度__________K2FeO4溶解度(填“低于”,“高于”, “不确定”),推测K2FeO4在净水方面的作用_______________。(至少答两条)
(3)已知K2FeO4水解显碱性。在洗涤K2FeO4固体时最好选用__________。
A.水 B.亚硫酸氢钠溶液 C.氢氧化钠溶液 D.先氢氧化钠溶液后乙醇
(4)熔融盐电镀中铝元素和氯元素主要以AlCl4-和Al2Cl7-形式存在,铝电镀的主要电极反应式为___________________。(写出一个电极反应即可)
(5)已知氯化铝受热易升华,气态氯化铝的密度为11.92g/L(已转化为标准状况),则气态氯化铝的分子式为______________________。
(6)氢氧化铝经常用于做药品,有两种溶解方式:可以溶解为Al3+或[Al(OH)4]-。已知25℃时氢氧化铝在pH=3和pH=10的两溶液中溶解度均为7.8×10-3g(溶液密度近似为1g/mL),则25℃下氢氧化铝的两种溶解方式的溶度积之比为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮及其化合物在人们的日常生活、生产和环保事业中属于“明星物质”。回答下列问题:
(1)氨气是农业肥料和化工生产的重要原料,其电子式为____。
(2)叠氮化钠(NaN3)在药物制备、合成影像、化学分析、汽车制造等行业有着广泛的用途,但该物质极易爆炸,且有副毒。可用NaClO溶液对含有叠氮化钠的溶液进行处理,生成一种无污染的气体单质,反应的化学方程式为______________。
(3)“固氮”是农业科学家研究的永恒主题。在某特殊催化剂和光照条件下,N2与水反应可生成NH3。
已知:
(i)4NH3(g)+3O2(g)![]() 2N2(g) +6H2O(g) △H1=-1266 kJ/mol;
2N2(g) +6H2O(g) △H1=-1266 kJ/mol;
(ii)H2O(g)=H2O(l) △H2= -44.0kJ/mol。
则2N2(g) +6H2O(l)![]() 4NH3(g)+3O2(g) △H3=______kJ/mol。
4NH3(g)+3O2(g) △H3=______kJ/mol。
(4)目前“人工固氮”最成功的应用就是工业合成氨:
N2(g) +3H2(g)![]() 2NH3(g) △H=-92.4kJ/mol。将1.00molN2和3.00molH2充入到容积为3L的恒容密闭容器中,发生上述反应。
2NH3(g) △H=-92.4kJ/mol。将1.00molN2和3.00molH2充入到容积为3L的恒容密闭容器中,发生上述反应。

①图甲是测得X、Y 的浓度随时间变化的曲线.其中Y 为_____(写化学式),反应达到平衡时的平均反应速率v(N2) =_________。
②在不同温度和压强下,平衡体系中NH3的体积分数与温度、压强关系如图乙,则压强p1_____p2(填“>”“<”“=”或“不确定”,下同),B、D 两点的平衡常数KB____KD,B 点N2 的转化率=_________(保留3位有效数字)。
(5)“绿水青山就是金山银山”,利用原电池原理(6NO2 +8NH3=7N2+12H2O)可以处理氮的氧化物和NH3 尾气,装置原理图如图丙:

负极反应式为__________,当有标准状况下4.48 L NO2被处理时,转移电子的物质的量为_____mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com