
【题目】已知:2FeSO4·7H2O ![]() Fe2O3+SO2↑+SO3↑+14H2O↑。用下图所示装置检验FeSO4·7H2O的所有分解产物,下列说法不正确的是
Fe2O3+SO2↑+SO3↑+14H2O↑。用下图所示装置检验FeSO4·7H2O的所有分解产物,下列说法不正确的是

A. 乙、丙、丁中可依改盛装无水CuSO4、Ba(NO3)2溶液、品红溶液
B. 实验时应先打开K,缓缓通入N2,再点燃酒精喷灯
C. 甲中残留固体加稀硫酸溶解,再滴加KSCN,溶液变红
D. 还应在丁装置后面连接盛有NaOH溶液的洗气瓶
【答案】A
【解析】因为2FeSO4·7H2O ![]() Fe2O3+SO2↑+SO3↑+14H2O↑,A. 乙中装无水CuSO4、可以检验生成的H2O,SO2和SO3通入到Ba(NO3)2溶液后,SO2被氧化成H2SO4,丁装置的品红溶液不会退色,不能鉴别SO2存在,所以A错;B. 实验时应先打开K,缓缓通入N2,排除装置中的空气,防止FeSO4中的Fe2+被氧,所以B正确;C. 因为甲中反应为2FeSO4·7H2O
Fe2O3+SO2↑+SO3↑+14H2O↑,A. 乙中装无水CuSO4、可以检验生成的H2O,SO2和SO3通入到Ba(NO3)2溶液后,SO2被氧化成H2SO4,丁装置的品红溶液不会退色,不能鉴别SO2存在,所以A错;B. 实验时应先打开K,缓缓通入N2,排除装置中的空气,防止FeSO4中的Fe2+被氧,所以B正确;C. 因为甲中反应为2FeSO4·7H2O ![]() Fe2O3+SO2↑+SO3↑+14H2O↑残留固体为Fe2O3,加稀硫酸溶解,生成了Fe3+再滴加KSCN,溶液变红,所以C正确;D. SO3有毒,为防止污染空气,应在丁装置后面连接盛有NaOH溶液的洗气瓶,故D正确;所以本题答案A。
Fe2O3+SO2↑+SO3↑+14H2O↑残留固体为Fe2O3,加稀硫酸溶解,生成了Fe3+再滴加KSCN,溶液变红,所以C正确;D. SO3有毒,为防止污染空气,应在丁装置后面连接盛有NaOH溶液的洗气瓶,故D正确;所以本题答案A。


科目:高中化学 来源: 题型:
【题目】(双选)碳有三种同素异形体:金刚石、石墨、足球烯(C60),其中足球烯是分子晶体。据此推测下列叙述正确的是( )
A. 金刚石、石墨、足球烯和氧气反应最终产物不同
B. 足球烯可以发生加成反应
C. 石墨、足球烯均作为生产耐高温润滑剂的原料
D. 足球烯在苯中的溶解度比在乙醇中的溶解度大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各表述与示意图一致的是( )
A.图①表示25℃时,用0.1 molL﹣1盐酸滴定20 mL 0.1 molL﹣1 NaOH溶液,溶液的p随加入酸体积的变化
B.图②中曲线表示反应2SO2(g)+O2(g)2SO3(g)△H<0正、逆反应的平衡常数K随温度的变化
C.图③表示10 mL 0.01 molL﹣1 KMnO4酸性溶液与过量的0.1 molL﹣1 H2C2O4溶液混合时,n(Mn2+)随时间的变化
D.图④中a、b曲线分别表示反应CH2═CH2(g)+H2(g)→CH3CH3(g)△H<0使用和未使用催化剂时,反应过程中的能量变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学欲用物质的量浓度为0.100 0molL﹣1的盐酸测定未知物质的量浓度的氢氧化钠溶液,选择酚酞作指示剂.请填写下列空白:
(1)用标准的盐酸滴定待测的氢氧化钠溶液时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,直到因加入一滴盐酸,溶液 , 立即停止滴定.
(2)下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是(填序号).
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
E.滴定过程中,锥形瓶的振荡过于激烈,使少量溶液溅出
(3)若某次滴定结束时,酸式滴定管中的液面如图所示,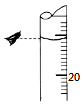
则读数为 mL.若仰视,会使读数偏(填“大”或“小”).
(4)再结合表数据,计算被测氢氧化钠溶液的物质的量浓度是 molL﹣1 .
滴定 | 待测溶液 | 标准酸体积 | |
滴定前的刻度/mL | 滴定后的刻度/mL | ||
第一次 | 10.00 | 1.34 | 19.39 |
第二次 | 10.00 | 4.10 | 21.10 |
第三次 | 10.00 | 0.40 | 17.60 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下。向20.00mL0.1mol/LHA溶液中滴入0.1mol/LNaOH溶液,溶液中由水电离出的氢离子浓度的负对数[-lgc水(H+)]与所加NaOH溶液体积的关系如图所示,下列说法不正确的是

A. 常温下,Ka(HA)约为10-5
B. M、P两点溶液对应的pH=7
C. b=20.00
D. M点后溶液中均存在c(Na+)>c(A-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学-选修5:有机化学基础]2017年治疗膀胱癌的有机小分子药物Aminolevulinic acid被批准使用,其合成路线如下:

已知:
请回答:
(1)A的名称为________,G中含氧官能团的名称为____________________________。
(2)⑤的反应类型为____________________,H的分子式为_____________________________。(3)①的化学方程式为__________________________________________。
(4)④的化学方程式为______________________________________________。
(5)D的同分异构体中,同时满足下列条件的共有____种(不含立体异构);
a.能与Na反应产生气体
b.既能发生银镜反应,又能发生水解反应
其中核磁共振氧谐有4组峰的物质的结构简式为________________(任写一种)。
(6)参照上述合成路线,设计由2-甲基丙酸和甲醇为起始原料制备2-甲基丙烯酸甲酯的合成路线(无机试剂任选)______________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)地下钢管连接镁块是金属防腐措施中的________________________法。
(2)铅及其化合物可用于蓄电池,耐酸设备及X射线防护材料等。回答下列问题:
①铅是碳的同族元素,比碳多4个电子层。铅在元素周期表的位置为_______________________;铅的最高价氧化物对应水化物的酸性比碳酸的_______(填“强”或“弱”)。
②PbO2与浓盐酸共热生成黄绿色气体,反应的化学方程式为___________________________。
③铅蓄电池放电时的正极反应式为__________________________________________ ,当电路中有2mol电子转移时,理论上两电极质量变化的差为_______ g。
(3)NO2、O2和熔融NaNO3可制作燃料电池,其原理见下图,石墨Ⅰ为电池的________极;该电池在使用过程中石墨Ⅰ电极上生成氧化物Y,其电极反应式为__________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列反应中,HCl作氧化剂的是( )
A.NaOH+HCl=NaCl+H2O
B.Zn+2HCl=ZnCl2+H2↑
C.MnO2+4HCl(浓) ![]() MnCl2+2H2O+Cl2↑
MnCl2+2H2O+Cl2↑
D.CuO+2HCl=CuCl2+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com