
【题目】在密闭容器中,m A(g)+n B(g) ![]() p C(g)反应达平衡时,测得 c(A)为 0.5molL1,温度不变的情况下,将容器体积增大一倍,当达到新的平衡时,测得 c(A)为 0.3molL1,则下列判断中正确的是
p C(g)反应达平衡时,测得 c(A)为 0.5molL1,温度不变的情况下,将容器体积增大一倍,当达到新的平衡时,测得 c(A)为 0.3molL1,则下列判断中正确的是
A. 平衡向正反应方向移动 B. 物质B的转化率减小
C. m + n <p D. 物质C的体积分数增加
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值。下列说法正确的是( )
A. 0.1molCH4和0.1molCl2充分反应,生成的C-Cl键和H-Cl键的数目均为0.2NA
B. 7.8gNa2S和Na2O2的混合物中所含阴离子的数目等于0.2NA
C. 18g固态水(冰)中含有的氢键的数目为2NA
D. 25℃时,Ksp(AgI)=1.0×10-16,则AgI饱和溶液中Ag+数目为1.0×10-8NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由相同金属电极及其不同浓度的盐溶液组成的电池,称浓差电池,电子由溶液浓度较小的一极流向浓度较大的一极。如图所示装置中,X电极与Y电极初始质量相等。进行实验时,先闭合K2,断开K1,一段时间后,再断开K2,闭合K1,即可形成浓差电池,电流计指针偏转。下列不正确的是( )
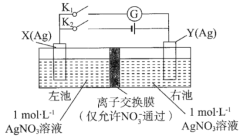
A. 充电前,该电池两电极存在电势差
B. 放电时,右池中的NO3-通过离了交换膜移向左池
C. 充电时,当外电路通过0.1 mol电子时,两电极的质量差为21.6g
D. 放电时,电极Y为电池的正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A是化学实验室中最常见的有机物,它易溶于水并有特殊香味;B的产量可以衡量一个国家石油化工发展的水平,有关物质的转化关系如图所示(部分反应条件、产物省略):(已知 2R-CHO + O2→2R-COOH R为烃基)
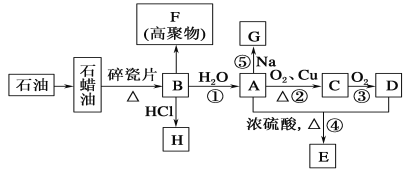
回答下列问题:
(1)①决定化合物A的化学特性的原子团的名称为________;F的结构简式为______________。
②B到A的反应类型为________,A到C的反应类型为________;
(2)写出下列反应的化学方程式:
反应②:______________________________________,
反应⑤:________________________________________。
(3)工业上制备H有以下两种方案:
Ⅰ.乙烷与氯气反应; Ⅱ.乙烯与氯化氢反应。
你认为最合理的方案是(填代号)________,理由是_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是
A. Na2CO3水解:CO32-+H2O == H2CO3+2OH-
B. NaHSO4溶液中滴加Ba(OH)2溶液至中性:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O
C. Cu与稀HNO3反应:Cu+4H++2NO3-=Cu2++2NO↑+2H2O
D. 醋酸除水垢:CO32-+2CH3COOH===2CH3COO-+CO2↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度时,向2.0 L恒容密闭容器中充入2 mol SO2和1 mol O2,发生反应:2SO2(g)+O2(g) ![]() 2SO3(g)。经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
2SO3(g)。经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
t / s | 0 | 2 | 4 | 6 | 8 |
n(SO3) / mol | 0 | 0. 8 | 1. 4 | 1.8 | 1.8 |
下列说法正确的是
A. 反应在前2 s 的平均速率v(O2) = 0. 4 mol·L-1·s-1
B. 保持其他条件不变,体积压缩到1.0 L,平衡常数将增大
C. 相同温度下,起始时向容器中充入4 mol SO3,达到平衡时,SO3的转化率大于10%
D. 保持温度不变,向该容器中再充入2 mol SO2、1 mol O2,反应达到新平衡时n(SO3)/n(O2)增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)一种熔融碳酸盐燃料电池原理示意如图:电池工作时,外电路上电流的方向应从电极___(“填A或B”)流向用电器。内电路中,CO32-向电极_____(“填A或B”)移动,电极A上CO参与的电极反应为______________________。

(2)将两铂片插入KOH溶液中作为电极,在两极区分别通入甲烷和氧气构成燃料电池,则通入甲烷气体的电极是原电池的____极,该极的电极反应式是___________。如果消耗甲烷160g,假设化学能完全转化为电能,需要消耗标准状况下氧气的体积为_______L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新型镁-锂双离子二次电池如图,下列关于该电池的说法不正确的是

A. 放电时,Li+由左向右移动
B. 放电时,正极的电极反应式为Li1-xFePO4+xLi++xe-= LiFePO4
C. 充电时,外加电源的正极与Y相连
D. 充电时,导线上每通过1mol e-,左室溶液质量减轻12g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA是阿伏加德罗常数的值,下列说法正确的是( )
A. 11g超重水(T2O)含中子数为5NA
B. 25℃,pH=13的1L Ba(OH)2溶液中OH—的数目为0.2NA
C. 1mol金刚石中C—C键的数目为2NA
D. 常温下,pH=6的MgCl2溶液中H+的数目为10-6NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com