
【题目】NA是阿伏加德罗常数的值,下列说法正确的是( )
A. 11g超重水(T2O)含中子数为5NA
B. 25℃,pH=13的1L Ba(OH)2溶液中OH—的数目为0.2NA
C. 1mol金刚石中C—C键的数目为2NA
D. 常温下,pH=6的MgCl2溶液中H+的数目为10-6NA
 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:高中化学 来源: 题型:
【题目】在密闭容器中,m A(g)+n B(g) ![]() p C(g)反应达平衡时,测得 c(A)为 0.5molL1,温度不变的情况下,将容器体积增大一倍,当达到新的平衡时,测得 c(A)为 0.3molL1,则下列判断中正确的是
p C(g)反应达平衡时,测得 c(A)为 0.5molL1,温度不变的情况下,将容器体积增大一倍,当达到新的平衡时,测得 c(A)为 0.3molL1,则下列判断中正确的是
A. 平衡向正反应方向移动 B. 物质B的转化率减小
C. m + n <p D. 物质C的体积分数增加
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】POCl3是重要的基础化工原料,广泛用于制药、染料、表面活性剂等行业。一种制备POCl3的原理为:PCl3+Cl2+SO2=POCl3+SOCl2。某化学学习小组拟利用如下装置在实验室模拟制备POCl3。有关物质的部分性质如下:
物质 | 熔点/℃ | 沸点/℃ | 密度/g·mL-1 | 其它 |
PCl3 | -93.6 | 76.1 | 1.574 | 遇水强烈水解,易与氧气反应 |
POCl3 | 1.25 | 105.8 | 1.645 | 遇水强烈水解,能溶于PCl3 |
SOCl2 | -105 | 78.8 | 1.638 | 遇水强烈水解,加热易分解 |

(1)仪器甲的名称为______________,与自来水进水管连接的接口编号是________________。(填“a”或“b”)。
(2)装置C的作用是___________________,乙中试剂的名称为____________________。
(3)该装置有一处缺陷,解决的方法是在现有装置中再添加一个装置,该装置中应装入的试剂为_________(写名称)。若无该装置,则可能会有什么后果?请用化学方程式进行说明__________________________。
(4)D中反应温度控制在60-65℃,其原因是_______________。
(5)测定POCl3含量。①准确称取30.70gPOCl3产品,置于盛有60.00mL蒸馏水的水解瓶中摇动至完全水解;②将水解液配成100.00mL溶液,取10.00mL溶液于锥形瓶中;③加入10.00mL3.200mol/LAgNO3标准溶液,并加入少许硝基苯用力摇动,使沉淀表面被有机物覆盖;④以Fe3+为指示剂,用0.2000mol/LKSCN溶液滴定过量的AgNO3溶液,达到滴定终点时共用去10.00mLKSCN溶液。
①滴定终点的现象为____________________,用硝基苯覆盖沉淀的目的是__________________。
②反应中POCl3的百分含量为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】配制100 mL0.020mol/L KMnO4溶液的过程如下图所示:
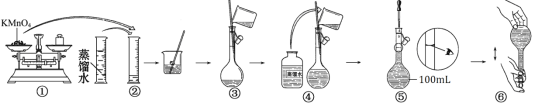
回答下列问题:
(1)图示中有两步操作不正确,它们是_____和_____ (填序号)。
(2)操作⑤图示中的两种仪器分别是________、 __________(填名称)。
(3)如果用图示的操作配制溶液,所配制的溶液浓度将_______(填“偏大”或“偏小”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列氮原子的电子排布图表示的状态中,能量由低到高的顺序是_______(填字母代号)。

(2)P4S3可用于制造火柴,其分子结构如图所示。
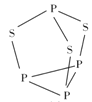
①P4S3分子中硫原子的杂化轨道类型为_______________。
②每个P4S3分子中含有的孤电子对的数目为__________________。
(3)科学家合成了一种阳离子“N5n+,其结构是对称的,5个N排成"V"形,每个N都达到8电子稳定结构,且含有2个氮氮三键;此后又合成了一种含有“N5n+”的化学式为”N8”的离子晶体,其电子式为_________________。分子(CN)2中键与键之间的夹角为180°,并有对称性,分子中每个原子的最外层均满是8电子稳定结构,其结构式为_____。
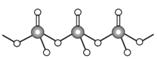
(4)直链多磷酸根阴离子是由两个或两个以上磷氧四面体通过共用顶角氧原子连接起来的,如图所示。则由n个磷氧四面体形成的这类磷酸根离子的通式为_________________。
(5)碳酸盐中的阳离子不同,热分解温度就不同。下表为四种碳酸盐的热分解温度和金属阳离子半径
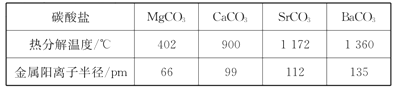
随着金属阳离子半径的增大,碳酸盐的热分解温度逐步升高,原因是_______________。
(6)石墨的晶体结构和晶胞结构如下图所示。已知石墨的密度为pgcm3,C—C键的键长为![]() cm,阿伏加德罗常数的值为NA,则石墨品体的层间距为_________cm。
cm,阿伏加德罗常数的值为NA,则石墨品体的层间距为_________cm。
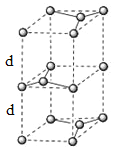
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家以MoS2为催化剂,在不同电解质溶液中实现常温电催化合成氨,其反应历程与相对能量模拟计算结果如图。下列说法错误的是( )
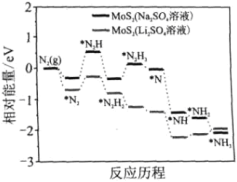
A. Li2SO4溶液利于MoS2对N2的活化
B. 两种电解质溶液环境下从N2→NH3的焓变不同
C. MoS2(Li2SO4溶液)将反应决速步(*N2→*N2H)的能量降低
D. N2的活化是N≡N键的断裂与N—H键形成的过程
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知草酸受热发生分解反应:H2C2O4![]() H2O+CO↑+CO2↑,某化学兴趣小组为验证草酸分解产物,设计如下实验:
H2O+CO↑+CO2↑,某化学兴趣小组为验证草酸分解产物,设计如下实验:

(1)按图连接好装置,检查气密性的方法是:_________________________________。
(2)实验中B中现象是:______________。
(3)已知C和E中装的是足量同种溶液,写出离子反应方程式:_________________。
(4)实验进行时D中黑色固体会逐渐变成红色。写出化学反应方程式:________________。
(5)实验过程中会有分解产生的气体经过D而未发生反应,采用F进行收集并测量气体体积,读数应注意____________________以便准确读出常压下的气体体积。
(6)某同学查资料了解到有如下反应:CO+PdCl2+H2O=CO2+Pd↓+2HCl,于是建议将浓硫酸换成PdCl2溶液并撤去D及后面的装置,实验完毕后预从PdCl2溶液中分离出固体并称量质量的实验操作依次为:_______,_______,_______,称量。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Fe(OH)3广泛应用于医药制剂、颜料制造等领域,其制备步骤及装置如下:在三颈烧瓶中加入16.7gFeSO4·7H2O和40.0ml蒸馏水。边搅拌边缓慢加入3.0mL浓H2SO4,再加入2.0gNaClO3固体。水浴加热至80℃,搅拌一段时间后,加入NaOH溶液,充分反应。经过滤、洗涤、干燥得产品。
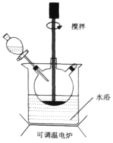
(1)NaClO3氧化FeSO4·7H2O的离子方程式为_____________。
(2)加入浓硫酸的作用为_________(填标号)。
a.提供酸性环境,增强NaClO3氧化性 b.脱去FeSO4·7H2O的结晶水
c.抑制Fe3+水解 d.作为氧化剂
(3)检验Fe2+已经完全被氧化需使用的试剂是_________。
(4)研究相同时间内温度与NaClO3用量对Fe2+氧化效果的影响,设计对比实验如下表
编号 | T/℃ | FeSO4·7H2O/g | NaClO3/g | 氧化效果/% |
i | 70 | 25 | 1.6 | a |
ii | 70 | 25 | m | b |
iii | 80 | n | 2.0 | c |
iv | 80 | 25 | 1.6 | 87.8 |
①m=______;n=______。
②若c>87.8>a,则a、b、c的大小关系为___________。
(5)加入NaOH溶液制备Fe(OH)3的过程中,若降低水浴温度,Fe(OH)3的产率下降,其原因是___
(6)判断Fe(OH)3沉淀洗涤干净的实验操作为_________________;
(7)设计实验证明制得的产品含FeOOH(假设不含其他杂质)。___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子被称为活化分子。使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJmol-1表示。请认真观察图1,然后回答问题。
(1)图中所示反应是________(填“吸热”或“放热”)反应。

(2)已知拆开1mol H﹣H键、1mol I﹣I、1mol H﹣I键分别需要吸收的能量为436kJ、151kJ、299kJ。则由1mol氢气和1mol 碘反应生成HI会________(填“放出”或“吸收”)________kJ的热量。在化学反应过程中,是将________转化为________。
(3)某实验小组同学进行如图2的实验,以探究化学反应中的能量变化。实验表明:①中的温度降低,由此判断氢氧化钡晶体与氯化铵晶体反应是________(填“吸热”或“放热”)反应;实验②中,该小组同学在烧杯中加入5mL 1.0mol/L盐酸,再放入用砂纸打磨过的铝条,该反应是________(填“吸热”或“放热”)反应。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com