
【题目】CO与N2O在铁催化剂表面进行如下两步反应,其相对能量与反应历程如图所示。
第一步:Fe*+N2O=FeO*+N2
第二步:FeO*+CO=Fe*+CO2
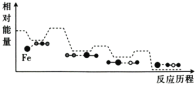
下列叙述错误的是( )
A.Fe*是反应的催化剂
B.两步反应的ΔH均小于0
C.第一步反应比第二步反应快
D.总反应为CO+N2O=N2+CO2
科目:高中化学 来源: 题型:
【题目】下列离子方程式与所述事实相符且正确的是
A.氯化铝溶液中加入过量氨水:Al3++4NH3·H2O=AlO+4NH+2H2O
B.Ca(HCO3)2溶液中加入过量NaOH溶液:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O
C.水玻璃中通入少量的二氧化碳:Na2SiO3+CO2+H2O=2Na++CO32-+H2SiO3↓
D.少量SO2通入漂白粉溶液中:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法不正确的是
A. CH2=CHCOOH、CH3COOCH=CH2均可作为合成聚合物的单体
B. C6Hn分子中的六个碳原子在同一直线上,则n可能等于2
C. 2,2-二甲基丁烷与2,4-二甲基戊烷的一氯代物种类相同
D.  与
与 都是酚且互为同系物
都是酚且互为同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮及其化合物是重要的化工原料
(1)利用图所示装置及药品制取氨气。
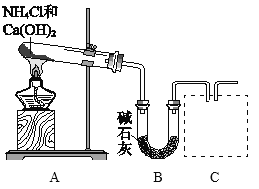
①A中制氨气的化学方程式是________。
②C处是用集气瓶收集氨气的装置,请绘出装置图。________
③证明氨气已集满的操作和现象是________。
(2)氨经催化氧化可制备硝酸,其过程中涉及如下反应。4NH3 + 5O2 ![]() 4NO + 6H2O
4NO + 6H2O
①作为氧化剂的物质是______,氮元素的化合价______(填“升高”或“降低”)。
②若反应中消耗了4 mol NH3,则生成NO的物质的量为______ mol,转移电子的物质的量为______ mol。
(3)含氮废水会加速藻类和其他浮游生物的大量繁殖,使水质恶化。利用微生物对含氮废水进行处理的流程如下:
![]()
请回答:
①过程Ⅲ发生化合反应的化学方程式为______。
②根据图1和图2,推断使用亚硝化菌的最佳条件为______。
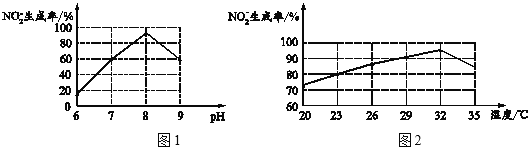
③利用微生物处理含氮废水的优点为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为氯及其化合物的“价-类”二维图。
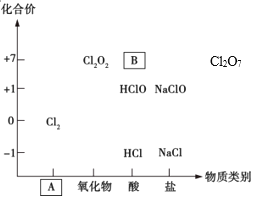
(1)填写二维图缺失的类别A_________和化学式B_________。
(2)某同学利用以下试剂研究HCl性质,进行了如下预测:
a.NaClO b.Fe c.NaOH d.KMnO4 e.AgNO3
从物质类别上看,HCl属于______,可能与__________发生反应(填序号);
从化合价角度看,Cl-具有______性,可能与_____发生反应(填序号)。
(3)某工厂用NaCl溶液制备氯气,其化学原理为如下反应:
![]() H2O +
H2O + ![]() NaCl == Cl2 +
NaCl == Cl2 + ![]() NaOH+
NaOH+![]()
①请将上述方程式补充完整,并用单线桥表示电子转移。_____________
②反应中NaCl作_________剂,理由是_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】B.[实验化学]
丙炔酸甲酯(![]() )是一种重要的有机化工原料,沸点为103~105 ℃。实验室制备少量丙炔酸甲酯的反应为
)是一种重要的有机化工原料,沸点为103~105 ℃。实验室制备少量丙炔酸甲酯的反应为
![]()
实验步骤如下:
步骤1:在反应瓶中,加入14 g丙炔酸、50 mL甲醇和2 mL浓硫酸,搅拌,加热回流一段时间。
步骤2:蒸出过量的甲醇(装置见下图)。
步骤3:反应液冷却后,依次用饱和NaCl溶液、5%Na2CO3溶液、水洗涤。分离出有机相。
步骤4:有机相经无水Na2SO4干燥、过滤、蒸馏,得丙炔酸甲酯。

(1)步骤1中,加入过量甲醇的目的是________。
(2)步骤2中,上图所示的装置中仪器A的名称是______;蒸馏烧瓶中加入碎瓷片的目的是______。
(3)步骤3中,用5%Na2CO3溶液洗涤,主要除去的物质是____;分离出有机相的操作名称为____。
(4)步骤4中,蒸馏时不能用水浴加热的原因是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na、Fe、Cl是中学化学常见的元素。回答下列问题:
(1)含上述元素的常见化合物中,呈淡黄色的是___(填化学式)。
(2)焰色反应的实验中,Na元素的焰色为___色,观察K元素的焰色需要透过___。
(3)实验室在制备Fe(OH)2时必须隔绝空气,否则发生的现象是___。
(4)MgO与碳粉和氯气在一定条件下反应可制备MgCl2,该反应的化学方程式为___。若尾气可用足量NaOH溶液完全吸收,则生成的盐为___(写化学式,只写一种)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂的工业废水中含有大量的FeSO4,较多的CuSO4和少量Na2SO4。为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。请根据下列流程图,完成回收硫酸亚铁和铜的实验方案。
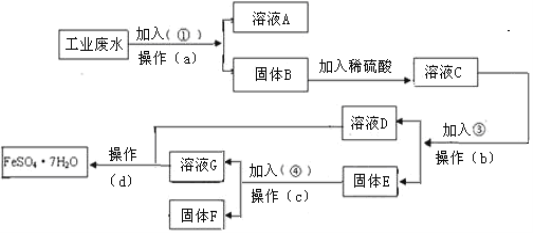
(1)若加入的试剂①为NaOH溶液,加入试剂①的目的___________________。
(2)操作a的名称为过滤、洗涤,所需要的玻璃仪器为烧杯、玻璃棒、_______。
(3)写出溶液C中加入试剂③发生反应的离子方程式为_______。
(4)写出固体E中加入试剂④发生反应的离子反应方程式为______________。
(5)从溶液D和溶液G中得到FeSO47H2O晶体的操作为蒸发浓缩、______、过滤、洗涤、干燥。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W为原子序数依次增大的四种短周期主族元素,W原子是同周期元素中原子半径最小的主族元素。已知A、B、C、D、E为上述四种元素中的两种或三种所组成的5种化合物间的转化关系如右图所示。A的相对分子质量为28,B分子中含有18个电子。下列有关说法错误的是( )

A.由W、Z、X三种元素组成的化合物一定是强酸
B.E能与金属钠反应产生气体
C.化合物D中含有极性键
D.最高价氧化物对应的水化物的酸性W最强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com