
【题目】用压强传感器探究生铁在pH=2和pH=4醋酸溶液中发生腐蚀的装置及得到的图象如下以下结论错误的是( )
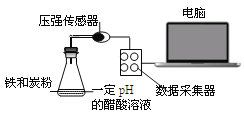
A.溶液pH≤2时,生铁发生析氢腐蚀
B.在酸性溶液中生铁不可能发生吸氧腐蚀
C.吸氧腐蚀的速率比析氢腐蚀快
D.两溶液中负极反应均为:Fe-2e-=Fe2+
【答案】D
【解析】
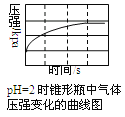
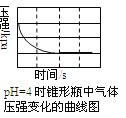
pH=2时由图可知压强随着反应的进行而增大,产生了大量气体,发生了析氢腐蚀,pH=4时压强随着反应的进行而减小,气体的量减少,发生了吸氧腐蚀,据此分析。
A. pH=2时由图可知压强随着反应的进行而增大,产生了大量气体,发生了析氢腐蚀,溶液pH≤2时,生铁发生析氢腐蚀,A项正确;
B. pH=4时压强随着反应的进行而减小,气体的量减少,发生了吸氧腐蚀,所以在酸性溶液中生铁可能发生析氢腐蚀也可能发生吸氧腐蚀,B项错误;
C.由两幅图可知变化相同的压强所用的时间不同,析氢腐蚀所用时间长而吸氧腐蚀所用的时间短,因而吸氧腐蚀的速率比析氢腐蚀快,C项正确;
D.不论是析氢腐蚀还是吸氧腐蚀,负极均为铁失电子,点击反应为:Fe-2e-=Fe2+,D项正确;
答案选B。


科目:高中化学 来源: 题型:
【题目】香豆素类化合物常用于治疗血栓性疾病,由 4-羟基香豆素(X)和苯代亚苄基丙酮(Y)反应可得到苯代苄丙酮香豆素(Z)。
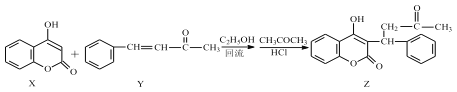
下列说法正确的是
A.X、Y 生成 Z 的反应为加成反应
B.Z 分子中所有碳原子可能共平面
C.1mol 化合物 X 最多能与 1mol NaOH 反应
D.1 mol 化合物 Y 最多能与 5 mol H2 发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
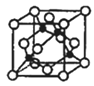
【题目】高温下超氧化钾晶体呈立方体结构,晶体中氧的化合价部分为0价,部分为﹣2价.如图所示为超氧化钾晶体的一个晶胞(晶体中最小的重复单元),则下列说法中正确的是

A. 晶体中每个K+周围有8个O2﹣,每个O2﹣周围有8个K+
B. 晶体中与每个K+距离最近的K+有8个
C. 超氧化钾的化学式为KO2,每个晶胞含有4个K+和4个O2﹣
D. 晶体中,0价氧与﹣2价氧的数目比为2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)FeCl3溶液呈_______性,原因是__________(用离子方程式表示)。把FeCl3溶液蒸干后并灼烧,最后得到的主要固体产物是_________。
(2)在25℃下,将a mol·L-1的CH3COOH与0.01 mol·L-1的NaOH等体积混合,反应平衡时溶液中c(CH3COO-)=c(Na+),则溶液显______ (填“酸”、“碱”或“中”)性;用含a的代数式表示CH3COOH的电离常数Ka=__________ 。
(3)已知298 K和101 kPa条件下:
N2(g)+3H2(g)=2NH3(g) ΔH1
2H2(g)+O2(g)=2H2O(l) ΔH2
2H2(g)+O2(g)=2H2O(g) ΔH3
4NH3(g)+O2(g)=2N2H4(l)+2H2O(l) ΔH4
则N2H4(l)的标准燃烧热ΔH=_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W 是四种原子序数依次增大的短周期元素,W 的最外层电子数比 X 的最外层电子数少1个,X、Y、Z为同一周期元素,X、Y、Z组成一种化合物(ZXY)2 的结构式如图所示。下列说法错误的是
![]()
A.化合物 WY 是良好的耐热冲击材料
B.Y的氧化物对应的水化物可能是弱酸
C.Y的简单氢化物的沸点一定高于 Z
D.化合物(ZXY)2 中所有原子均满足 8 电子稳定结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一真空密恒容闭容器中盛有1mol PCl5,加热到200℃时发生反应:PCl5(g)![]() PCl3(g)+Cl2(g),反应达到平衡时PCl5的分解率为M%,若在同一温度和同样容器中最初投入的是2mol PCl5,反应达到平衡时PCl5的分解率为N%。M与N的关系是
PCl3(g)+Cl2(g),反应达到平衡时PCl5的分解率为M%,若在同一温度和同样容器中最初投入的是2mol PCl5,反应达到平衡时PCl5的分解率为N%。M与N的关系是
A.M>NB.M<NC.M=ND.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质中,既能因发生化学反应使溴水褪色,又能使酸性KMnO4溶液褪色的是( )
①SO2 ②CH3CH2CH=CH2 ③![]() ④CH3CH3
④CH3CH3
A. ①②③④B. ②③C. ②④D. ①②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁、铜及其化合物在日常生产、生活有着广泛的应用。请回答下列问题:
(1)铁在元素周期表中的位置是______,基态铜原子的核外电子排布式为______。
(2)配合物Fe(CO)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于______![]() 填晶体类型
填晶体类型![]() 。
。
(3)写出CO的一种常见等电子体分子的结构式______,两者相比较沸点较高的为______(填化学式)。CN-中碳原子杂化轨道类型为______,C、N、O三元素的第一电离能最大的为______![]() 用元素符号表示
用元素符号表示![]() 。
。
(4)铜晶体中铜原子的堆积方式如图所示:

M原子的价电子排布式为3s23p5,铜与M形成化合物的晶胞如图所示(黑点代表铜原子)。
![]() 该晶体的化学式为______。
该晶体的化学式为______。
![]() 已知铜和M的电负性分别为1.9和3.0,则铜与M形成的化合物属于______(填“离子”、“共价”)化合物。
已知铜和M的电负性分别为1.9和3.0,则铜与M形成的化合物属于______(填“离子”、“共价”)化合物。
![]() 已知该晶体的密度为
已知该晶体的密度为![]() gcm-3,阿伏伽德罗常数为NA,已知该晶体中铜原子和M原子之间的最短距离为体对角线的
gcm-3,阿伏伽德罗常数为NA,已知该晶体中铜原子和M原子之间的最短距离为体对角线的![]() ,则该晶体中铜原子和M原子之间的最短距离为______pm(只写计算式)。
,则该晶体中铜原子和M原子之间的最短距离为______pm(只写计算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)依据反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如下图甲所示。

①电极X的材料是_________________;
②外电路中的电子是从___电极流向__电极(填电极材料名称或符号)。
③在电池放电过程中,盛有饱和KCl琼脂溶胶的盐桥中,向CuSO4溶液一端扩散的离子是___________(填离子符号)。
(2)①金属腐蚀一般可分为化学腐蚀和电化学腐蚀。炒过菜的铁锅未及时清洗容易发生电化学腐蚀而生锈。请写出铁锅生锈过程的正极反应式:____________________。
②为了减缓某水库铁闸门被腐蚀的速率,可以采用下图乙所示的方案,其中焊接在铁闸门上的固体材料R可以采用__________(填写字母序号)。
A.铜 B.钠 C.锌 D.石墨
③图丙所示方案也可以减缓铁闸门的腐蚀速率,则铁闸门应连接直流电源的____极。
(3)蓄电池是一种可以反复充电、放电的装置。有一种蓄电池在充电和放电时发生的反应是:NiO2+ Fe + 2H2O![]() Fe(OH)2+ Ni(OH)2。
Fe(OH)2+ Ni(OH)2。
①若此蓄电池放电时,该电池某一电极发生还原反应的物质是__(填序号)。
A.NiO2B.Fe C.Fe(OH)2D.Ni(OH)2
②该电池放电时,正极附近溶液的pH________(填增大、减小、不变)
③充电时该电池阳极的电极反应式___________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com