
【题目】(1)在25℃、101kPa下,一定质量的无水乙醇完全燃烧时放出热量Q kJ,其燃烧生成的CO2用过量饱和石灰水吸收可得100gCaCO3沉淀,则乙醇燃烧的热化学方程式为___。
(2)已知下列热化学方程式
Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) ΔH1= -25kJ·mol-1 ①
3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) ΔH2= -47kJ·mol-1 ②
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) ΔH3= +19kJ·mol-1 ③写出FeO(s)被CO还原成Fe和CO2的热化学方程式____。
(3)向足量H2SO4溶液中加入100mL 0.4mol·L-1Ba(OH)2溶液,放出的热量是5.12kJ。如果向足量Ba(OH)2溶液中加入100mL 0.4mol·L-1盐酸时,放出的热量为2.2kJ。则Na2SO4溶液与BaCl2溶液反应的热化学方程式为___。
【答案】C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l) ΔH= -2Q kJ/mol FeO(s)+CO(g)=Fe(s)+CO2(g) ΔH= -11kJ·mol-1 Ba2+(aq)+SO42-(aq)=BaSO4(s) ΔH= -18kJ·mol-1
【解析】
(1)因生成的CO2用过量饱和石灰水完全吸收,可得100g CaCO3沉淀,CaCO3的物质的量是1mol,由碳元素守恒可知,二氧化碳的物质的量也为1mol,即生成1mol二氧化碳放出的热量为Q,而完全燃烧1mol无水乙醇时生成2mol二氧化碳,则放出的热量为Q×2=2Q,热化学方程式为:C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l) ΔH= -2Q kJ/mol;
(2)①Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g);ΔH= -25kJ/mol,
②3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g);ΔH= -47kJ/mol,③Fe3O4(s)+CO(g)=3FeO(s)+CO2(g);ΔH= +19kJ/mol,
依据盖斯定律①×3-(③×2+②)得到:6CO(g)+6FeO(s)=6Fe(g)+6CO2(g) ΔH= -66kJ/mol;得到热化学方程式为:CO(g)+FeO(s)=Fe(s)+CO2(g) ΔH= -11kJ/mol;
(3)100mL 0.4mol·L-1 Ba(OH)2的物质的量为0.04mol,向H2SO4溶液中加入100mL 0.4mol·L-1 Ba(OH)2溶液反应涉及的离子方程式有Ba2+(aq)+SO42-(aq)=BaSO4(s),H+(aq)+OH(aq)=H2O(l),100mL 0.4mol·L-1HCl的物质的量为0.04mol,反应涉及的离子方程式为H+(aq)+OH(aq)=H2O(l),根据放出的热量为2.2kJ,可知H+(aq)+OH(aq)=H2O(l) ΔH= -![]() = -55kJmol-1,设Ba2+(aq)+SO42-(aq)=BaSO4(s) ΔH= -Q kJ·mol-1,则0.04Q+0.08mol×55kJ·mol-1=5.12kJ,解之得Q=18,所以Na2SO4溶液与BaCl2溶液反应的热化学方程式为Ba2+(aq)+SO42- (aq)=BaSO4(s) ΔH= -18 kJ·mol-1。
= -55kJmol-1,设Ba2+(aq)+SO42-(aq)=BaSO4(s) ΔH= -Q kJ·mol-1,则0.04Q+0.08mol×55kJ·mol-1=5.12kJ,解之得Q=18,所以Na2SO4溶液与BaCl2溶液反应的热化学方程式为Ba2+(aq)+SO42- (aq)=BaSO4(s) ΔH= -18 kJ·mol-1。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】硫酸铝铵[Ala(NH4)b(SO4)c.xH2O]又叫做明矾、宝石明矾,其相对分子质量为906,常用作净水剂和制造人工刚玉(γ-Al2O3)
(1)[Ala(NH4)b(SO4)c.xH2O]中a、b、c的代数关系式是_________。
(2)硫酸铝铵受热最终分解为Al2O3、H2O、NH3和另外一种气体的分子式是_______。
(3)为确定硫酸铝铵的组成,进行如下实验:
①明确称取4.530g样品与足量氯化钡溶液充分反应,生成白色沉淀4.660g
②另取4.530g样品在空气中加热,样品的固体残留率(![]() ×100%)随温度的变化如图所示:
×100%)随温度的变化如图所示:
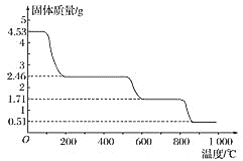
根据以上实验数据计算硫酸铝铵的分子式_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组的同学学习了同周期元素性质的递变规律后,设计了一套实验方案进行实验探究,并记录了有关实验现象,如下表。

请你帮助该同学整理并完成实验报告。
(1)实验目的:__________________。
(2)实验仪器:①________;②________;③________;④试管夹;⑤镊子;⑥小刀;⑦玻璃片;⑧砂纸;⑨胶头滴管等。
(3)实验药品:钠、镁带、铝条、2 mol·L-1盐酸、新制的氯水、硫化氢饱和溶液、氯化铝溶液、氢氧化钠溶液等。
(4)请你写出上述的实验操作对应的现象(用A~F表示):
①________;②________;③________;④________;⑤________;⑥________。
(5)写出实验操作②、⑥中有关反应的离子方程式:
实验②________________________,实验⑥______________________。
(6)实验结论:__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子序数为x的元素E在周期表中位于A、B、C、D四种元素中间(如图所示),则A、B、C、D四种元素的原子序数之和不可能是(镧系、锕系、0族元素除外)( )
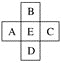
A. 4xB. 4x+14
C. 4x+10D. 4x+6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制取氯气,将多余的氯气用100 mL 1.7mol/L的NaOH溶液完全吸收。对吸收后的溶液进行分析化验,测知c(OH-)=0.1mol/L (不考虑反应前后溶液的体积变化) 。ClO-和ClO3-的物质的量浓度之比为5∶1。请回答:
(1)吸收氯气消耗的NaOH的物质的量为_______________mol。
(2)被氧化的氯气的物质的量为_______________mol,被还原的氯气的物质的量为 _______________mol。
(3)若采用二氧化锰和浓盐酸共热的方法制氯气,制备尾气中的氯气所消耗的二氧化锰的质量为_______________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸钴是制作氧化钴和金属钴的原料。一种利用含钴废料(主要成分为Co2O3,含少量Fe2O3、Al2O3、CaO、MgO、碳及有机物等)制取CoC2O4的工艺流程如图
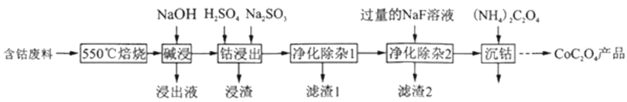
(1)“550℃焙烧”的目的是___;
(2)“浸出液”的主要成分是___;
(3)“钴浸出”过程中Co3+转化为Co2+,反应的离子方程式为___;
(4)“净化除杂1”过程中,先在4050℃加入H2O2,其作用是___(用离子方程式表示);再升温至8085℃,加入Na2CO3溶液,调pH至4.5,“滤渣1”主要成分的是___.
(5)“净化除杂2”可将钙、镁离子转化为沉淀过滤除去,若所得滤液中c(Ca2+)=1.0×l05mol/L,则滤液中c(Mg2+)为___[已知Ksp(MgF2)=7.35×1011、Ksp(CaF2)=1.05×1010.]
(6)为测定制得样品的纯度,现称取1.00g样品,将其用适当试剂转化,得到草酸铵[(NH4)2C2O4]溶液,再用过量稀硫酸酸化,用0.1000mol/LKMnO4溶液滴定,达到滴定终点时,共用去KMnO4溶液26.00mL,则草酸钴样品的纯度为___.(保留两位小数)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有三个热化学方程式:
(1)CH3COOH(l)+2O2(g)===2CO2(g)+2H2O(l) ΔH1=-870.3 kJ/mol
(2)C(s)+O2(g)===CO2(g) ΔH2=-393.5 kJ/mol
(3)H2(g)+![]() O2(g)===H2O(l) ΔH3=-285.8 kJ/mol
O2(g)===H2O(l) ΔH3=-285.8 kJ/mol
则反应2C(s)+2H2(g)+O2(g)===CH3COOH(l)的反应热为( )
A. -488.3 kJ/mol B. +488.3 kJ/mol
C. -2 228.9 kJ/mol D. +191 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知CH3OH(l)的燃烧热ΔH=-238.6kJ/mol,CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(g) ΔH=-a kJ/mol,则a__238.6(填“>”、“<”或“=”)。
(2)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1mol Cl2参与反应时释放出145kJ热量,写出该反应的热化学方程式:____。
(3)反应mA(g)+nB(g)![]() pC(g)+qD(g)过程中的能量变化如图所示,回答下列问题。
pC(g)+qD(g)过程中的能量变化如图所示,回答下列问题。
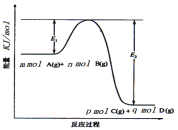
该反应ΔH=___(用含E1、E2式子表示);在反应体系中加入催化剂,E1__,E2__,(填增大、减小、不变)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海军成立68周年时,我国第一艘国产航母成功下水。建造航母需要大量的新型材料。航母的龙骨要耐冲击,航母的甲板要耐高温,航母的外壳要耐腐蚀。
(1)镍铬钢就是抗腐蚀性能强的新型材料。
①基态Ni原子的电子排布式为________________,铬元素在周期表中____区。
②Ni能与CO形成正四面体形的配合物Ni(CO)4,1 mol Ni(CO)4中含有________ mol σ键。
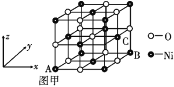
③NiO的晶体结构如图甲所示,其中离子坐标参数 A 为(0,0,0),B为(1,1,0),则C离子坐标参数为____。
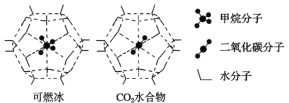
(2)海洋底部有储量丰富的可燃冰,一定条件下,CH4、CO2都能与H2O形成笼状结构(如下图所示)的水合物晶体,其相关参数见下表。CH4与H2O形成的水合物晶体俗称“可燃冰”。
参数 分子 | 分子直径/nm | 分子与H2O的结合能 E/kJ·mol-1 |
CH4 | 0.436 | 16.40 |
CO2 | 0.512 | 29.91 |
①“可燃冰”中分子间存在的2种作用力是_____________________。
②为开采深海海底的“可燃冰”,有科学家提出用CO2置换CH4的设想。已知如图中笼状结构的空腔直径为0.586 nm,根据上述图表,从物质结构及性质的角度分析,该设想的依据是___________________________________。
(3)①CH4和CO2所含的三种元素电负性从小到大的顺序为_______________
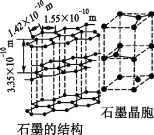
②碳的另一种同素异形体——石墨,其晶体结构如图所示,则石墨晶胞含碳原子个数为____个.已知石墨的密度为ρ g·cm—3,C—C键长为r cm,阿伏加德罗常数的值为NA,计算石墨晶体的层间距为__________cm。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com