
����Ŀ��T��ʱ��2L�ܱ�������ʹX(g)��Y(g)������Ӧ����Z(g)����Ӧ������X��Y��Z����
�ʵ����仯��ͼ-1��ʾ�������������������䣬�¶ȷֱ�ΪT1��T2��Y������ٷֺ�����ʱ��Ĺ�ϵ��ͼ-2��ʾ�����з�����ȷ����
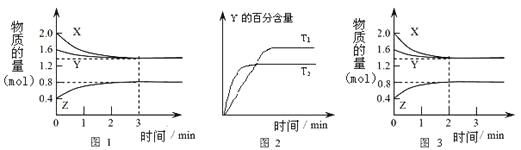
A.�����з����ķ�Ӧ�ɱ�ʾΪ��3X(g)��Y(g)![]() 2Z(g)
2Z(g)
B.0��3 min�ڣ�v(X)��0.2 molL-1min-1
C.�����������������¶ȣ�v����v��������������ƽ��ǰv����v��
D.���ı�������ʹ��Ӧ������ͼ-3��ʾ����ı����������������ѹǿ
���𰸡�AC
��������
A������ͼ1��֪��X��Y�Ƿ�Ӧ�Z�����������Ӧ����3min��������ʵ�Ũ�ȶ��������ı䣬��Ӧ����ƽ��״̬�����ǵ����ʵ����ı�ֵ�ǣ�X��0.6mol��Y��0.2mol;Z��0.4mol�����Է�Ӧʱ���ʵ����ı��ǣ�3:1:2���������з����ķ�Ӧ�ɱ�ʾΪ��3X(g)��Y(g)![]() 2Z(g)����ȷ��
2Z(g)����ȷ��
B��0��3 min�ڣ�v(X)��0.6mol ��2L��3min="0.1" molL-1min-1������
C������ͼ2��֪�����¶���T2ʱ���ȴﵽƽ�⣬˵�����ʸߣ���Ӧ�죬�¶�T2>T1�������������������¶ȣ�ƽ��ʱY�ĺ������ͣ�˵��ƽ�������ƶ�����v����v��������������ƽ��ǰv��>v������ȷ��
D�����ı�������ʹ��Ӧ������ͼ-3��ʾ����֪�ﵽƽ������Ҫ��ʱ�����̣�����ƽ��ʱ���ʵ���û�䣬˵��ƽ�ⲻ�����ƶ������ڸ÷�Ӧ�Ƿ�Ӧǰ������������ȵķ�Ӧ��������ı�����������Ǽ��������������˵����ѹǿ������
��ѡAC��


 ��Ȥ����¹�֪��ϵ�д�
��Ȥ����¹�֪��ϵ�д� Ӣ��СӢ������Ĭдϵ�д�
Ӣ��СӢ������Ĭдϵ�д� �����ҵ���������ͯ������ϵ�д�
�����ҵ���������ͯ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȫ��Һ�������һ�����͵���ɫ�������ܵ�ء������ܷ�ӦΪ��
![]() ������˵����ȷ����
������˵����ȷ����
A.�ŵ�ʱ������ӦΪ��![]()
B.���ʱ������ӦΪ��![]()
C.�ŵ�����е����ɸ��������·���������������������������Һ����
D.�������У�H+����������������Ǩ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪AG=lg![]() ���������=
���������=![]() ��100%�������£���10mL0.1mol/LHX��Һ�еμ�0.1mol/LNaOH��Һ�������Һ��AG��μ�NaOH��Һ����Ĺ�ϵ��ͼ��ʾ��
��100%�������£���10mL0.1mol/LHX��Һ�еμ�0.1mol/LNaOH��Һ�������Һ��AG��μ�NaOH��Һ����Ĺ�ϵ��ͼ��ʾ��
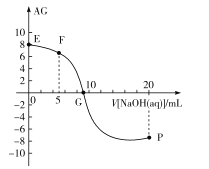
����˵��������ǣ� ��
A.F����ҺpH<7
B.G����Һ��c(Na+)=c��X-��>c(H+)=c��OH-��
C.V=10ʱ����Һ��c��OH-��<c(HX)
D.�����£�HX�ĵ����ԼΪ1%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Ķ����в��ϣ��������С�⡣
������ᾭ�õķ�չ�������ѽ���ǧ�����������dz��д��������ͬʱ����β����Ⱦ����Ҳ����ͻ�ԣ�����β���к�NO��NO2��CO2��SO2�������������ȡ��û���̿��ԭ��������������һ��ʵ�õĵ�������ת��������C(s)��2NO(g) ![]() N2(g)��CO2(g)����ʵ�ֵ���������ת����
N2(g)��CO2(g)����ʵ�ֵ���������ת����
��1�����л�������������β���Ĵ����ŷ��ص���
A.����B.����ЧӦC.PM2.5����D.��ɫ��Ⱦ
��2���÷�Ӧ���ڻ�ѧ������Ӧ�����е�
A.���Ϸ�ӦB.�ֽⷴӦC.�û���ӦD.���ֽⷴӦ
��3���÷�Ӧ����������ԭ��Ӧ������˵����ȷ��
A.CԪ�ر���ԭB.NO�õ�����C.NO����������ӦD.CO2��������
��4�����ڸ÷�Ӧ����˵������ȷ����
A.�����¶��ܹ��ӿ췴Ӧ����
B.����NOŨ���ܹ�������Ӧ����
C.ʹ�ú��ʵĴ������Լӿ췴Ӧ����
D.����������̿�ۿ���ʹNO 100%ת��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��Ӧ��2NO(g)��Br2(g)![]() 2NOBr(g) ��H=��a kJ��mol��1 (a>0)���䷴Ӧ��������
2NOBr(g) ��H=��a kJ��mol��1 (a>0)���䷴Ӧ��������
��NO(g)��Br2(g)![]() NOBr2(g) �� ��NO(g)��NOBr2(g)
NOBr2(g) �� ��NO(g)��NOBr2(g)![]() 2NOBr(g) ��
2NOBr(g) ��
�����йظ÷�Ӧ��˵����ȷ���ǣ� ��
A. �÷�Ӧ��������Ҫȡ���ڢٵĿ���
B. NOBr2�Ǹ÷�Ӧ�Ĵ���
C. ����Ӧ�Ļ�ܱ��淴Ӧ�Ļ��Сa kJ��mol��1
D. ����Br2(g)Ũ�����������Ӱٷ���, �ӿ췴Ӧ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ����С���ͬѧ��ѧϰNH3������ʱ���ۣ���ȻNH3���л�ԭ�ԣ��ܷ���H2������ԭCuO�أ������������������ʵ��װ�ã��г�װ��δ����������ʵ�顣
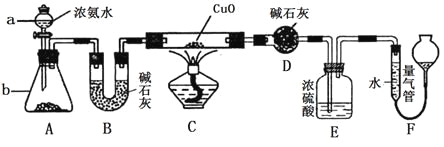
��ش��������⣺
��1������a������Ϊ______________������b�п�ѡ����Լ�Ϊ______________��
��2��ʵ���й۲쵽װ��C�к�ɫCuO��ĩ��Ϊ��ɫ���壬�����D���أ����������ռ�����ɫ��ζ�ĵ������壬�����������֤��NH3����________�ԣ�д����Ӧ�Ļ�ѧ����ʽ_____________��
��3��Eװ����Ũ�����������________________________________
��4����ȡ�������ǰ��Ӧ��װ��F���еIJ����ǣ�________________________������ʱ���������е�Һ�����ˮ�ܵ�Һ�棬��������������������_____��������ƫ��������ƫС����������������
��5����ͬѧ��Ϊ��NH3��CuO��Ӧ���ɵĺ�ɫ�����п��ܺ���Cu2O����֪��Cu2O��һ�ּ����������������Һ�У�Cu+����������������ԭ��Ӧ��2Cu+��Cu+Cu2+�����������һ����ʵ�����ú�ɫ�������Ƿ���Cu2O��_______________________________��
��6������ʵ��װ�û������ڲⶨ�����ķ�����ɡ���ʵ����ϣ���ø����D����m�ˣ�װ��F�����������Ϊn����������ɱ�״�����������е������ԭ�Ӹ�����Ϊ________���ú�m��n��ĸ�Ĵ���ʽ��ʾ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶��£���10 mL 0.1 mol/LCuCl2��Һ�еμ�0.1 mol/L��Na2S��Һ���μӹ�������Һ��lgc(Cu2+)��Na2S��Һ���(V)�Ĺ�ϵ��ͼ��ʾ�������й�˵����ȷ����

��֪��lg2��0.3��Ksp(ZnS)=3��10-25 mol2/L2��
A. a��b��c�����У�ˮ�ĵ���̶�����Ϊb��
B. Na2S��Һ�У�c(H+)+c(HS-)+c(H2S)= c(OH-)
C. ���¶���Ksp(CuS)=4��10-36 mol2/L2
D. ��100 mL Zn2+��Cu2+Ũ�Ⱦ�Ϊ10-5 molL-1�Ļ����Һ����μ���10-4 molL-1��Na2S��Һ��Zn2+�ȳ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��pH=a��ij�������Һ�У�������֧���Ե缫��ֱͨ����һ��ʱ�����Һ��pH��a����õ���ʿ�����
A. Na2SO4 B. H2SO4 C. AgNO3 D. NaCl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����13.6g Cu��Cu2O�Ļ�����м���ijŨ�ȵ�ϡ����0.25 L������������ȫ��Ӧ������NO��Cu(NO3)2����������Һ�м���0.5 mol/L��NaOH��Һ1 L����Ӧ����Һǡ�ó����ԣ�������������ȫ��������������Ϊ19.6 g������˵������ȷ����
A.Cu��Cu2O�����ʵ���֮��Ϊ2��1
B.��������ʵ���Ũ��Ϊ2 mol/L
C.Cu��Cu2O�����ᷴӦ��ʣ��HNO3�����ʵ���Ϊ0.5 mol
D.������NO�ڱ�״���µ����Ϊ2.24 L
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com