
ЁОЬтФПЁПСђЧшЫсбЮЁЂБНЗгМАСђДњСђЫсбЮЪЧHPFЭбСђЗЯвКжаЕФжївЊЮлШОЮя(ЦфжаЛЙКЌгаClЃЁЂSO![]() ЁЂNaЃЋЕШ)ЃЌПЩгУNaClO3ЁЂH2SO4зїЭбГ§ЕФЪдМСЁЃ
ЁЂNaЃЋЕШ)ЃЌПЩгУNaClO3ЁЂH2SO4зїЭбГ§ЕФЪдМСЁЃ
ЃЈ1ЃЉCl2гыШШЕФNaOHШмвКЗДгІЩњГЩNaClO3ЃЌИУЗДгІЕФЛЏбЇЗНГЬЪНЮЊ____________________________ЁЃ
ЃЈ2ЃЉ ГЃЮТЪБЃЌЗДгІC6H5OЃЃЋH2O ![]() C6H5OHЃЋOHЃЕФЦНКтГЃЪ§ЮЊKЃН________(C6H5OHЕФKaЃН1ЁС10Ѓ10)ЁЃ
C6H5OHЃЋOHЃЕФЦНКтГЃЪ§ЮЊKЃН________(C6H5OHЕФKaЃН1ЁС10Ѓ10)ЁЃ
ЃЈ3ЃЉДІРэИУЗЯЫЎашОдЄДІРэКЭдйДІРэНзЖЮЁЃ
ЂйгУХЈСђЫсЖд600 mL HPFЭбСђЗЯвКНјааЫсЛЏдЄДІРэ(ЗДгІЮТЖШ100Ёц)ЃЌЦфНсЙћШчБэ1ЫљЪОЃК
Бэ1ЁЁдЄДІРэЧАКѓШ§жжРызгХЈЖШБфЛЏЧщПі
ЯюФП | S2O | SCNЃ(gЁЄLЃ1) | БНЗг(gЁЄLЃ1) | pH |
ДІРэЧА | 34.28 | 70.11 | 1.3 | 8.55 |
ДІРэКѓ | 0.91 | 69.76 | 1.35 | 2.4 |
гЩБэ1ПЩжЊЃЌИУДІРэЙ§ГЬжажївЊБЛГ§ШЅЕФЮлШОЮяЪЧ________ЁЃ
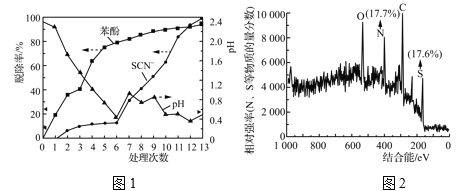
ЂкЖддЄДІРэКѓЗЯвКНјаадйДІРэ(ЗДгІЮТЖШ100 Ёц)ЪБЃЌ13ДЮвРДЮЯђЗЯвКжаМгШыЪдМСЧщПіШчБэ2ЫљЪОЃК
Бэ2ЁЁ13ДЮвРДЮМгШыЪдМСЧщПі
ДЮЪ§ | 1 | 2 | 3 | 4 | span>5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 |
NaClO3/g | 16.3 | 0 | 0 | 0 | 0 | 0 | 7.6 | 0 | 5.7 | 0 | 10.9 | 0 | 7.1 |
ХЈH2SO4/mL | 0 | 2 | 2 | 2 | 4 | 4 | 0 | 4 | 0 | 4 | 0 | 4 | 0 |
ЪЕбщНсЙћШчЭМ1ЫљЪОЃК
ЧА![]() КЭClЃЗДгІВњЩњCl2гаЙиЁЃИУАзЩЋГСЕэПЩФмЕФНсЙЙМђЪНЮЊ______________ЁЃ
КЭClЃЗДгІВњЩњCl2гаЙиЁЃИУАзЩЋГСЕэПЩФмЕФНсЙЙМђЪНЮЊ______________ЁЃ
ЂлгЩБэ2КЭЭМ1жаЪ§ОнЕУГіЃЌЕк7ЁЋ13ДЮВйзїжаSCNЃдкНЯЧПЫсадЬѕМўЯТБЛClO![]() (ВЛЫЎНт)бѕЛЏЕФвРОнЪЧ________ЁЃДЫЙ§ГЬжаВњЩњДѓСПзЉКьЩЋГСЕэ(МадгЩйСПАзЩЋГСЕэ)ЃЌЖдГСЕэНјааXPSЗжЮіЃЌВПЗждЊЫиЕФЮяжЪЕФСПЗжЪ§ШчЭМ2ЫљЪОЁЃвбжЊSCNЃПЩБЛФГаЉбѕЛЏМС(ШчCu2ЃЋЕШ)зюжебѕЛЏЮЊзЉКьЩЋЕФГСЕэ(SCN)xЁЃвЛжжЭЦВтШЯЮЊИУЪЕбщжаВњЩњЕФзЉКьЩЋГСЕэЮЊ(SCN)xЃЌжЇГжИУЭЦВтЕФжЄОнгаЃК________ЁЃ
(ВЛЫЎНт)бѕЛЏЕФвРОнЪЧ________ЁЃДЫЙ§ГЬжаВњЩњДѓСПзЉКьЩЋГСЕэ(МадгЩйСПАзЩЋГСЕэ)ЃЌЖдГСЕэНјааXPSЗжЮіЃЌВПЗждЊЫиЕФЮяжЪЕФСПЗжЪ§ШчЭМ2ЫљЪОЁЃвбжЊSCNЃПЩБЛФГаЉбѕЛЏМС(ШчCu2ЃЋЕШ)зюжебѕЛЏЮЊзЉКьЩЋЕФГСЕэ(SCN)xЁЃвЛжжЭЦВтШЯЮЊИУЪЕбщжаВњЩњЕФзЉКьЩЋГСЕэЮЊ(SCN)xЃЌжЇГжИУЭЦВтЕФжЄОнгаЃК________ЁЃ
ЁОД№АИЁП 3Cl2 ЃЋ 6NaOH![]() NaClO3ЃЋ5NaClЃЋ3H2O 1ЁС10Ѓ4 S2O
NaClO3ЃЋ5NaClЃЋ3H2O 1ЁС10Ѓ4 S2O![]() (СђДњСђЫсбЮ) ClClOHCl(ЛђClOHClЁЂClOHЕШ Ек7ЁЂ9ЁЂ11ЁЂ13ДЮМгШыNaClO3ЪБЃЌpHУїЯддіДѓЃЌSCNЃЭбГ§ТЪЯргІдіДѓ(ЛђЃК7ЁЋ13ДЮМгШыNaClO3ЪБSCNЃЭбГ§ТЪУїЯддіДѓЃЌЖјБНЗгЭбГ§ТЪдіДѓВЛУїЯд) SCNЃПЩБЛФГаЉбѕЛЏМС(ШчCu2ЃЋЕШ)бѕЛЏЮЊзЉКьЩЋЕФГСЕэЃЌClO
(СђДњСђЫсбЮ) ClClOHCl(ЛђClOHClЁЂClOHЕШ Ек7ЁЂ9ЁЂ11ЁЂ13ДЮМгШыNaClO3ЪБЃЌpHУїЯддіДѓЃЌSCNЃЭбГ§ТЪЯргІдіДѓ(ЛђЃК7ЁЋ13ДЮМгШыNaClO3ЪБSCNЃЭбГ§ТЪУїЯддіДѓЃЌЖјБНЗгЭбГ§ТЪдіДѓВЛУїЯд) SCNЃПЩБЛФГаЉбѕЛЏМС(ШчCu2ЃЋЕШ)бѕЛЏЮЊзЉКьЩЋЕФГСЕэЃЌClO![]() ОпгаНЯЧПЕФбѕЛЏадЃЌSCNЃвВПЩБЛClO
ОпгаНЯЧПЕФбѕЛЏадЃЌSCNЃвВПЩБЛClO![]() бѕЛЏЃЌГСЕэжаNЁЂSЮяжЪЕФСПжЎБШМИКѕЮЊ1ЁУ1ЧвЛЙКЌC
бѕЛЏЃЌГСЕэжаNЁЂSЮяжЪЕФСПжЎБШМИКѕЮЊ1ЁУ1ЧвЛЙКЌC
ЁОНтЮіЁП(1)вРЬтвтПЩЕУCl2гыШШЕФNaOH ШмвКЗДгІЕФЛЏбЇЗНГЬЪНЮЊ3Cl2+6NaOHNaClO3+ 5NaCl+3H2OЃЛ
(2)вбжЊC6H5OHЕФKa=1ЁС10-10ЃЌдђЗДгІC6H5O-+H2O![]() C6H5OH+OH -ЕФЦНКтГЃЪ§ЮЊK=
C6H5OH+OH -ЕФЦНКтГЃЪ§ЮЊK=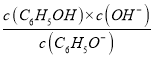 =
= 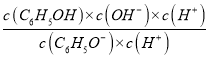 =
= ![]() = 1ЁС10-4ЃЛ
= 1ЁС10-4ЃЛ
(3) ЂйгЩБэ-1Ъ§ОнЕФБфЛЏПЩжЊЃЌИУДІРэЙ§ГЬжажївЊБЛГ§ШЅЕФЮлШОЮяЪЧS2O32-ЃЈСђДњСђЫсбЮЃЉЃЛЂкШмвКжаClO3-КЭCl-ЗДгІВњЩњЕФCl2ФмгыБНЗгЗДгІЩњГЩШ§ТШБНЗгАзЩЋГСЕэЃЌЦфНсЙЙМђЪНЮЊ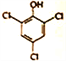 ЃЛЂлгЩЭМ1ПЩжЊЃЌЫцNaClO3МгШыЃЌpHдіДѓЃЌSCN-ЭбГ§ТЪУїЯддіДѓЃЌЖјБНЗгЭбГ§ТЪдіДѓВЛУїЯдЃЌЫљвдSCN-дкНЯЧПЫсадЬѕМўЯТБЛClO3-бѕЛЏСЫЃЛгЩЬтФПа№ЪіПЩжЊSCN-ПЩБЛФГаЉбѕЛЏМСЃЈШчCu2+ЕШЃЉбѕЛЏЮЊзЉКьЩЋЕФГСЕэЃЌClO3-ОпгаНЯЧПЕФбѕЛЏадЃЌгЩЭМЯѓ2ПЩжЊГСЕэжаNЁЂSЮяжЪЕФСПжЎБШМИКѕЮЊ1ЁУ1ЃЌЧвЛЙКЌгаCдЊЫиЃЌЫљвдИУЪЕбщжаВњЩњЕФзЉКьЩЋГСЕэЮЊ(SCN)xЁЃ
ЃЛЂлгЩЭМ1ПЩжЊЃЌЫцNaClO3МгШыЃЌpHдіДѓЃЌSCN-ЭбГ§ТЪУїЯддіДѓЃЌЖјБНЗгЭбГ§ТЪдіДѓВЛУїЯдЃЌЫљвдSCN-дкНЯЧПЫсадЬѕМўЯТБЛClO3-бѕЛЏСЫЃЛгЩЬтФПа№ЪіПЩжЊSCN-ПЩБЛФГаЉбѕЛЏМСЃЈШчCu2+ЕШЃЉбѕЛЏЮЊзЉКьЩЋЕФГСЕэЃЌClO3-ОпгаНЯЧПЕФбѕЛЏадЃЌгЩЭМЯѓ2ПЩжЊГСЕэжаNЁЂSЮяжЪЕФСПжЎБШМИКѕЮЊ1ЁУ1ЃЌЧвЛЙКЌгаCдЊЫиЃЌЫљвдИУЪЕбщжаВњЩњЕФзЉКьЩЋГСЕэЮЊ(SCN)xЁЃ


 ЯАЬтОЋбЁЯЕСаД№АИ
ЯАЬтОЋбЁЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвЛжжяЎЭПЩГфЕчЕчГиЃЌЙЄзїдРэШчЭМЁЃдкИУЕчГижаЃЌЗЧЫЎЯЕЕчНтвККЭЫЎЯЕЕчНтвКБЛяЎРызгЙЬЬхЕчНтжЪЬеДЩЦЌ(LISICON)ИєПЊЁЃЯТСаЫЕЗЈВЛе§ШЗЕФЪЧ
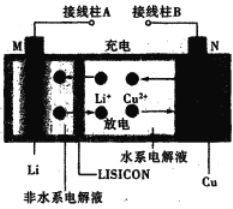
A. ЬеДЩЦЌдЪаэLi+ЭЈЙ§ЃЌВЛдЪаэЫЎЗжзгЭЈЙ§
B. ЗХЕчЪБЃЌNЮЊЕчГиЕФе§МЋ
C. ГфЕчЪБЃЌвѕМЋЗДгІЮЊЃКLi+ +e-=Li
D. ГфЕчЪБЃЌНгЯпжљAгІгыЭтНгЕчдДЕФе§МЋЯрСЌ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПГЃЮТЯТЃЌЯТСаИїзщРызгдкжИЖЈШмвКжаФмДѓСПЙВДцЕФЪЧ(ЁЁЁЁ)
A. ЮоЩЋЭИУїШмвКжаЃК Ca2ЃЋЁЂCu2ЃЋЁЂBrЃЁЂClЃ
B. ФмЪЙЗгЬЊБфКьЕФШмвКжаЃК KЃЋЁЂNaЃЋЁЂCO![]() ЁЂAlO
ЁЂAlO![]()
C. c(ClOЃ)ЃН1molЁЄLЃ1ЕФШмвКжаЃК Fe2ЃЋЁЂAl3ЃЋЁЂNO![]() ЁЂIЃ
ЁЂIЃ
D. ![]() ЃН0.1 molЁЄLЃ1ЕФШмвКжаЃК NH
ЃН0.1 molЁЄLЃ1ЕФШмвКжаЃК NH![]() ЁЂMg2ЃЋЁЂSO
ЁЂMg2ЃЋЁЂSO![]() ЁЂCH3COOЃ
ЁЂCH3COOЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПLEDВњЦЗЕФЪЙгУЮЊГЧЪадіЬэЩЋВЪЁЃгвЭМЪЧЧтбѕШМСЯЕчГиЧ§ЖЏLEDЗЂЙтЕФвЛжжзАжУЪОвтЭМЁЃЯТСагаЙиа№Ъіе§ШЗЕФЪЧЃЈ ЃЉ
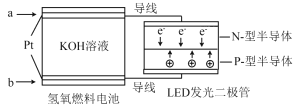
A. ИУзАжУНЋЛЏбЇФмзюжезЊЛЏЮЊЕчФм
B. bДІЮЊЕчГие§МЋЃЌЗЂЩњЛЙдЗДгІ
C. aДІЭЈШыO2
D. ЭЈШыO2ЕФЕчМЋЩЯЗЂЩњЕФЕчМЋЗДгІЮЊO2 ЃЋ4H+ ЃЋ4eЈCЃН2H2O
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПСђЫсУЬяЇОЇЬхПЩгУзїжЏЮяКЭФОВФМгЙЄЕФЗРЛ№МСЕШЁЃгЩЖўбѕЛЏУЬЕШзїдСЯжЦШЁСђЫсУЬяЇОЇЬхВНжшШчЯТЃК
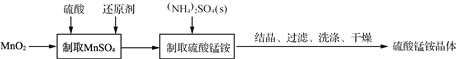
ЃЈ1ЃЉЪЕбщЧАЃЌашГЦСПMnO2ЕФжЪСПЃЌетЪЧвђЮЊ____________________________ЁЃ
ЃЈ2ЃЉ ЁАжЦШЁMnSO4ЁБЪБЃЌПЩгУC6H12O6(ЦЯЬбЬЧ)ЁЂH2C2O4(ВнЫс)ЕШЮяжЪзїЛЙдМСЁЃ
ЂйгУC6H12O6зїЛЙдМС(БЛбѕЛЏЮЊCO2)ЪБЃЌЗЂЩњЗДгІЕФn(MnO2)/n(C6H12O6)ЃН________ЁЃЁЁ
ЂкгУH2C2O4зїЛЙдМСЃЌЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНЮЊ____________________________ЁЃ
ЃЈ3ЃЉвЛжжВтЖЈСђЫсУЬяЇОЇЬх[ЩшЮЊЃК (NH4)xMny(SO4)zЁЄwH2O]зщГЩЕФЗНЗЈШчЯТЃК
ЂйГЦШЁвЛЖЈСПЕФСђЫсУЬяЇОЇЬхХфГЩ250 mLШмвКAЁЃ
ЂкШЁ25.00 mLШмвКAМгШызуСПЕФBaCl2ШмвКЕУBaSO4 0.512 6 gЁЃ
ЂлСэШЁ25.00 mLШмвКAМгШы10 mL 20%ЕФжаадМзШЉШмвКЃЌвЁдШЁЂОВжУ5 min[4NH![]() ЃЋ6HCHO===3HЃЋЃЋ6H2OЃЋ(CH2)6N4HЃЋЃЌЕЮЖЈЪБЃЌ1 mol(CH2)6N4HЃЋгы1 mol HЃЋЯрЕБ]ЃЌМгШы1ЁЋ2ЕЮЗгЬЊШмвКЃЌгУ0.100 0 molЁЄLЃ1 NaOHБъзМШмвКЕЮЖЈжСжеЕу(дкИУЙ§ГЬжаMn2ЃЋВЛГСЕэ)ЃЌЯћКФNaOHШмвК22.00 mLЁЃ
ЃЋ6HCHO===3HЃЋЃЋ6H2OЃЋ(CH2)6N4HЃЋЃЌЕЮЖЈЪБЃЌ1 mol(CH2)6N4HЃЋгы1 mol HЃЋЯрЕБ]ЃЌМгШы1ЁЋ2ЕЮЗгЬЊШмвКЃЌгУ0.100 0 molЁЄLЃ1 NaOHБъзМШмвКЕЮЖЈжСжеЕу(дкИУЙ§ГЬжаMn2ЃЋВЛГСЕэ)ЃЌЯћКФNaOHШмвК22.00 mLЁЃ
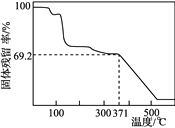
ЂмШЁвЛЖЈСПбљЦЗдкПеЦјжаМгШШЃЌбљЦЗЕФЙЬЬхВаСєТЪ(ЙЬЬхбљЦЗЕФЪЃгржЪСП/ЙЬЬхбљЦЗЕФЦ№ЪМжЪСПЁС100%)ЫцЮТЖШЕФБфЛЏШчгвЭМЫљЪО(бљЦЗдк371 ЁцЪБвбЭъШЋЪЇШЅНсОЇЫЎ)ЁЃИљОнвдЩЯЪЕбщЪ§ОнМЦЫуШЗЖЈСђЫсУЬяЇОЇЬхЕФЛЏбЇЪН(аДГіМЦЫуЙ§ГЬ)ЁЃ__________________
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЩњЮяВёгЭЪЧвЛжжгУжВЮягЭЁЂЖЏЮягЭЛђЗЯЦњгЭжЌЕШЮЊдСЯМгЙЄЖјГЩЕФЧхНрШМСЯЃЌжївЊГЩЗжЮЊИпМЖжЌЗОЫсМзѕЅЁЃвЛжжгУВЫзбгЭЕШЮЊдСЯжЦБИЩњЮяВёгЭЕФЪЕбщВНжшШчЯТЃК
ЂйЯђгвЭМЫљЪОЕФШ§ПкЩеЦПжаМгШы3.2 g CH3OHЁЂ0.2 g NaOHЃЌШмНтКѓЯђЦфжаМгШы20 g(0.021ЁЋ0.023 mol)ВЫзбгЭМА60 mLе§МКЭщЁЃ

ЂкМгШШжС60ЁЋ65 ЁцЃЌНСАш2.5ЁЋ3 hЃЌОВжУЁЃЩЯВуЮЊЩњЮяВёгЭЁЂе§МКЭщМАМзДМЃЌЯТВужївЊЮЊИЪгЭЁЃ
ЂлЗжвКЁЂЫЎЯДЁЃ
ЂмеєСѓЃЌБЃГж120ЁцЪБжСЮовКЬхСїГіЃЌЪЃгрЮяЮЊЩњЮяВёгЭЁЃ
ЃЈ1ЃЉВНжшЂйжаПижЦn(CH3OH)/n(гЭжЌ)ЃО3ЕФФПЕФЪЧ________ЃЛе§МКЭщЕФзїгУЪЧ________ЁЃ
ЃЈ2ЃЉВНжшЂкЪЪвЫЕФМгШШЗНЪНЪЧ________ЃЛВЫзбгЭЕФГЩЗжжЎвЛгЭЫсИЪгЭѕЅ(НсЙЙМђЪНШчгвЭМ)гыМзДМЗДгІЕФЛЏбЇЗНГЬЪНЮЊ________________________________________________ЁЃ
ЃЈ3ЃЉВНжшЂлгУЗжвКТЉЖЗЗжРыЪБЃЌЛёШЁЩЯВувКЬхЕФЗНЗЈЪЧ________ЃЛгУЫЎЯДЕгЩЯВувКЬхЪБЃЌЫЕУївбЯДЕгИЩОЛЕФвРОнЪЧ__________________________________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаИїзщРызгдкЭЌвЛШмвКжавЛЖЈФмДѓСПЙВДцЕФЪЧ(ЁЁЁЁ)
A. КЌДѓСПBa2ЃЋЕФШмвКжаЃКClЃЁЂKЃЋЁЂSO![]() ЁЂCO
ЁЂCO![]()
B. КЌДѓСПHЃЋЕФШмвКжаЃКMg2ЃЋЁЂNaЃЋЁЂCO![]() ЁЂSO
ЁЂSO![]()
C. КЌДѓСПOHЃЕФШмвКжаЃКKЃЋЁЂNOЁЂSO![]() ЁЂCu2ЃЋ
ЁЂCu2ЃЋ
D. КЌДѓСПNaЃЋЕФШмвКжаЃКHЃЋЁЂKЃЋЁЂSO![]() ЁЂNO
ЁЂNO
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЫЕЗЈе§ШЗЕФЪЧ( )
AЃЎдіДѓЗДгІЮяХЈЖШПЩдіДѓЛюЛЏЗжзгАйЗжЪ§ЃЌЫљвдЗДгІЫйТЪдіДѓ
BЃЎЗХШШЗДгІЕФЗДгІЫйТЪвЛЖЈДѓгкЮќШШЗДгІЕФЗДгІЫйТЪ
CЃЎЗДгІNH3(g) + HCl(g)![]() NH4Cl(s)дкЪвЮТЯТПЩздЗЂНјааЃЌдђИУЗДгІЕФЁїHЃМ0
NH4Cl(s)дкЪвЮТЯТПЩздЗЂНјааЃЌдђИУЗДгІЕФЁїHЃМ0
DЃЎЖдгкЗДгІX(s)ЃЋaY(g)![]() bZ(g)ЃЋW(g) ЁїHЃО0ЃЌЩ§ИпЮТЖШЃЌе§ЗДгІЫйТЪдіДѓЃЌФцЗДгІЫйТЪМѕаЁ
bZ(g)ЃЋW(g) ЁїHЃО0ЃЌЩ§ИпЮТЖШЃЌе§ЗДгІЫйТЪдіДѓЃЌФцЗДгІЫйТЪМѕаЁ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЪТЪЕВЛФмгУРеЯФЬиСадРэНтЪЭЕФЪЧЃЈ ЃЉ
A. FeCl3+3KSCN![]() Fe(SCN)3+3KClЦНКтЬхЯЕжаМгШыЩйСПKSCNЙЬЬхЃЌШмвКбеЩЋМгЩю
Fe(SCN)3+3KClЦНКтЬхЯЕжаМгШыЩйСПKSCNЙЬЬхЃЌШмвКбеЩЋМгЩю
B. ЙЄвЕКЯГЩАБжаЃЌНЋАБЦјвКЛЏЗжРы
C. AЁЂBСНжЇЪдЙмжаЗжБ№МгШыЕШЬхЛ§5%ЕФH2O2ШмвКЃЌдкBЪдЙмжаМгШы2ЁЋ3ЕЮFeCl3ШмвКЃЌBжаЪдЙмжаВњЩњЦјХнПь
D. ЖдгкЗДгІ2NO2(g)![]() N2O4(g) ЁїH<0ЃЌЩ§ИпЮТЖШПЩЪЙЬхЯЕбеЩЋБфЩю
N2O4(g) ЁїH<0ЃЌЩ§ИпЮТЖШПЩЪЙЬхЯЕбеЩЋБфЩю
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com