
����Ŀ����������Ԫ�أ�����B��C��D��EΪ����������Ԫ�أ�F��GΪ��������Ԫ�أ����ǵ�ԭ����������������������������Ϣ���ش�����
BԪ��ԭ�ӵĺ���p��������s��������1 |
Cԭ�ӵĵ�һ�����ĵ����ֱܷ��ǣ�I1=738kJ/mol I2=1451kJ/mol I3=7733kJ/mol I4=10540kJ/mol |
Dԭ�Ӻ�������p���ȫ������� |
EԪ�ص����������������������4 |
F ��ǰ������ԭ�ӵ����Ų�ͼ�е�����������Ԫ�� |
G�����ڱ��ĵ�ʮһ�� |
��1��B��̬ԭ�ӵĵ����Ų�ʽΪ��F��̬ԭ�ӵļ۵����Ų�ʽΪ��G��̬ԭ�ӵ����������Ų�ͼΪ ��
��2��C��������������Ԫ��ԭ�ӵĵ�һ�������ɴ�С��˳��������Ԫ�ط�����գ���
��3��B��D�ĵ縺����Դ�С��BD���á����ڡ�����С�ڡ����ڡ���գ���
��4����������Ԫ���У�λ��s�������֣�λ��p�������֣�
��5��DE3�ĵ���ʽΪ ��
���𰸡�
��1��1s22s22p3��3d54s1�� ![]()
��2��Mg��Al��Na
��3������
��4��1��4
��5��
���������⣺��1��BΪNԪ�أ�ԭ�Ӻ�������Ų�Ϊ1s22s22p3��FΪCr����̬ԭ�ӵļ۵����Ų�ʽΪ3d54s1��GΪGa���������3�����ӣ���̬ԭ�ӵ����������Ų�ͼΪ ![]() ���ʴ�Ϊ��1s22s22p3��3d54s1��
���ʴ�Ϊ��1s22s22p3��3d54s1�� ![]() ����2��CΪMgԪ�أ������Ϊȫ��������Ϊ�ȶ�����һ�����ܴ�С˳��ΪMg��Al��Na���ʴ�Ϊ��Mg��Al��Na����3��ͬ����Ԫ�ش��ϵ��µ縺����С����N����P���ʴ�Ϊ�����ڣ���4����������Ԫ���У�Mgλ��s����N��P��Cl��Gaλ��p������4�֣��ʴ�Ϊ��1�� 4����5��PCl3Ϊ���ۻ��������ʽΪ
����2��CΪMgԪ�أ������Ϊȫ��������Ϊ�ȶ�����һ�����ܴ�С˳��ΪMg��Al��Na���ʴ�Ϊ��Mg��Al��Na����3��ͬ����Ԫ�ش��ϵ��µ縺����С����N����P���ʴ�Ϊ�����ڣ���4����������Ԫ���У�Mgλ��s����N��P��Cl��Gaλ��p������4�֣��ʴ�Ϊ��1�� 4����5��PCl3Ϊ���ۻ��������ʽΪ  ���ʴ�Ϊ��
���ʴ�Ϊ��  ��
��
BԪ��ԭ�ӵĺ���p��������s��������1��ԭ�Ӻ�������Ų�Ϊ1s22s22p3����BΪNԪ�أ�
��Cԭ�ӵĵ�һ�����ĵ��������ݿ�֪�����������ܾ�������C����+2�ۣ����ڢ�A�壬ԭ����������NԪ�أ���CΪMgԪ�أ�
D���ڵ������ڣ�Dԭ�Ӻ�������p���ȫ���������������Ų�Ϊ3s23p3����DΪPԪ�أ�
E���ڵ������ڣ�EԪ�ص������������������IJ�Ϊ4��E���ڵڢ�A�壬��EΪClԪ�أ�
F��ǰ������ԭ�ӵ����Ų�ͼ�е�����������Ԫ�أ���Χ�����Ų�Ϊ3d54s1����Ԫ��ΪCr��
G�ڵ����������ڱ��ĵ�11�У�GΪGaԪ�أ��Դ˽����⣮


 ���ٴ�����ɽ����ϵ�д�
���ٴ�����ɽ����ϵ�д� ���ٴ���������ѧϰ����ѧ�ں����ν�ϵ�д�
���ٴ���������ѧϰ����ѧ�ں����ν�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������һ�ַdz����õĽ���Ԫ�أ��䵥�ʼ��������ڿ��С�������������Ҫ���ã�
��1�����ý����ƺ�CO2��Ӧ���Ʊ����ʯ������ط�Ӧ���Ȼ�ѧ����ʽ���£� 4Na��g��+3CO2��g���T2Na2CO3��l��+C��s�����ʯ����H=a kJmol��1
CO2��g��+4Na��g���T2Na2O��s��+C��s�����ʯ����H=b kJmol��1
��Ӧ6Na2O��s��+2C��s�����ʯ���T8Na��g��+2Na2CO3��l���ġ�H=kJmol��1���ú�a��b�Ĵ���ʽ��ʾ����
��2��T��ʱ�����Ϊ2L�ĺ��������м���һ������Na2SO4������������������·�Ӧ�� Na2SO4��s��+4H2��g��Na2S��s��+4H2O��g����
���������¶ȣ�Kֵ��С����Ӧ�ġ�H0�������������
������˵��������� ��
A������Na2SO4��s�������ɼӿ췴Ӧ����
B�������������ܶ�һ��ʱ���÷�Ӧ�ﵽƽ��״̬
C�������¶Ȳ��䣬��ƽ����ϵ����ͨ��һ������H2 �� ��H����
D�������������䣬�����¶ȣ���v����������v���棩��С��ƽ������
����2min�ڷ�Ӧ�ﵽƽ�⣬��ʱ��������������8g������H2��ʾ�ķ�Ӧ����Ϊ����֪��Ӧ������H2�����������ʱ��Ĺ�ϵ����ͼ��ʾ����T���¸÷�Ӧ��ƽ�ⳣ��Ϊ ��
������Ӧ��ƽ�����һ������H2 �� �ٴ�ƽ���H2O������������������С�����䡱����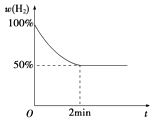
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪���ڵ��볣��ΪKa��ijһԪ����ζ������У�pHͻ������Ũ�ȵ������������Ũ����ҪӰ��ζ��յ�͵ζ��յ�֮������߲��֡������£��ò�ͬŨ�ȵ�NaOH��Һ�ֱ�ζ�20mL����ͬŨ�ȵ�ij����HA��Һ���ζ�������ͼ��ʾ������˵������ȷ����

A. ��ͼ��֪��c1>c2>c3
B. M����Һ�д���:c(H+)+c(HA)=c(OH-)+c(A-)
C. ǡ���к�ʱ����Һ������Ũ�ȵĴ�С��ϵ: c(Na+)>c(A-��>c(OH-)>c(H+)
D. ��pH=7��Һ�����: ![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͼ����һ���������ォ��ˮ�е�����CO(NH2)2]ת��Ϊ�����Ѻ����ʵ�ԭ��Ҳװ��ʾ��ͼ�����øõ����ͼ��װ���е����϶�ͭ������˵����ȷ����
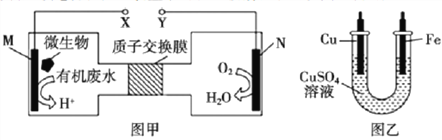
A. ͼ����Fe�缫Ӧ��ͼ����Y������
B. ͼ����H+�����ӽ���Ĥ���������ƶ�
C. ͼ����M�缫��Ӧʽ��CO(NH2)2+5H2O-14e=CO2+2NO2+14H+
D. ��ͼ����M�缫����0.5mol����ʱ��ͼ�������缫����96g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CuCl������ӡˢ����̪ݼ������Ҫԭ�ϣ���ҵ�Ͽ���һ�ֵ�Ʒλͭ��(��Ҫ�ɷ�CuS��Cu2S��CuO��Fe2O3��FeO������������������)�����̿�(��Ҫ�ɷ�ΪMnO2������������������)����������������������

�ش�����������
��1���������з�Ӧ�϶������з�Ӧ������֮һ��Cu2S+2MnO2+4H2SO4=2CuSO4+2MnSO4+4H2O+S���÷�Ӧ����������Ϊ____________________(�ѧʽ)��
��2��Ϊȷ����Һ1���Ƿ���Fe2+���������л���ȡ����ȥ��Һ��MnSO4����ȡ�²�ˮ��Һ���м���������Լ�Ϊ_____________________��
��3�����������백ˮ������Һ��pHΪ5������Ŀ����______________________��
��4��Ϊģ�ⲽ����������������ijͬѧ�������ʵ�飬�����й�������ȷ����_____________��

A.aͨ��CO2��Ȼ��bͨ��NH3��c�зż�ʯ��
B.bͨ��NH3��Ȼ��aͨ��CO2��c�зż�ʯ��
C.aͨ��NH3��Ȼ��bͨ��CO2��c�з�պϡ�������֬��
D.bͨ��CO2��Ȼ��aͨ��NH3��c�з�պϡ����|����֬��
��5������������Һ����Ҫ�ɷ�X�Dz������Ͳ��������еIJ��������Ի�����Ϊ����ʹ�ã��÷���_______(����������������������)���ľ��(��Ч�ɷ�K2CO3)����������ԭ����__________��
��6����֪CuClΪ������ˮ�İ�ɫ������д��������������Ӧ�����ӷ���ʽ��_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ںϳɻ��ʣ���ũҵ��Ӧ�ù㷺�����й��ڰ������ʵ���������ȷ����
A. ��ɫ B. ������ C. �ܶȱȿ���С D. ��������ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����÷�Ӧ6NO2+8NH3=7N2+12H2O���ɵ�صķ���������ʵ����Ч��������������ŷţ����ỷ����Ⱦ�����ܳ�����û�ѧ�ܣ�װ����ͼ��ʾ������˵����ȷ���ǣ������� 
A.�缫BΪ����
B.�缫A�ķ�ӦʽΪ2NH3��6e��+6OH��=N2+6H2O
C.��Һ��OH��ͨ�������ӽ���Ĥ��������Ǩ��
D.����4.48LNO2����״���£�������ʱ��ת�Ƶĵ���Ϊ0.4mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����4.6 g��Ͷ�뵽95.4gˮ�У�������Һ�����ʵ���������(����)
A.����4.6%B.����8%
C.����8%D.��8%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ̽����������Է�Ӧ��mA��g��+nB��g��cZ��g����H ��Ӱ�죬��A��B���ʵ���֮��Ϊm��n��ʼ��Ӧ��ͨ��ʵ��õ���ͬ�����´ﵽƽ��ʱZ�����ʵ���������ʵ������ͼ��ʾ�������ж���ȷ���� ��������
A.�ں��º�ѹ�����£����Ѵﵽƽ�����ϵ�м�������Z������ƽ ��ʱ��Z�����ʵ�����������
B.�����¶ȣ������淴Ӧ���ʶ�����ƽ�ⳣ������
C.��H��0��m+n��c
D.�¶Ȳ��䣬����ѹǿ��ƽ�������ƶ�������ƽ��ʱ��A��Ũ�ȱ�ԭƽ���С
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com